 Aminosyrer er byggestenene i levende ting. Lange kæder af aminosyrer udgør proteiner, som igen udgør mange strukturelle og funktionelle cellekomponenter.
Aminosyrer er byggestenene i levende ting. Lange kæder af aminosyrer udgør proteiner, som igen udgør mange strukturelle og funktionelle cellekomponenter.
Jeg kan godt lide at tænke på cellen som en selvstændig by, hvor kernen er hovedstaden, mitokondrierne er kraftværket og så videre. Men så har du dine arbejdere, transportsystem og selve strukturen i cellebyen, som alle er lavet af proteiner – som igen er lavet af aminosyrer.,
kompleksiteten af en proteinstruktur bestemmes af dens sekvens af aminosyrer og den kemiske karakter af deres variable gruppe sidekæder. Den MCAT kræver forståelse af, polære og upolære sidekæder og vride og protein, der er forårsaget af hydrofobe og hydrofile interaktioner
Og ja, du skal være lagrer hver aminosyre for MCAT. Dette omfatter sidekæden, fulde navn, 3 bogstaver navn og enkelt bogstav forkortelse. Men du behøver ikke blot holde ord og strukturer på flashcards i håb om at tvinge det ind i din hukommelse., Du skal aktivt tackle hver aminosyre individuelt.
For en hurtig reference liste downloade min gratis Amino Syre Cheat Sheet studievejledning
- Skriv det fulde navn
- Trække aminosyre struktur og variabel-gruppen
- Skriv de 3-brev og enkelt bogstav forkortelser
- Ord på noget unikt ved denne specifikke side chain – out loud! Jo mere sjov og skør forbindelsen er, jo lettere vil du huske det.,
- Gentag navngivning/tegning proces, når HØJRE VÆK
- Gentag hver uge, indtil du føler dig FAST med denne information
Den Grundlæggende Struktur af en aminosyre
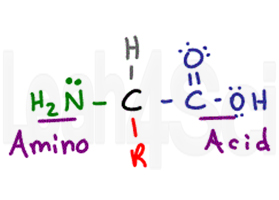 aminosyren får sit navn fra dens to primære funktionelle grupper. Aminosyren har en central chiral carbon kaldet alpha carbon (sort). Vedhæftet til det centrale kulstof har du et hydrogenatom (Grå), en amino-eller NH2-gruppe (grøn) og en Carbo .ylsyre COOH-gruppe (lilla). Endelig har vi R-gruppen (rød), som er en variabel sidekæde.,
aminosyren får sit navn fra dens to primære funktionelle grupper. Aminosyren har en central chiral carbon kaldet alpha carbon (sort). Vedhæftet til det centrale kulstof har du et hydrogenatom (Grå), en amino-eller NH2-gruppe (grøn) og en Carbo .ylsyre COOH-gruppe (lilla). Endelig har vi R-gruppen (rød), som er en variabel sidekæde.,
der er 20 forskellige aminosyrer kendetegnet ved deres unikke sidekæder. De spænder fra et simpelt hydrogenatom (glycin) til et komplekst 2-ring resonerende aromatisk system (tryptophan).mens den fuldt neutrale version Ovenfor er, hvordan de fleste studerende studerer aminosyrer, og den form, vi bruger i denne artikel, skal du huske, at dette er teknisk ukorrekt.
aminosyre i Amino .itterionform
da Carbo .ylgruppen er sur og aminogruppen basisk, vil de to eksistere som en..itterion i deres konjugerede ladede former i fysiologisk pH., Mere om charges .itterion og aminosyre afgifter i min næste artikel (link til at følge).
et sidste koncept, før vi nedbryder de individuelle aminosyrer, og det er den 3-dimensionelle proteinstruktur. I et biologisk system bestemmer strukturen funktion, så forståelse af aminosyreegenskaber er nøglen til forståelse af struktur og i sidste ende proteinfunktion.
primær struktur af et 3-D-Protein
Den første og mere vigtige bestemmelsesfaktor for proteinstruktur er sekvensen af aminosyrer., Hvis polypeptidkæden er fastgjort i en anden rækkefølge, får du en meget anden overordnet struktur.
sekundær struktur af et 3-D-Protein
den sekundære struktur kommer fra rygrad hydrogenbindingsinteraktioner. Peptidbindingen omdanner hver tidligere Carbo .yl-og aminogruppe til en amidfunktionel gruppe. Den sekundære struktur af alfa-Heli.og beta-plisserede plader kommer fra hydrogenbinding mellem det delvist negative ilt på carbonyl og det delvist positive hydrogen på nitrogenet.,
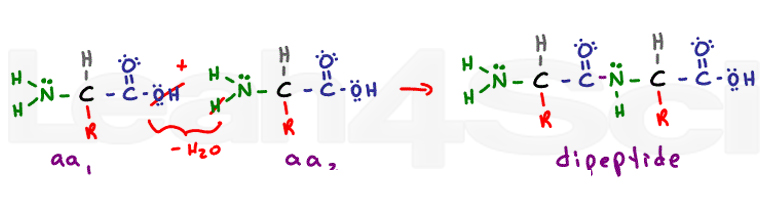
tertiær struktur af et 3-D-Protein
den tertiære struktur er, hvor den virkelige 3-dimensionelle foldning introduceres, og det er første gang, du vil bemærke sidekædeinteraktioner. Det er her viden og forståelse af aminosyresidekæder er kritiske.
Lad mig gentage mig selv, tertiær struktur er første gang, du ser variable R-gruppe sidekædeinteraktioner på polypeptidkæden. Mange studerende forveksler dette med sekundær struktur, som kun er rygradsinteraktioner.,
kvaternær struktur af et 3-D Multi-Polypeptidprotein
kvaternær struktur refererer til de variable gruppeinteraktioner mellem forskellige polypeptider for at danne et enkelt større protein.
kvaternære strukturer findes ikke i hvert protein. Hvis proteinet kun indeholder en enkelt aminosyrestreng, er det højeste niveau af foldning dets tertiære struktur. Hvis proteinet imidlertid består af flere polypeptidunderenheder, er den kvartære struktur det, der holder de forskellige polypeptider sammen.,
nu hvor du forstår betydningen af sidekædeegenskaber, lad os dykke ind i aminosyrer. Husk, at da forældrenes amino – og Carbo .ylgrupper er ‘optaget’ med primær/sekundær struktur, analyseres de ikke, når de studerer sidekædeegenskaber og egenskaber.
dette betyder, at du ignorerer enhver potentiel polaritet på både Carbo .yl-og aminogrupperne og kun ser på sidekæderne.
ikke-polære hydrofobe aminosyrer
hydrofob, som navnet antyder, er hydro – vand, fobisk frygt., Hydrofobe aminosyrer har ringe eller ingen polaritet i deres sidekæder. Manglen på polaritet betyder, at de ikke har nogen måde at interagere med meget polære vandmolekyler, hvilket gør dem vandfrygtige.
Der er kun fem atomer, der vises i dine aminosyrevariabelgrupper: H, C, N, O og S.
overvej kun polaritet, når du har N, O, S som ‘majoritetsfaktoren’. Jeg vil påpege disse, når de forekommer. Men hvis alt hvad du ser er Cs og Hs, skal du automatisk genkende en vandfrygtig aminosyre.,
GlycineGlyG
glycin er en unik aminosyre, idet den ikke rigtig har en R-gruppe. Når du tænker ‘variabel R-gruppe’, skal du tænke på kulstof knyttet til andre atomer. Men glycin har kun et brint i sin sidekædeposition. Da glycin har 2 hydrogenatomer, en hver på forælder-og sidekæden, er det den eneste symmetriske og dermed achirale aminosyre. Da hydrogen er ikke-polær, er glycin en hydrofob aminosyre. Brint sidekæden gør glycin til den mindste aminosyre.,
AlanineAlaA
alanin er en simpel aminosyre, der kun har en methyl-eller CH3-gruppe som sidekæde. Da du ikke ser andet end kulstof og brint, er alanin en ikke-polær hydrofob aminosyre. Det er vigtigt at erkende, at dette er en meget lille aminosyre og i stand til at blive ‘klemt’ i stramme sløjfer eller kæder.
ValineValV
valin er en anden simpel aminosyre med blot en isopropyl variabel gruppe. Ligesom alanin ser vi intet andet end kulstof og brint, hvilket gør valin til en ikke-polær hydrofob aminosyre.,
LeucineLeuL
Du kan genkende leucin som den samme variable gruppe som valin, men med en ekstra CH2-gruppe. Eller du kan blot genkende dens isobutyl sidekæde.
se denne video, hvis du ikke er bekendt med forgrenede sidekæder som isopropyl eller sec-butyl. Da leucin kun har Cs og Hs, er det en vandfrygtig ikke-polær aminosyre.
IsoleucineIleI
isoleucin, som navnet antyder, er en isomer af leucin. Forskellen er placeringen af CH3 i en sec-butyl snarere end en isobutyl sidekæde. Ligesom dens isomer er isoleucin ikke-polær og hydrofob.,
MethionineMetM
methionin er den første potentielt vanskelige aminosyre. Det er sidekæde indeholder for det meste Cs og Hs, men med et indlejret svovlatom. Mens du måske synes, det er hydrofil, skal du være opmærksom på svovlatomets placering. Indlejret i kæden og fastgjort til bare carbonatomer, er svovl delvist ‘skjult’ fra det ydre miljø.
mens du ikke behøver at kende elektronegativitetsværdier for MCAT hjælper det med at forstå, at s = 2.58 og C = 2.55. Da forskellen i elektronegativitet er mindre end 0,5, er der ingen polaritet på denne sidekæde.,
du skal også genkende methionin som startkodon AUG i RNA-oversættelse til proteiner.
PhenylalaninePheF
for at hjælpe dig med at huske, at phenylalanin er F, skal du huske, at ‘ph’ udtales som et ‘f’. Bland ikke dette op med P for proline.
Vær opmærksom på strukturen af phenylalanin. Den har en enkelt carbongruppe med en vedhæftet ben .enring. Phenyl er navnet på en ben .ensubstituent, og dette molekyle har en ben .en (phenyl) bundet til strukturen af alanin. Da phenylalanin kun har Cs og Hs i sin aromatiske sidekæde, er det ikke-polært og hydrofobt.,
Tryptophantrp.
Dette er en vanskelig. Bemærk N-H i denne sidekæde. N-H skal være polær og kunne binde brint. Der er dog to grunde til, at denne aminosyre stadig er ikke-polær og hydrofob.
- n-H-gruppen er en lille del af den meget store sidekæde.
- se nøje på nitrogen, og endnu vigtigere, på sine ensomme par. Nitrogen ‘ s elektroner er integreret i den konjugerede aromaticitet for tryptophan sidekæden., Med andre ord, tænk på dets elektroner som ‘for distraheret’ af resonans for at være meget opmærksom på det ydre vandmiljø.
MCAT kræver, at du erkender, at dette er en stor og voluminøs aminosyre. Men da det er en multiple choice-eksamen, kan du simpelthen huske, at tryptophan er den eneste aminosyre med to smeltede ringe.
faktisk er det så stort, at det kan Trippe (trp) over sig selv og råbe Waaaaaaa (
(Note om mnemonics: jo sjovere, mere skræmmende eller snavset mnemonic, jo mere sandsynligt vil du huske det. Husk dette for medicinskolen.,)
ProlineProP
prolin er en unik aminosyre, da den er den eneste, der inkorporerer rygraden i sin sidekæde. Prolin-sidekæden er en 3-carbon kæde, der løber rundt og fastgøres tilbage til den overordnede aminogruppe. Dette betyder, at prolin i modsætning til de andre aminosyrer ikke har et hydrogenatom på dets nitrogen, når det er en del af en polypeptidkæde.
Du kan dog ikke glemme, at nitrogen ikke rigtig er en del af den variable gruppe, hvilket betyder, at det ikke kan bidrage med nogen polaritet. Da vi lige har 3 CH2-grupper til at analysere, får vi en ikke-polær hydrofob sidekæde., Denne forældresløjfe skaber en bule og tillader ikke, at en prolinholdig kæde er lineær, hvilket betyder, at du ofte finder den i sløjfer og i slutningen af en alfa-Heli..
polære hydrofobe aminosyrer
*Dette er en klæbrig sektion, og afhængigt af hvor du undersøger, kan du finde følgende kategoriseret som polær eller ikke-polær, hydrofil eller hydrofob. Vær opmærksom på tilstedeværelsen af polære grupper, der er små sammenlignet med den samlede sidekæde, eller meget svagt polær og derfor hydrofob.,
CysteineCysC
cystein har en let polær S-H, men dens polaritet er så mild, at cystein ikke er i stand til korrekt at interagere med vand, hvilket gør det hydrofobt.
cystein er en meget vigtig aminosyre, når det kommer til tertiær og kvaternær struktur. De fleste Side-chain interaktioner omfatter polære/ladede interaktioner eller ikke-polære Van der Deraals og London dispersion. Cysteins sidekæde er imidlertid i stand til at danne en disulfidbro, som er en kovalente bindinger mellem 2 svovlatomer gennem sidekædeo .idation og fjernelse af 2 hydrogenatomer., Denne kovalente binding er meget stærkere og mere permanent sammenlignet med de almindelige tertiære og kvaternære interaktioner.
dette er også årsagen til eksperimentel fejl ved bestemmelse af proteinstørrelse/længde for proteiner med flere underenheder.
TyrosineTyrY
Nogle studerende ser dette som OH lækker fra et dæk (tyr).
se nærmere på tyrosin. Hvad ser du? Det ligner den aromatiske phenylalanin med en OH-gruppe I para-positionen (ortho/meta/para 2.video).,
På den ene side har vi en meget polær og hydrogenbindingsdygtig OH-gruppe, men på den anden side er OH lille sammenlignet med størrelsen af ben .ylgruppen (CH2-phenyl). Dette conundrum er en almindelig kilde til forvirring, men hvis du forstår dette, vil du erkende, at tyrosin, mens polær, stadig er en hydrofob aminosyre.
polære hydrofile aminosyrer
hydrofile som navnet antyder kommer fra hydro-vand og filisk – elskende.
polaritet kommer fra en 0,5-1,9 forskel i elektronegativitet mellem bundne atomer., Selvom du ikke behøver at kende disse værdier for MCAT, skal du erkende, at polære bindinger vil eksistere, når N og O er bundet til ikke-carbonatomer.
elektronegativitetsforskellen er nok til at skabe en lille adskillelse af ladning eller polaritet. Og da ligesom tiltrækker ligesom, disse delvist ladede grupper vil blive tiltrukket af modsat ladede eller delvist ladede grupper såsom vand. Disse grupper vil vride polypeptidkæden for at interagere med hinanden og med vand.
hydrofobe grupper vil vride sig væk fra disse sidekæder.,
SerineSerS
tænk på serin som alanin med en OH-gruppe knyttet. I modsætning til tyrosin er OH størstedelen i dette molekyle, og dets polaritet er nok til at påvirke hele gruppen. Dette gør serien polær og meget hydrofil.
ThreonineThrT
Der er flere måder at se på denne gruppe. Du kan tænke på det som serin med en ekstra methylgruppe eller som valin, men med en OH, der erstatter en af methylgrupperne. Jeg husker THREEonine som havende 3 forskellige grupper: CH, CH3, og OH.
ligesom serin er denne variable gruppe polær og hydrofil.,
AsparagineAsnN
prøv dette: Slur din tale som du siger ‘asparagin’ virkelig hurtigt. Det lyder som om du siger som…N, hvilket er, hvordan jeg husker forkortelsen 3 bogstaver for denne aminosyre. NH2 i slutningen af dette molekyle får dig til at tænke ‘base’, men se på det er nabo. NH2 nær en carbonyl danner et amid, som ikke kan lide at virke som en syre eller base under standard fysiologiske forhold. Imidlertid, med partielle ladninger og H-bindingsevne ved både carbonylo .ygen og NH2-grupperne, vi får en polær hydrofil aminosyre.,
Glutaminegln.
Jeg tænker på begge ‘glut’ aminosyrer som gluttons, der har ‘forbrugt’ en ekstra CH2-gruppe. Glutamin har den samme struktur som asparagin, men med en ekstra glutton CH2 i sin kæde. Ligesom asparagin er det polært og hydrofil.
sure og basiske Aminosyresidekæder
surhed og basicitet i aminosyrer er endnu en kilde til forvirring blandt studerende. Hvis det starter som en syre, bliver det så en base? Hvordan finder jeg afgiften? Og så videre.
Her er tricket: en Carbo .ylsyre i sidekæden giver dig en sur aminosyre., Når en Carbo .ylgruppe deprotoneres, får du et konjugatbasisalt. Så hvis du ser saltversionen af en Carbo .ylsyresidekæde, mens den teknisk set er en ‘konjugatbase’, vil vi blot henvise til den som saltversionen af den sure aminosyre. Samme for basen. Hold øje med’ ikke-distraherede ‘ nitrogenatomer i sidekæden.
sure aminosyrer
de sure aminosyrer skal se meget velkendte ud sammenlignet med asparagin og glutamin. Og det skyldes, at alt om dem er det samme bortset fra terminalfunktions-gruppen., Amider (diskuteret ovenfor) er polære, men hvis NH2 byttes til en OH-gruppe, får du en sur Carbo .ylgruppe.
asparaginsyre / AspartateAspD
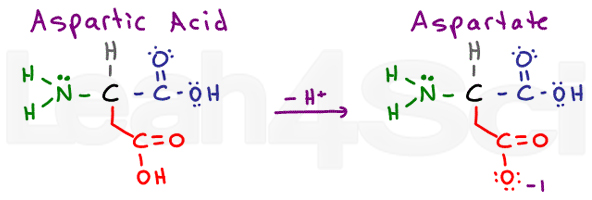
asparaginsyre refererer til protoniserede sure form af aminosyrer. Når deprotoneret, vil du ofte se konjugatbasisaltet kaldet aspartat. Dette er standardnomenklaturen for Carbo .ylsyrer.
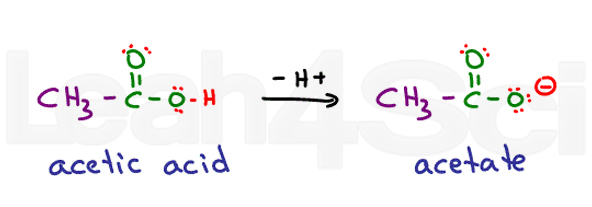
tænk på ethansyre. Dets almindelige navn er eddikesyre. Når deprotoneret får du acetat., Syrer er meget stabile i vand, da de er delvist ladede i deres protonerede form og fuldt ladede i deres deprotonerede form. Dette gør dem meget hydrofile.
glutaminsyre/GlutamateGluE
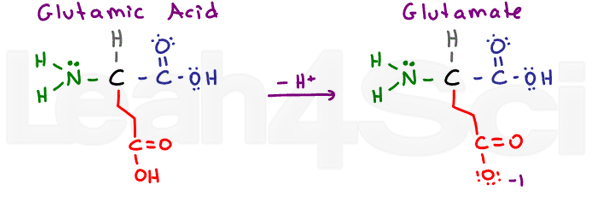
endnu en gang har vi en ‘glutton’ aminosyre med en ekstra CH2-gruppe. Glutaminsyre henviser til den protonerede sure form, og glutamat henviser til den deprotonerede konjugatbase/saltform.
ligesom asparaginsyre er glutaminsyre meget stabil i vand og dermed hydrofil.,
basiske aminosyrer
basiske aminosyrer indeholder et nitrogenatom med et ensomt elektronpar, der er i stand til at angribe et hydrogenatom. Når en basisk aminosyre udsættes for en lav (sur) pH, vil den gribe en af de frie protoner i opløsning for at danne et konjugatsyresalt. Disse genkendes let af det positive nitrogen i sidekæden. I modsætning til de sure aminosyrer er der ingen ‘almindeligt anvendte navne’ til at huske for disse konjugatsalte.
LysineLysK
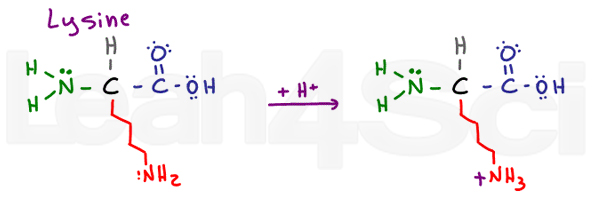
lysin er en simpel basisk aminosyre., På trods af en lang og potentielt hydrofob kæde har den en grundlæggende NH2 i slutningen. I sin grundlæggende deprotonerede form er lysin neutral og hydrofil; men hvis den findes i fysiologisk pH, vil lysin afhente en H+ fra opløsning til dannelse af et NH3+ salt. Salte er opladet, og derfor helt sikkert hydrofile
ArginineArgR
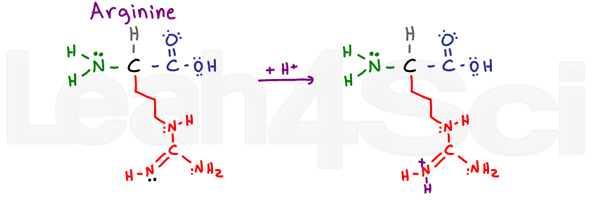
Arginin er forvirrende og får mig til at sige ARGh eller R for kort. Hvorfor? Den grundlæggende del af denne variable gruppe består af en NH, C=N-h og NH2.,
de 2 enkeltbundne nitrogenatomer kan bruge deres ensomme par til at resonere med det kulstof-og dobbeltbundne nitrogenatom. Dette gør deres elektroner utilgængelige for at fungere som en base. Imidlertid bruger det dobbeltbundne nitrogen sin pi-binding til at resonere, hvilket efterlader sit frie ensomme par (vist i sort) til at fungere som det grundlæggende nitrogen i denne gruppe.
Argh!
HistidineHisH

histidin er en anden vanskelig base af samme grund som arginin. Hvilket nitrogen er det grundlæggende? Se på tegningen her, især på de ensomme par på de 2 nitrogenatomer., Histidinringen er en heterocyklisk aromatisk forbindelse. Det øvre nitrogenatom har ikke en pi-binding. Dette betyder, at det skal bruge sine ensomme par til at deltage i resonans.
det lavere nitrogenatom har allerede en resonerende pi-binding. Dette efterlader sine ensomme elektroner (vist i sort) fri til at gribe en proton, hvilket gør dette til det grundlæggende atom.
afslutningsvis
aminosyrer er en kritisk komponent til biologiske strukturer og til din forståelse af biologi og biokemi på MCAT., Og så, som du forsøger at huske alt om disse 20 aminosyrer, er det vigtigt, at du også forstå, hvorfor du har polære og upolære aminosyrer, hvad der gør den variable gruppe hydrofobe eller hydrofil, og selvfølgelig, den logik bag protoniserede/deprotonated sure og basiske aminosyrer.