 az aminosavak az élőlények építőkövei. Az aminosavak hosszú láncai fehérjéket alkotnak, amelyek viszont számos szerkezeti és funkcionális sejtkomponenst alkotnak.
az aminosavak az élőlények építőkövei. Az aminosavak hosszú láncai fehérjéket alkotnak, amelyek viszont számos szerkezeti és funkcionális sejtkomponenst alkotnak.
szeretem a sejtet önálló városnak tekinteni, ahol a mag a főváros, a mitokondriumok az erőmű stb. De akkor ott van a dolgozók, közlekedési rendszer, valamint a nagyon szerkezet a sejt város, amelyek mind a fehérjék – amelyek viszont aminosavakból.,
a fehérjeszerkezet összetettségét az aminosavak szekvenciája és a változó csoport oldalláncaik kémiai jellege határozza meg. A FELVÉTELI megköveteli a megértést, a természet, a polar pedig nonpolar oldalon láncok, valamint a motort, s conformations által okozott hidrofób, valamint hidrofil kölcsönhatások
De igen, kellene memorizálni minden aminosav a FELVÉTELI. Ide tartozik az oldallánc, a teljes név, a 3 betűs név és az egybetűs rövidítés. De ne egyszerűen ragassza a szavakat és struktúrákat a kártyákat, abban a reményben, hogy kényszeríteni a memóriába., Minden egyes aminosavat külön-külön kell kezelnie.
A gyors referencia lista letölthető a szabad Aminosav puskát tanulmányozást
- Írja ki a teljes nevét
- Draw-az aminosav felépítése, változó csoport
- Írd le a 3-levelet, levelet rövidítések
- Szavakba valami különleges ebben a konkrét oldalon lánc – hangosan! Minél viccesebb és őrültebb a kapcsolat, annál könnyebb lesz emlékezni rá.,
- ismételje meg az elnevezési / rajzolási folyamatot azonnal
- ismételje meg hetente, amíg szilárdnak érzi magát ezzel az információval
egy aminosav alapszerkezete
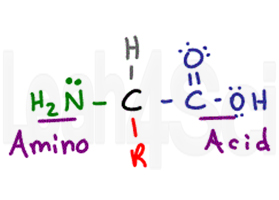 az aminosav nevét két elsődleges funkcionális csoportjából kapja. Az aminosavnak van egy központi királis szénje, az úgynevezett alfa-szén (fekete). A központi szénhez kapcsolódik egy hidrogénatom( szürke), egy amino vagy NH2 csoport (zöld), valamint egy karbonsav COOH csoport (lila). Végül megvan az R csoport (piros), amely egy változó oldallánc.,
az aminosav nevét két elsődleges funkcionális csoportjából kapja. Az aminosavnak van egy központi királis szénje, az úgynevezett alfa-szén (fekete). A központi szénhez kapcsolódik egy hidrogénatom( szürke), egy amino vagy NH2 csoport (zöld), valamint egy karbonsav COOH csoport (lila). Végül megvan az R csoport (piros), amely egy változó oldallánc.,
20 különböző aminosav van, amelyeket egyedi oldalláncaik különböztetnek meg. Ezek egy egyszerű hidrogénatomtól (glicin) egy komplex 2 gyűrűs rezonáló aromás rendszerig (triptofán) terjednek.
míg a fenti teljesen semleges változat az, hogy a legtöbb diák hogyan tanulmányozza az aminosavakat, valamint az ebben a cikkben használt formát, ne feledje, hogy ez technikailag helytelen.
aminosav zwitterion formában
mivel a karboxilcsoport savas és a bázikus aminocsoport, a kettő fiziológiás pH-ban konjugált töltött formájukban zwitterionként fog létezni., További információ a zwitterionról és az aminosavak töltéséről a következő cikkemben (link a követéshez).
egy végső koncepció, mielőtt lebontjuk az egyes aminosavakat, ez pedig a 3 dimenziós fehérjeszerkezet. A biológiai rendszer szerkezete meghatározza a funkciót, így az aminosav jellemzőinek megértése kulcsfontosságú a szerkezet és végül a fehérje funkció megértéséhez.
egy 3-D fehérje elsődleges szerkezete
a fehérjeszerkezet első és fontosabb meghatározási tényezője az aminosavak szekvenciája., Ha a polipeptidlánc más sorrendben van rögzítve, akkor nagyon eltérő általános struktúrát kap.
egy 3-D fehérje másodlagos szerkezete
a másodlagos szerkezet a gerinces hidrogénkötési kölcsönhatásokból származik. A peptidkötés minden korábbi karboxil-és amino-csoportot amid-funkcionális csoportgá alakít. Az alfa-hélix és a béta-redős lemezek másodlagos szerkezete a karbonil részlegesen negatív oxigénje és a nitrogénen lévő részlegesen pozitív hidrogén közötti hidrogénkötésből származik.,
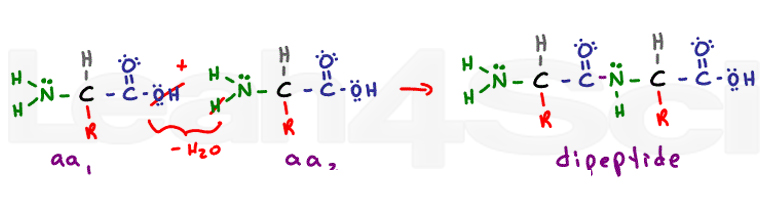
tercier szerkezete egy 3-D fehérje
a tercier szerkezet, ahol a valódi 3-dimenziós hajtogatás kerül bevezetésre, és ez az első alkalom, hogy észre oldallánc kölcsönhatások. Ez az, ahol a tudás és a megértés aminosav oldalláncok kritikus.
hadd ismételjem meg magam, a harmadlagos szerkezet az első alkalom, hogy változó R-csoport oldalsó lánc kölcsönhatásokat lát a polipeptidláncon. Sok diák összekeveri ezt a másodlagos struktúrával, ami csak gerinc kölcsönhatások.,
a 3-D Multi-polipeptid fehérje kvaterner szerkezete
a kvaterner szerkezet a különböző polipeptidek közötti változó csoport kölcsönhatásokra utal, hogy egyetlen nagyobb fehérjét képezzen.
a kvaterner struktúrák nem találhatók minden proteinben. Ha a fehérje csak egyetlen aminosavszálat tartalmaz, akkor a legmagasabb szintű hajtogatás a tercier szerkezete. Ha azonban a fehérje több polipeptid alegységből áll, akkor a kvaterner szerkezet tartja össze a különböző polipeptideket.,
most, hogy megérted az oldallánc jellemzőinek jelentőségét, merüljünk bele az aminosavakba. Ne feledje, hogy mivel a szülő amino-és karboxilcsoportok “elfoglaltak” az elsődleges/másodlagos szerkezettel, nem elemzik őket az oldallánc tulajdonságainak és jellemzőinek tanulmányozása során.
Ez azt jelenti, hogy figyelmen kívül hagy minden lehetséges polaritást mind a karboxil, mind az aminocsoportokon, és csak az oldalláncokat nézi.
nem poláris hidrofób aminosavak
hidrofób, ahogy a neve is sugallja, hidro – víz, fóbikus félelem., A hidrofób aminosavaknak kevés vagy semmilyen polaritása nincs az oldalláncukban. A polaritás hiánya azt jelenti, hogy nincs mód arra, hogy kölcsönhatásba lépjenek a rendkívül poláris vízmolekulákkal, ami vízfélővé teszi őket.
csak öt Atom jelenik meg az aminosav változó csoportokban: H, C, N, O és S.
csak akkor vegye figyelembe a polaritást, ha N, O, S a “többség” tényezője. Rámutatok ezekre, ahogy előfordulnak. Ha azonban csak Cs-t és Hs-t lát, akkor automatikusan fel kell ismernie a vízfélő aminosavat.,
GlycineGlyG
a glicin egy egyedülálló aminosav, mivel nem igazán rendelkezik R csoporttal. Ha úgy gondolja, “változó R csoport,” meg kell gondolni a szén kapcsolódik más atomok. De a glicinnek csak hidrogénje van az oldalsó lánc helyzetében. Mivel a glicinnek 2 hidrogénatomja van, mindegyik a szülő-és oldalláncon van, ez az egyetlen szimmetrikus és így achirális aminosav. Mivel a hidrogén nem poláris, a glicin hidrofób aminosav. A hidrogén oldallánc teszi glicin a legkisebb aminosav.,
AlanineAlaA
az alanin egy egyszerű aminosav, amelynek oldallánca csak metil-vagy CH3-csoport. Mivel csak a szén és a hidrogén látható, az alanin egy nem poláris hidrofób aminosav. Fontos felismerni, hogy ez egy nagyon kicsi aminosav, amely képes szűk hurkokba vagy láncokba “ékelni”.
ValineValV
a valin egy másik egyszerű aminosav, csak egy izopropil változó csoporttal. Csakúgy, mint az alanin, csak szenet és hidrogént látunk, így a valin nem poláris hidrofób aminosav.,
LeucineLeuL
felismerheti, hogy a leucin ugyanolyan változó csoporttal rendelkezik, mint a valin, de egy extra CH2 csoporttal. Vagy egyszerűen felismerheti az izobutil oldalláncát.
nézze meg ezt a videót, ha nem ismeri az elágazó oldalláncokat, mint például az izopropil vagy a sec-butil. Mivel a leucin csak Cs és Hs, ez egy vízfélő nem poláris aminosav.
IsoleucineIleI
az izoleucin, ahogy a neve is sugallja, a leucin izomerje. A különbség a CH3 elhelyezése egy sec-butil helyett izobutil oldallánc. Az izomeréhez hasonlóan az izoleucin nem poláris és hidrofób.,
Metioninemetm
a metionin az első potenciálisan trükkös aminosav. Oldallánca többnyire Cs-t és H-t tartalmaz, de beágyazott kénatommal rendelkezik. Bár azt gondolhatja, hogy hidrofil, figyeljen a kénatom helyére. A láncba ágyazva, csak szénatomokhoz kapcsolódva a kén részben “el van rejtve” a külső környezetből.
miközben nem kell ismernie az MCAT elektronegativitási értékeit, segít megérteni, hogy S = 2,58 és C = 2,55. Mivel az elektronegativitás különbsége kevesebb, mint 0,5, ezen az oldalon nincs polaritás.,
a metionint is fel kell ismernie, mint a kiindulási kodont AUG az RNS-ben a fehérjékre fordítva.
PhenylalaninePheF
annak érdekében, hogy ne feledje, hogy a fenilalanin F ne feledje, hogy a ” ph “- T ” F ” – nek ejtik. Ne keverje össze ezt a P-vel a proline-hoz.
vegye figyelembe a fenilalanin szerkezetét. Egyetlen széncsoporttal rendelkezik, csatolt benzolgyűrűvel. A fenil a benzol szubsztituens neve, ennek a molekulának az alanin szerkezetéhez benzol (fenil) kapcsolódik. Mivel a fenilalanin aromás oldalláncában csak Cs és Hs található, nem poláris és hidrofób.,
Triptophantrpw
Ez egy trükkös. Figyeld meg az N-H-t ebben az oldalláncban. Az N-H-nak polárisnak kell lennie, és képesnek kell lennie hidrogénkötésre. Ennek azonban két oka van: ez az aminosav még mindig nem poláris és hidrofób.
- az N-H Csoport a nagyon nagy oldallánc apró része.
- nézze meg alaposan a nitrogént, és ami még fontosabb, a magányos párjait. A nitrogén elektronjai szerves részét képezik a triptofán oldallánc konjugált aromájának., Más szavakkal, gondoljon az elektronjaira, mint “túlságosan zavart” a rezonancia, hogy nagy figyelmet fordítson a külső vízkörnyezetre.
az MCAT megköveteli, hogy felismerje, hogy ez egy nagy és terjedelmes aminosav. De mivel ez egy feleletválasztós vizsga, egyszerűen megjegyezheti, hogy a triptofán az egyetlen aminosav, két olvasztott gyűrűvel.
valójában olyan nagy, hogy képes átugrani (trp) magát, és kiáltani Waaaaaa(W)
(Megjegyzés: mnemonics: a viccesebb, furcsább, vagy piszkosabb a mnemonic, annál valószínűbb, hogy emlékezni fog rá. Tartsa ezt szem előtt az orvosira.,)
ProlineProP
prolin egy egyedülálló aminosav, mivel ez az egyetlen, amely magában foglalja a gerincet az oldalláncába. A prolin oldallánc egy 3-szénlánc, amely körül forog, és visszakapcsolódik a szülő aminocsoporthoz. Ez azt jelenti, hogy a többi aminosavtól eltérően a prolin nem tartalmaz hidrogénatomot a nitrogénén, amikor egy polipeptidlánc része.
azonban nem szabad elfelejteni, hogy a nitrogén nem igazán része a változó csoportnak, ami azt jelenti, hogy nem tud hozzájárulni semmilyen polaritáshoz. Mivel csak 3 CH2 csoportunk van az elemzéshez, nem poláris hidrofób oldalláncot kapunk., Ez a szülőhurok egy dudort hoz létre, és nem engedi, hogy a prolin tartalmú lánc lineáris legyen, ami azt jelenti, hogy gyakran hurkokban és egy alfa-spirál végén találja meg.
poláris hidrofób aminosavak
* Ez egy ragacsos szakasz, és attól függően, hogy hol kutatsz, a következőket lehet poláris vagy nempoláris, hidrofil vagy hidrofób kategóriába sorolni. Ügyeljen a poláris csoportok jelenlétére, amelyek kicsiek az Általános oldallánchoz képest, vagy nagyon gyengén polárisak, ezért hidrofób.,
CysteineCysC
a cisztein kissé poláris S-H-val rendelkezik, de polaritása olyan enyhe, hogy a cisztein nem képes megfelelően kölcsönhatásba lépni a vízzel, így hidrofób.
a cisztein nagyon fontos aminosav a tercier és kvaterner szerkezetben. A legtöbb oldallánc kölcsönhatások közé poláris / töltött kölcsönhatások vagy nem poláris Van Der Waals és London diszperziós. A cisztein oldallánca azonban képes diszulfidhíd kialakítására, amely 2 kénatom közötti kovalens kötés az oldallánc oxidációján és 2 hidrogénatom eltávolításán keresztül., Ez a kovalens kötés sokkal erősebb és állandóbb a standard tercier és kvaterner kölcsönhatásokhoz képest.
Ez a kísérleti hiba oka a több alegységgel rendelkező fehérjék fehérje méretének/hosszának meghatározásában is.
TyrosineTyrY
egyes diákok ezt OH szivárgásnak tekintik egy gumiabroncsból (tyr).
vessen egy pillantást a tirozinra. Mit látsz? Úgy néz ki, mint az aromás fenilalanin egy OH csoporttal para helyzetben (ortho/meta/para 2nd videó).,
egyrészt nagyon poláris és hidrogénkötésre képes OH csoportunk van, másrészt az Oh kicsi a benzilcsoport (CH2-fenil) méretéhez képest. Ez a talány a zavartság gyakori forrása, de ha ezt megérted, felismered, hogy a tirozin, míg a poláris, még mindig hidrofób aminosav.
poláris hidrofil aminosavak
hidrofil, ahogy a neve is sugallja, hidro-vízből és filikus szeretetből származik.
a polaritás a kötött atomok közötti Elektronegativitás 0,5-1,9 különbségéből származik., Bár nem kell ismernie ezeket az értékeket az MCAT számára, fel kell ismernie, hogy a poláris kötések akkor fognak létezni, ha N és O nem szénatomokhoz vannak kötve.
az elektronegativitási különbség elegendő a töltés vagy a polaritás enyhe elválasztásához. És mivel a hasonlók vonzóak, ezek a részlegesen feltöltött csoportok vonzódnak az ellentétesen feltöltött vagy részben feltöltött csoportokhoz, például a vízhez. Ezek a csoportok megcsavarják a polipeptidláncot, hogy kölcsönhatásba lépjenek egymással és vízzel.
a hidrofób csoportok elfordulnak ezektől az oldalláncoktól.,
SerineSerS
Gondolj a szerinre alaninként, egy OH csoporttal együtt. A tirozinnal ellentétben az OH a molekula többsége, polaritása pedig elegendő ahhoz, hogy befolyásolja az egész csoportot. Ez teszi a sorozat poláris és nagyon hidrofil.
Threoninthrt
többféle módon lehet megnézni ezt a csoportot. Azt gondolhatja, hogy szerin egy extra metil-csoporttal, vagy valinként, de OH-val helyettesítve az egyik metil-csoportot. Emlékszem, hogy három különböző csoport volt: CH, CH3 és OH.
a szerinhez hasonlóan ez a változó csoport poláris és hidrofil.,
AsparagineAsnN
próbáld ki ezt: Slur a beszéd, ahogy azt mondod “asparagine” nagyon gyors. Úgy hangzik, mintha azt mondanád, hogy…N, így emlékszem az aminosav 3 betűs rövidítésére. A molekula végén lévő NH2 azt gondolja, hogy “bázis”, de nézd meg a szomszédját. A karbonil közelében lévő NH2 amidot képez, amely nem szeret savként vagy bázisként működni standard fiziológiai körülmények között. A karbonil-oxigén és az NH2 csoport részleges töltésével és H-kötési képességével azonban poláris hidrofil aminosavat kapunk.,
GlutamineGlnQ
mindkét “glut” aminosavra úgy gondolok, mint a gluttonokra, amelyek egy extra CH2 csoportot “fogyasztottak”. A glutamin ugyanolyan szerkezetű, mint az aszparagin, de láncában extra torkos CH2 van. Az aszparaginhoz hasonlóan poláris és hidrofil.
savas és bázikus aminosav oldalláncok
az aminosavak savassága és bázikussága újabb zavart okoz a diákok körében. Ha savként indul, akkor bázis lesz? Hogyan találom meg a díjat? És így tovább.
itt van a trükk: az oldalláncban lévő karbonsav savas aminosavat ad., Amikor egy karboxilcsoport deprotonálódik, konjugált bázissót kap. Tehát ha egy karbonsav oldallánc sóváltozatát látja, miközben technikailag “konjugált bázis”, akkor egyszerűen a savas aminosav sóváltozatának nevezzük. Ugyanaz a bázis. Vigyázzon az oldalsó láncban lévő “nem zavart” nitrogénatomokra.
savas aminosavak
a savas aminosavaknak nagyon ismerősnek kell lenniük az aszparaginhoz és a glutaminhoz képest. Ez azért van, mert minden róluk ugyanaz, kivéve a terminál funkcionális csoport., Az amidok (fent tárgyalt) polárisak, de ha az NH2-t OH csoportra cserélik, akkor savas karboxilcsoportot kap.
aszparaginsav / Aszpartateaszpd
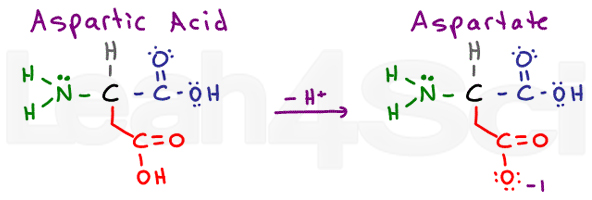
az aszparaginsav az aminosav protonált savas formájára utal. Amikor deprotonált, akkor gyakran látni a konjugált bázis só említett aszpartát. Ez a karbonsavak standard nómenklatúrája.
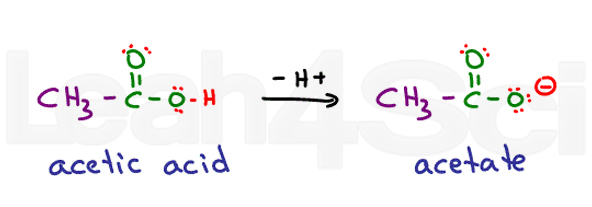
Gondolj az etánsavra. Közös neve ecetsav. Amikor deprotonált kapsz acetát., A savak vízben nagyon stabilak, mivel részlegesen töltődnek protonált formájukban, és teljesen feltöltődnek deprotonált formájukban. Ez nagyon hidrofilvá teszi őket.
glutaminsav / GlutamateGluE
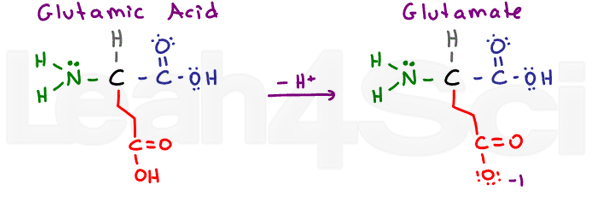
ismét van egy “falánk” aminosav egy extra CH2 csoporttal. A glutaminsav a protonált savas formára utal, a glutamát pedig a deprotonált konjugált bázis/só formára utal.
az aszparaginsavhoz hasonlóan a glutaminsav vízben nagyon stabil, így hidrofil.,
bázikus aminosavak
a bázikus aminosavak nitrogénatomot tartalmaznak egy magányos elektronpárral, amely képes megtámadni egy hidrogénatomot. Ha egy bázikus aminosavat alacsony (savas) pH-nak vetünk alá, akkor az oldatban megragadja az egyik szabad protont, hogy konjugált savas sót képezzen. Ezek könnyen felismerhetők az oldallánc pozitív nitrogénjével. A savas aminosavakkal ellentétben ezeknek a konjugált sóknak nincs “általánosan használt neve”.
LysineLysK
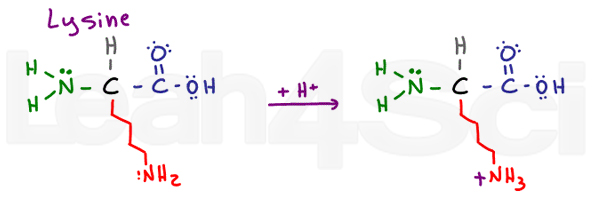
a lizin egy egyszerű bázikus aminosav., Annak ellenére, hogy hosszú és potenciálisan hidrofób lánc, ez egy alapvető NH2 végén. Bázikus deprotonált formájában a lizin semleges és hidrofil; azonban, ha fiziológiás pH-ban található, a lizin felveszi a H+ – ot az oldatból, hogy NH3+ sót képezzen. A sók feltöltődnek, ezért határozottan hidrofil
ArginineArgR
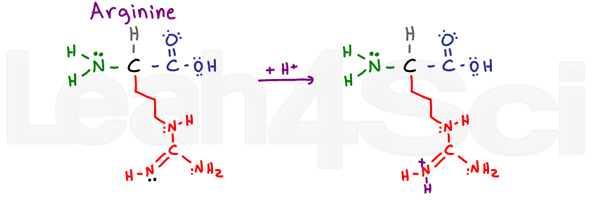
arginin zavaró, és röviden ARGh vagy R-t mondok. Miért? Ennek a változócsoportnak az alaprésze NH, C=N-H és NH2.,
a 2 egyszeres kötésű nitrogénatomból a szénnel és a kettős kötésű nitrogénatommal rezonálhatnak a magányos párjaik. Ez teszi az elektronok elérhetetlenné jár, mint egy bázis. A kettős kötésű nitrogén azonban pi-kötését rezonál, így szabad magányos párja (fekete színben látható) alapvető nitrogénként működik ebben a csoportban.
Hisztidinehish

hisztidin egy másik trükkös bázis ugyanazon okból, mint arginin. Melyik nitrogén az alap? Nézd meg a rajz itt, különösen a magányos pár a 2 nitrogénatomok., A hisztidin gyűrű heterociklusos aromás vegyület. A felső nitrogénatom nem rendelkezik pi kötéssel. Ez azt jelenti, hogy magányos párjait kell használnia a rezonanciában való részvételhez.
az alsó nitrogénatom már rezonáló pi kötéssel rendelkezik. Ez elhagyja a magányos elektronok (fekete) szabadon megragad egy proton, így ez az alapvető atom.
összefoglalva
az aminosavak a biológiai struktúrák és az MCAT biológiájának és biokémiájának kritikus alkotóelemei., Tehát, amikor megpróbálsz mindent megjegyezni erről a 20 aminosavról, fontos, hogy megértsd, miért vannak poláris és nem poláris aminosavak, mi teszi a változó csoportot hidrofób vagy hidrofil, és természetesen a protonált / deprotonált savas és bázikus aminosavak logikáját.