 aminokwasy są budulcem żywych istot. Długie łańcuchy aminokwasów tworzą białka, które z kolei tworzą wiele strukturalnych i funkcjonalnych składników komórkowych.
aminokwasy są budulcem żywych istot. Długie łańcuchy aminokwasów tworzą białka, które z kolei tworzą wiele strukturalnych i funkcjonalnych składników komórkowych.
lubię myśleć o komórce jako o samodzielnym mieście, w którym jądro jest stolicą, mitochondria elektrownią i tak dalej. Ale potem masz swoich pracowników, system transportu i samą strukturę miasta komórkowego, które są zbudowane z białek – które z kolei są zbudowane z aminokwasów.,
złożoność struktury białka zależy od jego sekwencji aminokwasów i chemicznego charakteru ich łańcuchów bocznych zmiennych grup. MCAT wymaga zrozumienia natury polarnych i Niepolarnych łańcuchów bocznych oraz skręcania i konformacji spowodowanych oddziaływaniami hydrofobowymi i hydrofilowymi
i tak, powinieneś zapamiętać każdy aminokwas dla MCAT. Obejmuje to łańcuch boczny, pełną nazwę, 3-literową nazwę i jednoliterowy Skrót. Ale nie przyklejaj słów i struktur na fiszki, mając nadzieję, że wpłynie to na Twoją pamięć., Musisz aktywnie walczyć z każdym aminokwasem indywidualnie.
aby uzyskać szybką listę referencyjną Pobierz my free Amino Acid Cheat Sheet Study Guide
- napisz pełną nazwę
- narysuj strukturę aminokwasów i grupę zmiennych
- napisz trzyliterowe i jednoliterowe skróty
- Zwerbalizuj coś wyjątkowego w tym konkretnym łańcuchu bocznym-na głos! Im bardziej zabawne i szalone Połączenie, tym łatwiej będzie zapamiętać.,
- powtórz proces nazewnictwa/rysowania raz od razu
- powtarzaj co tydzień, aż poczujesz się solidny z tymi informacjami
podstawowa struktura aminokwasu
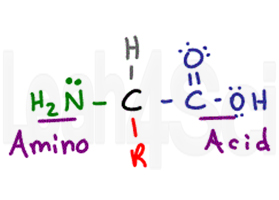 aminokwas otrzymuje swoją nazwę od dwóch podstawowych grup funkcyjnych. Aminokwas ma centralny chiralny węgiel zwany węglem Alfa (czarny). Dołączony do centralnego węgla masz atom wodoru (szary), grupę aminową lub NH2 (zielony) i grupę COOH kwasu karboksylowego (fioletowy). Wreszcie mamy grupę R (Czerwoną), która jest zmiennym łańcuchem bocznym.,
aminokwas otrzymuje swoją nazwę od dwóch podstawowych grup funkcyjnych. Aminokwas ma centralny chiralny węgiel zwany węglem Alfa (czarny). Dołączony do centralnego węgla masz atom wodoru (szary), grupę aminową lub NH2 (zielony) i grupę COOH kwasu karboksylowego (fioletowy). Wreszcie mamy grupę R (Czerwoną), która jest zmiennym łańcuchem bocznym.,
istnieje 20 różnych aminokwasów wyróżniających się unikalnymi łańcuchami bocznymi. Obejmują one od prostego atomu wodoru (glicyny) do złożonego 2-pierścieniowego rezonującego układu aromatycznego (tryptofanu).
podczas gdy powyższa w pełni neutralna wersja to sposób, w jaki większość studentów studiuje aminokwasy i forma, której użyjemy w tym artykule, należy pamiętać, że jest to technicznie niepoprawne.
aminokwas w postaci Zwitterionu
ponieważ grupa karboksylowa jest kwaśna, a grupa aminowa zasadowa, te dwa będą istnieć jako zwitterion w ich sprzężonych formach naładowanych w fizjologicznym pH., Więcej na temat zwitterionu i ładunków aminokwasowych w moim następnym artykule(link do naśladowania).
jedna ostateczna koncepcja, zanim rozbijemy poszczególne aminokwasy, a mianowicie trójwymiarową strukturę białka. W układzie biologicznym struktura określa funkcję, więc zrozumienie cech aminokwasów jest kluczem do zrozumienia struktury i ostatecznie funkcji białka.
struktura podstawowa białka 3-D
pierwszym i ważniejszym czynnikiem determinującym strukturę białka jest sekwencja aminokwasów., Jeśli łańcuch polipeptydowy jest przymocowany w innej kolejności, otrzymujesz bardzo inną ogólną strukturę.
struktura wtórna białka 3-D
struktura wtórna pochodzi z oddziaływań wiązania wodorowego szkieletu. Wiązanie peptydowe zamienia każdą dawną grupę karboksylową i aminową w amidową grupę funkcyjną. Struktura wtórna Alfa helisy i beta plisowanych arkuszy pochodzą z wiązania wodorowego między częściowo ujemnym tlenem na karbonylu i częściowo dodatnim Wodorem na azocie.,
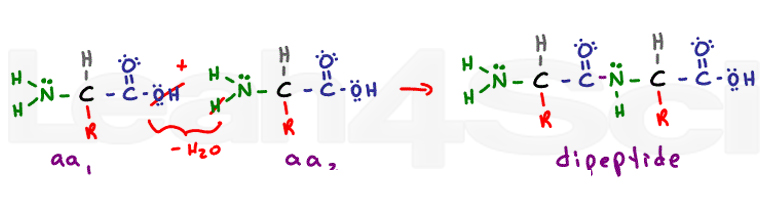
struktura trzeciorzędowa białka 3-D
struktura trzeciorzędowa jest miejscem, w którym wprowadza się rzeczywiste składanie trójwymiarowe i jest to pierwszy raz, gdy zauważysz interakcje z łańcuchem bocznym. To jest, gdzie wiedza i zrozumienie łańcuchów bocznych aminokwasów są krytyczne.
powtórzę, po raz pierwszy w łańcuchu polipeptydowym zobaczysz zmienne interakcje po stronie Grupy R. Wielu uczniów myli to z drugorzędną strukturą, która jest jedynie szkieletową interakcją.,
czwartorzędowa Struktura 3-D Multi-polipeptydowego białka
czwartorzędowa struktura odnosi się do zmiennych oddziaływań grupowych między różnymi polipeptydami, tworząc jedno większe białko.
struktury Czwartorzędowe nie występują w każdym białku. Jeśli białko zawiera tylko jedną nić aminokwasową, to najwyższym poziomem fałdowania jest jego trzeciorzędowa struktura. Jeśli jednak białko składa się z wielu podjednostek polipeptydowych, to struktura czwartorzędowa jest tym, co utrzymuje różne polipeptydy razem.,
teraz, gdy rozumiesz znaczenie cech łańcucha bocznego, zagłębimy się w aminokwasy. Należy pamiętać, że ponieważ macierzyste grupy aminowe i karboksylowe są „zajęte” strukturą pierwotną/wtórną, nie są analizowane podczas badania właściwości i właściwości łańcucha bocznego.
oznacza to, że ignoruje się potencjalną polaryzację zarówno grup karboksylowych, jak i aminowych i patrzy się tylko na łańcuchy boczne.
niepolarne aminokwasy hydrofobowe
hydrofobowe, jak sama nazwa wskazuje jest hydrofobowe, fobowe., Aminokwasy hydrofobowe mają niewielką lub brak polaryzacji w łańcuchach bocznych. Brak polaryzacji oznacza, że nie mają możliwości interakcji z wysoce polarnymi cząsteczkami wody, co powoduje, że boją się wody.
istnieje tylko pięć atomów, które pojawią się w Twoich zmiennych aminokwasowych: H, C, N, O i S.
rozważaj polaryzację tylko wtedy, gdy masz N, O, S jako czynnik 'większości'. Wskażę je, gdy się pojawią. Jednak, jeśli wszystko, co widzisz to Cs i Hs, powinieneś automatycznie rozpoznać aminokwas bojący się wody.,
GlycineGlyG
Glicyna jest unikalnym aminokwasem, ponieważ tak naprawdę nie ma grupy R. Kiedy myślisz o 'zmiennej grupie R', powinieneś pomyśleć o węglu przyłączonym do innych atomów. Ale glicyna ma tylko wodór w bocznym położeniu łańcucha. Ponieważ glicyna ma 2 atomy wodoru, po jednym na łańcuchu macierzystym i bocznym, jest jedynym symetrycznym, a więc achiralnym aminokwasem. Ponieważ wodór jest niepolarny, glicyna jest aminokwasem hydrofobowym. Wodorowy łańcuch boczny sprawia, że glicyna jest najmniejszym aminokwasem.,
Alaninaaa
Alanina jest prostym aminokwasem, który ma tylko grupę metylową lub CH3 jako swój łańcuch boczny. Ponieważ widzisz tylko węgiel i wodór, Alanina jest niepolarnym hydrofobowym aminokwasem. Ważne jest, aby rozpoznać, że jest to bardzo mały aminokwas i może być „zaklinowany” w ciasne pętle lub łańcuchy.
ValineValV
walina jest kolejnym prostym aminokwasem o zmiennej grupie izopropylowej. Podobnie jak alanina, widzimy tylko węgiel i wodór, czyniąc walinę niepolarnym hydrofobowym aminokwasem.,
LeucineLeuL
można rozpoznać leucynę jako posiadającą tę samą zmienną grupę co walina, ale z dodatkową grupą CH2. Lub możesz po prostu rozpoznać jego łańcuch boczny izobutylu.
Zobacz ten film, jeśli nie znasz rozgałęzionych łańcuchów bocznych, takich jak izopropyl lub sec-butyl. Ponieważ leucyna ma tylko Cs i Hs, Jest to woda, która nie jest polarnym aminokwasem.
IsoleucineIleI
izoleucyna, jak sama nazwa wskazuje, jest izomerem leucyny. Różnica polega na umieszczeniu CH3 w łańcuchu bocznym sec-butylowym, a nie izobutylowym. Podobnie jak izomer, izoleucyna jest niepolarna i hydrofobowa.,
Metioninemetm
metionina jest pierwszym potencjalnie trudnym aminokwasem. Jego boczny łańcuch zawiera głównie Cs i Hs, ale z osadzonym atomem siarki. Chociaż możesz myśleć, że to hydrofilowe, zwróć szczególną uwagę na lokalizację atomu siarki. Osadzona w łańcuchu i przymocowana tylko do atomów węgla, siarka jest częściowo „ukryta” przed środowiskiem zewnętrznym.
chociaż nie musisz znać wartości elektroenergetycznych dla MCAT, pomaga zrozumieć, że S = 2,58 i C = 2,55. Ponieważ różnica w elektroujemności jest mniejsza niż 0,5, nie ma polaryzacji na tym łańcuchu bocznym.,
należy również rozpoznać metioninę jako początkowy kodon AUG w translacji RNA do białek.
Fenyloalaninefef
aby pomóc ci pamiętać, że fenyloalanina jest F pamiętaj, że ” ph „jest wymawiane jako „F”. Nie mieszaj tego z P Jak proline.
zwróć uwagę na strukturę fenyloalaniny. Posiada pojedynczą grupę węglową z dołączonym pierścieniem benzenowym. Fenyl to nazwa podstawnika benzenowego, a cząsteczka ta ma benzen (fenyl) przyłączony do struktury alaniny. Ponieważ fenyloalanina ma tylko Cs i Hs w aromatycznym łańcuchu bocznym, jest niepolarna i hydrofobowa.,
Tryptofantrpw
To jest trudne. Zwróć uwagę na N-H w tym łańcuchu bocznym. N-H powinno być polarne i zdolne do wiązania wodorowego. Istnieją jednak dwa powody, dla których aminokwas ten jest nadal niepolarny i hydrofobowy.
- Grupa N-H jest niewielką częścią bardzo dużego łańcucha bocznego.
- przyjrzyj się uważnie azotowi, a co ważniejsze jego samotnym param. Elektrony azotu są integralną częścią sprzężonej aromatyczności dla łańcucha bocznego tryptofanu., Innymi słowy, pomyśl o jego elektronach jako „zbyt rozproszonych” przez rezonans, aby zwrócić dużą uwagę na zewnętrzne środowisko wodne.
MCAT wymaga uznania, że jest to duży i nieporęczny aminokwas. Ale ponieważ jest to badanie wielokrotnego wyboru, możesz po prostu zapamiętać, że tryptofan jest jedynym aminokwasem z dwoma zespolonymi pierścieniami.
w rzeczywistości jest tak duży, że może się potknąć (trp) o siebie i zawołać Waaaaaa (W)
(uwaga na mnemonikę: im śmieszniejszy, dziwniejszy lub brudniejszy mnemonik, tym bardziej prawdopodobne, że go zapamiętasz. Pamiętaj o tym do szkoły medycznej.,)
ProlineProP
Prolina jest unikalnym aminokwasem, ponieważ jako jedyny zawiera kręgosłup w swoim łańcuchu bocznym. Łańcuch boczny proliny to łańcuch 3-węglowy, który pętli wokół i przyłącza się z powrotem do macierzystej grupy aminowej. Oznacza to, że w przeciwieństwie do innych aminokwasów, prolina nie ma atomu wodoru na swoim azocie, gdy jest częścią łańcucha polipeptydowego.
nie można jednak zapominać, że azot tak naprawdę nie należy do grupy zmiennych, co oznacza, że nie może mieć żadnej polaryzacji. Ponieważ mamy tylko 3 grupy CH2 do analizy, otrzymujemy niepolarny hydrofobowy łańcuch boczny., Ta pętla rodzica tworzy wybrzuszenie i nie pozwala, aby łańcuch zawierający prolinę był liniowy, co oznacza, że często znajdziesz go w pętlach i na końcu helisy Alfa.
Polarne aminokwasy hydrofobowe
*jest to sekcja lepka i w zależności od tego, gdzie badasz, możesz znaleźć następujące kategorie: polarne lub niepolarne, hydrofilowe lub hydrofobowe. Zwróć uwagę na obecność grup polarnych, które są małe w porównaniu z ogólnym łańcuchem bocznym, lub bardzo słabo polarne, a zatem hydrofobowe.,
CysteineCysC
cysteina ma lekko polarny S-H, ale jej polaryzacja jest tak łagodna, że cysteina nie jest w stanie prawidłowo oddziaływać z wodą, czyniąc ją hydrofobową.
Cysteina jest bardzo ważnym aminokwasem, jeśli chodzi o strukturę trzeciorzędową i czwartorzędową. Większość oddziaływań bocznych obejmuje interakcje polarne/naładowane lub niepolarne van Der Waalsa i dyspersję londyńską. Jednak łańcuch boczny cysteiny jest w stanie utworzyć most dwusiarczkowy, który jest wiązaniem kowalencyjnym między 2 atomami siarki poprzez utlenianie łańcucha bocznego i usunięcie 2 atomów wodoru., To wiązanie kowalencyjne jest znacznie silniejsze i bardziej trwałe w porównaniu do standardowych oddziaływań trzeciorzędowych i czwartorzędowych.
jest to również przyczyna błędu doświadczalnego w określaniu wielkości/długości białka dla białek z wieloma podjednostkami.
TyrosineTyrY
niektórzy studenci postrzegają to jako wyciek z opony (tyr).
przyjrzyj się bliżej tyrozynie. Co widzisz? Wygląda jak aromatyczna fenyloalanina z grupą OH w pozycji para (Ortho/meta / para 2nd wideo).,
z jednej strony mamy bardzo polarną i zdolną do wiązania wodorowego grupę OH, ale z drugiej strony OH jest mała w porównaniu do wielkości grupy benzylowej (CH2-fenylowej). Ta zagadka jest częstym źródłem nieporozumień, ale jeśli to zrozumiesz, rozpoznasz, że tyrozyna, choć polarna, jest nadal hydrofobowym aminokwasem.
Polarne aminokwasy hydrofilowe
hydrofilowe jak sama nazwa wskazuje pochodzi od hydrofilowych i filikotwórczych.
Polaryzacja wynika z różnicy elektronowej 0,5-1,9 pomiędzy wiązanymi atomami., Chociaż nie musisz znać tych wartości dla MCAT, powinieneś zauważyć, że wiązania polarne będą istniały, gdy N I O są związane z atomami innych niż węgiel.
różnica elektroujemności jest wystarczająca, aby wytworzyć nieznaczne rozdzielenie ładunku lub polaryzacji. A ponieważ podobne przyciąga podobne, te częściowo naładowane grupy będą przyciągane do przeciwstawnie naładowanych lub częściowo naładowanych grup, takich jak woda. Grupy te skręcają łańcuch polipeptydowy w celu interakcji ze sobą i z wodą.
grupy hydrofobowe skręcają się od tych łańcuchów bocznych.,
seryny
pomyśl o serynie jako alaninie z dołączoną grupą OH. W przeciwieństwie do tyrozyny, OH jest większość w tej cząsteczce i jej polaryzacja jest wystarczająca, aby wpłynąć na całą grupę. Dzięki temu seria jest polarna i bardzo hydrofilowa.
Treoninethrt
istnieje wiele sposobów patrzenia na tę grupę. Można o tym myśleć jako seryna z dodatkową grupą metylową lub jako walina, ale z OH zastępującą jedną z grup metylowych. Pamiętam, że trzy osoby miały 3 różne grupy: CH, CH3 i OH.
podobnie jak seryna, ta zmienna grupa jest polarna i hydrofilowa.,
Szparagina
spróbuj tak: Oblewaj swoją mowę, gdy mówisz „szparagina” naprawdę szybko. Brzmi to tak, jakbyś mówił „N”, tak pamiętam 3-literowy skrót tego aminokwasu. NH2 na końcu tej cząsteczki sprawia, że myślisz „bazowo”, ale spójrz na to, że jest sąsiadem. NH2 w pobliżu karbonylu tworzy amid, który nie lubi działać jako kwas lub zasada w standardowych warunkach fizjologicznych. Jednak z częściowymi ładunkami i zdolnością wiązania H zarówno w tlenach karbonylowych, jak i w grupach NH2, otrzymujemy polarny aminokwas hydrofilowy.,
GlutamineGlnQ
myślę, że oba 'glut' aminokwasy jako obżarstwo 'zjadły' dodatkową grupę CH2. Glutamina ma taką samą strukturę jak asparagina, ale z dodatkowym obżartym CH2 w łańcuchu. Podobnie jak asparagina, jest polarna i hydrofilna.
kwaśne i zasadowe Łańcuchy aminokwasowe
kwasowość i zasadowość aminokwasów jest kolejnym źródłem nieporozumień wśród studentów. Jeśli zaczyna się jako kwas, czy staje się zasadą? Jak mogę znaleźć opłatę? I tak dalej.
oto sztuczka: kwas karboksylowy w łańcuchu bocznym da ci aminokwas kwaśny., Kiedy grupa karboksylowa jest deprotonowana, otrzymujemy sprzężoną sól zasadową. Więc jeśli widzisz solną wersję bocznego łańcucha kwasu karboksylowego, podczas gdy jest on technicznie 'sprzężoną zasadą', po prostu będziemy nazywać go solną wersją kwaśnego aminokwasu. To samo dotyczy bazy. Zwróć uwagę na „nie rozproszone” atomy azotu w łańcuchu bocznym.
aminokwasy kwaśne
aminokwasy kwaśne powinny wyglądać bardzo znajomo w porównaniu do asparaginy i glutaminy. A to dlatego, że wszystko w nich jest takie samo, z wyjątkiem terminalowej grupy funkcyjnej., Amidy (omówione powyżej) są polarne, ale jeśli NH2 zostanie zamienione na Grupę OH, otrzymamy kwaśną grupę karboksylową.
kwas asparaginowy / AspartateAspD
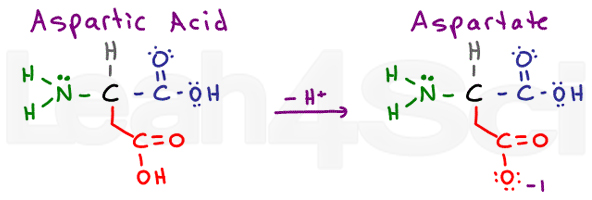
Po deprotonacji często zobaczysz sprzężoną sól zasadową określaną jako asparaginian. Jest to standardowa nomenklatura dla kwasów karboksylowych.
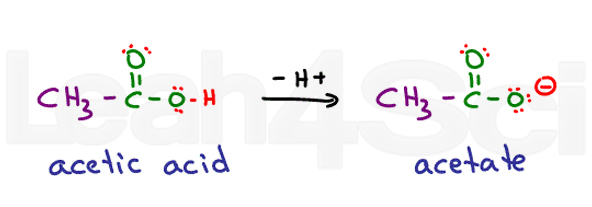
Jego potoczna nazwa to kwas octowy. Po deprotonacji dostajesz octan., Kwasy są bardzo stabilne w wodzie, ponieważ są częściowo naładowane w formie protonowanej i całkowicie naładowane w formie deprotonowanej. To czyni je wysoce hydrofilnymi.
kwas glutaminowy / GlutamateGluE
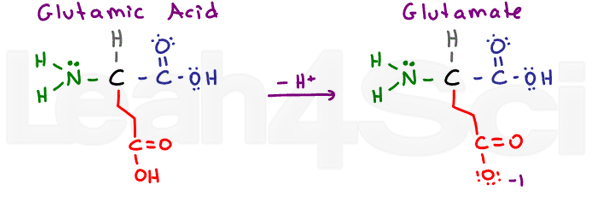
po raz kolejny mamy aminokwas „glutonowy” z dodatkową grupą CH2. Kwas glutaminowy odnosi się do protonowanej postaci kwasowej, a glutaminian odnosi się do deprotonowanej sprzężonej Zasady/formy soli.
podobnie jak kwas asparaginowy, kwas glutaminowy jest bardzo stabilny w wodzie, a tym samym hydrofilowy.,
aminokwasy podstawowe
aminokwasy podstawowe zawierają atom azotu z pojedynczą parą elektronową zdolną do ataku na atom wodoru. Gdy zasadowy aminokwas jest poddawany niskiemu (kwaśnemu) pH, chwyci jeden z wolnych protonów w roztworze, tworząc sprzężoną sól kwasową. Łatwo je rozpoznać po dodatnim azocie w łańcuchu bocznym. W przeciwieństwie do aminokwasów kwaśnych, nie ma „powszechnie używanych nazw” do zapamiętywania dla tych koniugowanych soli.
LysineLysK
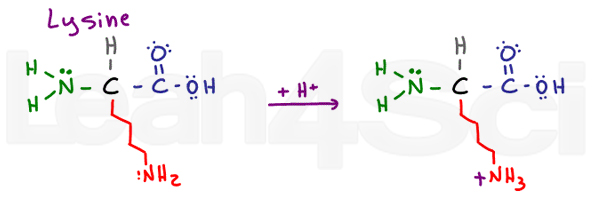
Lizyna jest prostym aminokwasem zasadowym., Pomimo długiego i potencjalnie hydrofobowego łańcucha, na końcu ma podstawowy NH2. W swojej podstawowej postaci deprotonowanej lizyna jest neutralna i hydrofilna; jednak jeśli znajdzie się w fizjologicznym pH, lizyna odbierze H + z roztworu, tworząc sól NH3+. Sole są naładowane i dlatego zdecydowanie hydrofilowe
ArginineArgR
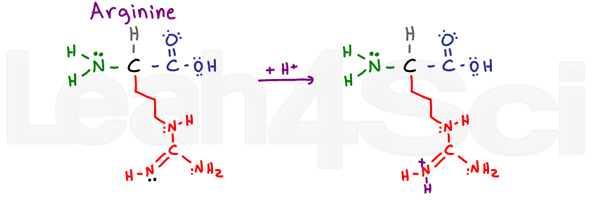
arginina jest myląca i sprawia, że mówię ARGh lub R W skrócie. Dlaczego? Podstawowa część tej grupy zmiennych składa się z nh, C=N-H i NH2.,
2 pojedyncze atomy azotu mogą używać swoich samotnych par do rezonowania z atomem węgla i podwójnym atomem azotu. To sprawia, że ich elektrony są niedostępne do działania jako podstawa. Jednak podwójnie związany azot wykorzystuje Wiązanie pi do rezonowania, pozostawiając wolną samotną parę (pokazaną na czarno), która działa jako podstawowy azot w tej grupie.
Argh!
Histydynehish

histydyna jest kolejną bazą z tego samego powodu co arginina. Który azot jest podstawowy? Spójrz na rysunek tutaj, szczególnie na samotne pary na 2 atomy azotu., Pierścień histydyny jest heterocyklicznym Związkiem aromatycznym. Górny atom azotu nie ma wiązania pi. Oznacza to, że musi używać swoich samotnych par do udziału w rezonansie.
dolny atom azotu ma już rezonujące Wiązanie pi. To pozostawia jego samotne elektrony (pokazane na czarno) swobodnie chwycić proton, co czyni go ATOM podstawowy.
podsumowując
aminokwasy są kluczowym składnikiem struktur biologicznych i twojego zrozumienia biologii i biochemii na MCAT., Tak więc, próbując zapamiętać wszystko o tych 20 aminokwasach, ważne jest, abyś zrozumiał również, dlaczego masz polarne i niepolarne aminokwasy, co sprawia, że zmienna grupa jest hydrofobowa lub hydrofilowa, i oczywiście logika stojąca za protonowanymi / deprotonowanymi kwasowymi i zasadowymi aminokwasami.