 aminozuren zijn de bouwstenen van levende dingen. De lange kettingen van aminozuren maken omhoog proteã nen, die op zijn beurt omhoog vele structurele en functionele celcomponenten vormen.
aminozuren zijn de bouwstenen van levende dingen. De lange kettingen van aminozuren maken omhoog proteã nen, die op zijn beurt omhoog vele structurele en functionele celcomponenten vormen.
Ik zie de cel graag als een op zichzelf staande stad waar de kern de hoofdstad is, de mitochondriën de energiecentrale enzovoort. Maar dan heb je je werknemers, het transportsysteem en de structuur van de celstad, die allemaal gemaakt zijn van eiwitten – die op hun beurt gemaakt zijn van aminozuren.,
de complexiteit van een eiwitstructuur wordt bepaald door de sequentie van aminozuren en de chemische aard van de zijketens van de variabele groep. Het MCAT vereist inzicht in de aard van polaire en niet-polaire zijketens en de verdraaiing en conformaties veroorzaakt door hydrofobe en hydrofiele interacties
en ja, je moet elk aminozuur voor het MCAT onthouden. Dit omvat de zijketen, volledige naam, 3-letter naam en enkele letter afkorting. Maar plak niet gewoon de woorden en structuren op flashcards in de hoop om het te dwingen in je geheugen., Je moet elk aminozuur afzonderlijk actief aanpakken.
voor een snelle referentielijst download mijn gratis aminozuur Cheat Sheet studiegids
- schrijf de volledige naam
- teken de aminozuurstructuur en variabele groep
- schrijf de afkortingen
- Verbaliseer iets unieks over deze specifieke zijketen – hardop! Hoe grappiger en gekker de verbinding, hoe makkelijker je het zult onthouden.,
- herhaal onmiddellijk het naam – / tekenproces
- herhaal wekelijks totdat u zich vast voelt met deze informatie
de basisstructuur van een aminozuur
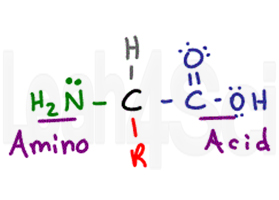 het aminozuur krijgt zijn naam van zijn twee primaire functionele groepen. Het aminozuur heeft een centrale chirale koolstof genoemd de alpha koolstof (zwart). Aan de centrale koolstof zit een waterstofatoom (grijs), een amino-of NH2-groep (groen) en een carbonzuur-COOH-groep (paars). Tot slot hebben we de R groep (rood), dat is een variabele zijketen.,
het aminozuur krijgt zijn naam van zijn twee primaire functionele groepen. Het aminozuur heeft een centrale chirale koolstof genoemd de alpha koolstof (zwart). Aan de centrale koolstof zit een waterstofatoom (grijs), een amino-of NH2-groep (groen) en een carbonzuur-COOH-groep (paars). Tot slot hebben we de R groep (rood), dat is een variabele zijketen.,
er zijn 20 verschillende aminozuren die zich onderscheiden door hun unieke zijketens. Ze variëren van een eenvoudig waterstofatoom (glycine) tot een complex 2-ring resonerend aromatisch systeem (tryptofaan).
hoewel de volledig neutrale versie hierboven is hoe de meeste studenten aminozuren bestuderen, en de vorm die we in dit artikel zullen gebruiken, houd er rekening mee dat dit technisch onjuist is.
aminozuur in Zwitterionvorm
aangezien de carboxylgroep zuur is en de aminogroep basisch, zullen de twee bestaan als zwitterion in hun geconjugeerde geladen vormen in fysiologische pH., Meer over zwitterion en aminozuurladingen in mijn volgende artikel (link te volgen).
een laatste concept voordat we de individuele aminozuren afbreken, en dat is de 3-dimensionale eiwitstructuur. In een biologisch systeem bepaalt de structuur functie, zodat is het begrijpen van aminozuurkenmerken sleutel tot het begrijpen van structuur en uiteindelijk eiwitfunctie.
primaire structuur van een 3-D eiwit
De eerste en belangrijkste determinatiefactor van de eiwitstructuur is de sequentie van aminozuren., Als de polypeptideketen in een andere volgorde is bevestigd, krijg je een heel andere algemene structuur.
secundaire structuur van een 3-D-eiwit
De secundaire structuur komt van backbone waterstofbindingsinteracties. De peptidebinding verandert elke voormalige carboxyl-en aminogroep in een amide functionele groep. De secundaire structuur van Alfa-helix en bèta-geplooide platen komt van waterstofbinding tussen de gedeeltelijk negatieve zuurstof op het carbonyl en de gedeeltelijk positieve waterstof op de stikstof.,
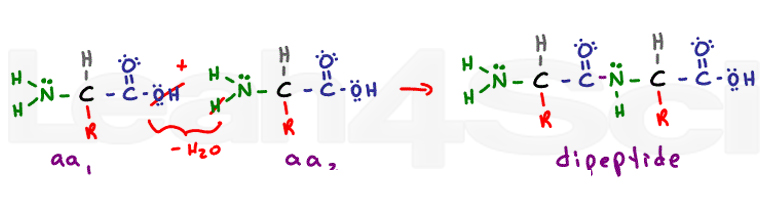
tertiaire structuur van een 3-D eiwit
de tertiaire structuur is waar de echte 3-dimensionale vouwen wordt geïntroduceerd, en dit is de eerste keer dat u zijketeninteracties zult opmerken. Dit is waar de kennis en het begrip van aminozuur zijketens kritiek zijn.
laat me mezelf herhalen, tertiaire structuur is de eerste keer dat je variabele R-groep zijketting interacties ziet op de polypeptideketen. Veel studenten verwarren dit met secundaire structuur, die slechts backbone interacties.,
quaternaire structuur van een 3-D Multi-Polypeptide eiwit
quaternaire structuur verwijst naar de variabele groepsinteracties tussen verschillende polypeptiden om één enkel groter eiwit te vormen.
quaternaire structuren worden niet in elk eiwit gevonden. Als het eiwit slechts één aminozuurstreng bevat, dan is het hoogste niveau van vouwen zijn tertiaire structuur. Nochtans, als de proteã ne uit veelvoudige polypeptidesubeenheden wordt samengesteld, dan is de quaternaire structuur wat de verschillende polypeptides samen houdt.,
nu u de Betekenis van side-chain kenmerken begrijpt, laten we ons verdiepen in aminozuren. Houd er rekening mee dat aangezien de moeder-amino-en carboxylgroepen ‘bezig’ zijn met primaire/secundaire structuur, ze niet worden geanalyseerd bij het bestuderen van zijketeneigenschappen en-kenmerken.
dit betekent dat je elke mogelijke polariteit op zowel de carboxyl-als aminogroepen negeert en alleen naar de zijketens kijkt.
niet-polaire hydrofobe aminozuren
hydrofoob, zoals de naam al aangeeft is hydro-water, fobisch-vrezend., Hydrophobic aminozuren hebben weinig of geen polariteit in hun zijketens. Het gebrek aan polariteit betekent dat ze geen manier hebben om te communiceren met zeer polaire watermoleculen, waardoor ze watervrees hebben.
Er zijn slechts vijf atomen die zullen verschijnen in uw aminozuur variabele groepen: H, C, N, O, en S.
beschouw polariteit alleen als u n, O, S als de ‘meerderheid’ factor. Ik zal ze aanwijzen als ze gebeuren. Echter, als alles wat je ziet Cs en Hs moet u automatisch herkennen een water-vrezend aminozuur.,
GlycineGlyG
Glycine is een uniek aminozuur omdat het niet echt een R-groep heeft. Als je denkt aan ‘variabele R-groep’, moet je denken aan koolstof die aan andere atomen vastzit. Maar glycine heeft alleen een waterstof aan zijn zijketting positie. Aangezien glycine 2 waterstofatomen heeft, elk één aan de ouder-en zijketen, is het het enige symmetrische en dus achirale aminozuur. Aangezien waterstof apolair is, is glycine een hydrofoob aminozuur. De zijketen van waterstof maakt glycine het kleinste aminozuur.,
AlanineAlaA
Alanine is een eenvoudig aminozuur dat slechts een methyl-of CH3-groep als zijketen heeft. Aangezien je niets anders ziet dan koolstof en waterstof, is Alanine een apolair hydrofoob aminozuur. Het is belangrijk om te erkennen dat dit een zeer klein aminozuur is en geschikt om in strakke lijnen of kettingen te worden ‘ingeklemd’.
ValineValV
Valine is een ander eenvoudig aminozuur met slechts een isopropyl variabele groep. Net als alanine zien we niets anders dan koolstof en waterstof, waardoor valine een apolair hydrofoob aminozuur wordt.,
LeucineLeuL
u kunt leucine herkennen als met dezelfde variabele groep als valine, maar met een extra CH2 groep. Of je kunt gewoon de isobutyl zijketting herkennen.
zie deze video als u niet bekend bent met vertakte zijketens zoals isopropyl of sec-butyl. Omdat leucine alleen Cs en Hs heeft, is het een water vrezend apolair aminozuur.
IsoleucineIleI
Isoleucine, zoals de naam al aangeeft, is een isomeer van leucine. Het verschil is de plaatsing van de CH3 voor een sec-butyl in plaats van een isobutyl zijketen. Net als zijn isomeer is isoleucine niet-polair en hydrofoob.,
MethionineMetM
Methionine is het eerste potentieel lastige aminozuur. Zijn zijketting bevat voornamelijk Cs en Hs maar met een ingesloten zwavelatoom. Hoewel je misschien denkt dat het hydrofiel is, let goed op de locatie van het zwavelatoom. Ingebed in de ketting en vastgemaakt aan alleen koolstofatomen, zwavel is gedeeltelijk ‘verborgen’ voor de buitenwereld.
hoewel je geen elektronegativiteitswaarden voor de MCAT hoeft te kennen, helpt het om te begrijpen dat S = 2.58 en C = 2.55. Aangezien het verschil in elektronegativiteit kleiner is dan 0,5, is er geen polariteit op deze zijketel.,
U moet methionine ook herkennen als het STARTCODON AUG in RNA-vertaling naar eiwitten.
Fenylalaninef
om u te helpen herinneren dat fenylalanine F is onthoud dat ‘ph’ wordt uitgesproken als een ‘F’. Meng dit niet met P voor proline.let op de structuur van fenylalanine. Het heeft een enkele koolstofgroep met een bevestigde benzeenring. Fenyl is de naam voor een benzeen substituent, en dit molecuul heeft een benzeen (fenyl) bevestigd aan de structuur van alanine. Aangezien fenylalanine niets anders dan Cs en Hs in zijn aromatische zijketen heeft, is het niet-polair en hydrofoob.,
Tryptofantrpw
Dit is een lastige. Let op de N-H in deze zijketting. N-H moet polair zijn en in staat zijn waterstof te binden. Nochtans, zijn er twee redenen dit aminozuur nog apolair en hydrophobic is.
- De N-H-Groep is een klein deel van de zeer grote zijketen.
- kijk zorgvuldig naar stikstof, en nog belangrijker, naar de eenzame paren. De elektronen van stikstof zijn integraal in de geconjugeerde aromaticiteit voor de tryptofaan zijketen., Met andere woorden, beschouw haar elektronen als ‘te afgeleid’ door resonantie om veel aandacht te besteden aan de externe wateromgeving.
het MCAT vereist dat u erkent dat dit een groot en omvangrijk aminozuur is. Maar omdat het een multiple choice examen je gewoon kunt onthouden dat tryptofaan is het enige aminozuur met twee gesmolten ringen.
In feite is het zo groot dat het kan struikelen (trp) over zichzelf en schreeuwen Waaaaaa (W)
(opmerking over ezelsbruggen: hoe grappiger, vreemder of smeriger de ezelsbruggetje, hoe groter de kans dat je het zult onthouden. Hou dit in gedachten voor de medische school.,)
ProlineProP
Proline is een uniek aminozuur omdat het het enige aminozuur is dat de ruggengraat in zijn zijketen integreert. De Proline zijketen is een 3-carbon keten die rondloopt en zich terug hecht aan de ouder aminogroep. Dit betekent dat in tegenstelling tot de andere aminozuren, proline geen waterstofatoom op zijn stikstof wanneer deel van een polypeptideketen heeft.
echter, Je mag niet vergeten dat stikstof niet echt deel uitmaakt van de variabele groep, wat betekent dat het geen polariteit kan bijdragen. Omdat we maar 3 CH2 groepen hebben om te analyseren krijgen we een niet-polaire hydrofobe zijketen., Deze parent-lus creëert een bobbel en staat niet toe dat een Proline-bevattende keten lineair is, wat betekent dat je hem vaak in lussen en aan het einde van een alpha helix vindt.
polaire hydrofobe aminozuren
*Dit is een kleverig gedeelte, en afhankelijk van waar u onderzoek doet, kunt u het volgende vinden gecategoriseerd als polair of niet-polair, hydrofiel of hydrofoob. Besteed aandacht aan de aanwezigheid van polaire groepen die klein zijn in vergelijking met de Algemene sidechain, of zeer zwak polair en daarom hydrofoob.,
Cysteïnecysc
cysteïne heeft een licht polaire S-H, maar de polariteit is zo mild dat cysteïne niet goed kan interageren met water waardoor het hydrofoob is.
cysteïne is een zeer belangrijk aminozuur als het gaat om tertiaire en quaternaire structuur. De meeste zijketeninteracties omvatten polaire / geladen interacties of apolaire van der Waals en Londense dispersie. De zijketen van cysteïne kan echter een disulfidebrug vormen, een covalente binding tussen 2 zwavelatomen door oxidatie van de zijketen en verwijdering van 2 waterstofatomen., Deze covalente binding is veel sterker en meer permanent in vergelijking met de standaard tertiaire en quaternaire interacties.
Dit is ook de oorzaak van experimentele fout bij het bepalen van eiwitgrootte/ – lengte voor eiwitten met meerdere subeenheden.
TyrosineTyrY
sommige studenten zien dit als Oh lekt uit een band (tyr).
kijk eens goed naar tyrosine. Wat zie je? Het lijkt op de aromatische fenylalanine met een OH groep op de para positie (ortho/meta/para 2nd video).,
aan de ene kant hebben we een zeer polaire en waterstofbindende OH-groep, maar aan de andere kant is de OH klein in vergelijking met de grootte van de benzylgroep (CH2-fenyl). Dit raadsel is een veel voorkomende bron van verwarring, maar als je dit begrijpt, zul je herkennen dat tyrosine, terwijl polair, nog steeds een hydrofoob aminozuur is.
polaire hydrofiele aminozuren
hydrofiele zoals de naam al aangeeft, zijn afkomstig van hydro-water en filic – loving.
polariteit komt van een 0.5-1.9 verschil in elektronegativiteit tussen gebonden atomen., Hoewel je deze waarden voor het MCAT niet hoeft te kennen, moet je erkennen dat polaire bindingen zullen bestaan wanneer N en O gebonden zijn aan niet-koolstofatomen.het verschil in elektronegativiteit is voldoende om een lichte scheiding van lading of polariteit te creëren. En aangezien gelijke trekt gelijke, zullen deze gedeeltelijk geladen groepen worden aangetrokken tot tegengesteld geladen of gedeeltelijk geladen groepen zoals water. Deze groepen zullen de polypeptideketen verdraaien om met elkaar en met water te interageren.hydrofobe groepen zullen zich van deze zijketens verwijderen.,
SerineSerS
zie serine als alanine met een OH-groep. In tegenstelling tot tyrosine, is OH de meerderheid in dit molecuul en zijn polariteit is genoeg om de hele groep te beïnvloeden. Dit maakt serie polair en zeer hydrofiel.
ThreonineThrT
Er zijn meerdere manieren om naar deze groep te kijken. Je kunt het zien als serine met een extra methylgroep, of als valine maar met een OH die één van de methylgroepen vervangt. Ik herinner me THREEonine als het hebben van 3 verschillende groepen: CH, CH3, en OH.
net als serine is deze variabele groep polair en hydrofiel.,
AsparagineAsnN
probeer het volgende: Slur je toespraak zoals je ‘asparagine’ zegt heel snel. Het klinkt alsof je zegt Als…N, zo herinner ik me de drie-letter afkorting voor dit aminozuur. De NH2 aan het eind van dit molecuul doet je denken aan ‘base’, maar kijk naar zijn buurman. NH2 in de buurt van een carbonyl vormt een amide,die niet graag als zuur of base onder standaard fysiologische omstandigheden. Echter, met gedeeltelijke ladingen en H-bindingen bij zowel de carbonylzuurstof als de NH2-groepen, krijgen we een polair hydrofiel aminozuur.,
GlutamineGlnQ
Ik denk aan beide ‘glut’ aminozuren als vraatdieren die een extra CH2-groep hebben ‘geconsumeerd’. Glutamine heeft dezelfde structuur als asparagine, maar met een extra vraatzuchtige CH2 in zijn keten. Net als asparagine is het polair en hydrofiel.
zure en basische Aminozuurzijketens
zuurgraad en basiciteit in aminozuren zijn nog een andere bron van verwarring onder studenten. Als het begint als een zuur, wordt het dan een base? Hoe vind ik de lading? En zo verder.
Hier is de truc: een carboxylzuur in de zijketen geeft je een zuur aminozuur., Als een carboxylgroep wordt gedeprotoneerd, krijg je een geconjugeerd basiszout. Dus als je de zout versie van een carboxylzuur zijketen ziet, terwijl het technisch gezien een ‘geconjugeerde base’ is, zullen we er gewoon naar verwijzen als de zout versie van het zure aminozuur. Hetzelfde voor de basis. Kijk uit voor’ niet-afgeleide ‘ stikstofatomen in de zijketen.
zure aminozuren
de zure aminozuren moeten er zeer bekend uitzien in vergelijking met asparagine en glutamine. En dat komt omdat alles aan hen hetzelfde is, behalve voor de terminale functionele groep., Amiden (hierboven besproken) zijn polair, maar als de NH2 wordt verwisseld voor een OH groep, krijg je een zure carboxyl groep.
asparaginezuur / AspartateAspD
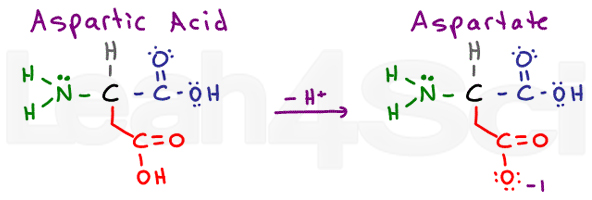
asparaginezuur verwijst naar de geprotoneerde zure vorm van het aminozuur. Wanneer gedeprotoneerd, zie je vaak het geconjugeerde base zout aangeduid als aspartaat. Dit is de standaard nomenclatuur voor carbonzuren.
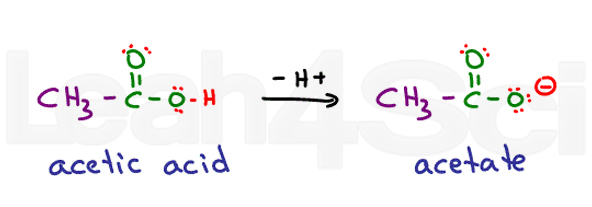
denk aan ethaanzuur. De algemene naam is azijnzuur. Wanneer gedeprotoneerd krijg je acetaat., Zuren zijn zeer stabiel in water omdat ze gedeeltelijk zijn opgeladen in hun geprotoneerde vorm en volledig opgeladen in hun gedeprotoneerde vorm. Dit maakt ze zeer hydrofiel.
glutaminezuur / GlutamateGluE
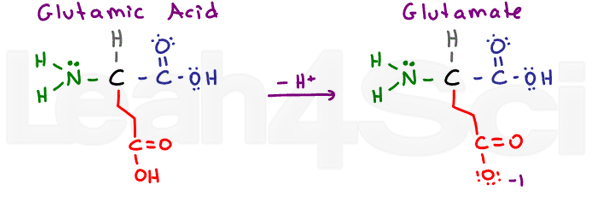
opnieuw hebben we een ‘gluton’ aminozuur met een extra CH2-groep. Glutaminezuur verwijst naar de geprotoneerde zure vorm, en glutamaat verwijst naar de gedeprotoneerde geconjugeerde base/zoutvorm.glutaminezuur is, net als asparaginezuur, zeer stabiel in water en dus hydrofiel.,
basische aminozuren
basische aminozuren bevatten een stikstofatoom met een enkel elektronenpaar dat een waterstofatoom kan aanvallen. Wanneer een basisch aminozuur aan een lage (zure) pH wordt onderworpen, zal het één van de vrije protonen in oplossing grijpen om een geconjugeerd zuurzout te vormen. Deze zijn gemakkelijk te herkennen aan de positieve stikstof in de zijketen. In tegenstelling tot de zure aminozuren, zijn er geen ‘algemeen gebruikte namen’ om voor deze geconjugeerde zouten te onthouden.
LysineLysK
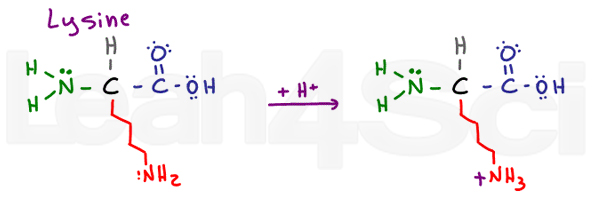
Lysine is een eenvoudig basisch aminozuur., Ondanks een lange en potentieel hydrofobe keten, heeft het een basis NH2 aan het einde. In zijn basis gedeprotoneerde vorm, is lysine neutraal en hydrofiel; echter, indien gevonden in fysiologische pH, zal lysine een H+ Van oplossing opnemen om een NH3+ zout te vormen. Zouten zijn geladen en daarom is arginineargr
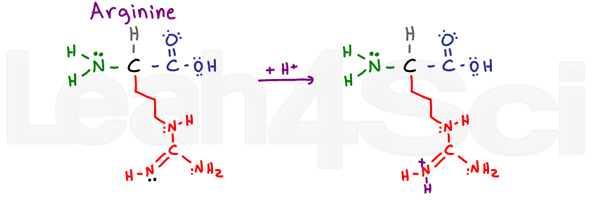
Arginine is verwarrend en doet me zeggen ARGh of R in het kort. Waarom? Het basisgedeelte van deze variabele groep bestaat uit een NH, C=N-H en NH2.,
de twee enkelgebonden stikstofatomen kunnen hun eenzame paren gebruiken om te resoneren met het koolstof-en dubbelgebonden stikstofatoom. Dit maakt hun elektronen niet beschikbaar voor het functioneren als een base. De dubbelgebonden stikstof gebruikt echter zijn pi-binding om te resoneren, waardoor het vrije eenzame paar (in het zwart) als basisstikstof op deze groep fungeert.
Argh!
HistidineHisH

Histidine is een andere lastige basis om dezelfde reden als arginine. Welke stikstof is de basis? Kijk naar de tekening hier, vooral naar de eenzame paren op de 2 stikstofatomen., De histidinering is een heterocyclische aromatische verbinding. Het bovenste stikstofatoom heeft geen pi-binding. Dit betekent dat het zijn eenzame paren moet gebruiken om deel te nemen aan resonantie.het lagere stikstofatoom heeft al een resonerende pi-binding. Dit laat de eenzame elektronen (afgebeeld in het zwart) vrij om een proton te grijpen, waardoor dit het basisatoom is.
concluderend
aminozuren zijn een kritische component voor biologische structuren en voor uw begrip van de biologie en biochemie op het MCAT., Als je alles probeert te onthouden over deze 20 aminozuren, is het belangrijk dat je ook begrijpt waarom je polaire en niet-polaire aminozuren hebt, wat de variabele groep hydrofoob of hydrofiel maakt, en natuurlijk de logica achter geprotoneerde/gedeprotoneerde zure en basische aminozuren.