 Gli amminoacidi sono i mattoni degli esseri viventi. Lunghe catene di aminoacidi costituiscono proteine, che a loro volta costituiscono molti componenti cellulari strutturali e funzionali.
Gli amminoacidi sono i mattoni degli esseri viventi. Lunghe catene di aminoacidi costituiscono proteine, che a loro volta costituiscono molti componenti cellulari strutturali e funzionali.
Mi piace pensare alla cellula come a una città autonoma in cui il nucleo è la capitale, i mitocondri sono la centrale elettrica e così via. Ma poi hai i tuoi lavoratori, il sistema di trasporto e la struttura stessa della città cellulare, che sono tutti fatti di proteine – che a loro volta sono fatti di aminoacidi.,
La complessità di una struttura proteica è determinata dalla sua sequenza di amminoacidi e dalla natura chimica delle loro catene laterali del gruppo variabile. Il MCAT richiede la comprensione della natura delle catene laterali polari e non polari e delle torsioni e conformazioni causate dalle interazioni idrofobiche e idrofile
E sì, dovresti memorizzare ogni amminoacido per il MCAT. Questo include la catena laterale, il nome completo, il nome a 3 lettere e l’abbreviazione a lettera singola. Ma non semplicemente attaccare le parole e le strutture sulle flashcard sperando di forzarlo nella tua memoria., È necessario affrontare attivamente ogni amminoacido individualmente.
Per un elenco di riferimento rapido scarica my free Amino Acid Cheat Sheet Study Guide
- Scrivi il nome completo
- Disegna la struttura dell’amminoacido e il gruppo variabile
- Scrivi le abbreviazioni a 3 lettere e singole lettere
- Verbalizza qualcosa di unico in questa specifica catena laterale-ad alta voce! Più divertente e folle è la connessione, più facile la ricorderai.,
- Ripeti il processo di denominazione/disegno una volta SUBITO
- Ripeti settimanalmente fino a quando non ti senti SOLIDO con queste informazioni
La struttura di base di un amminoacido
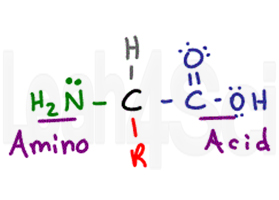 L’amminoacido prende il nome dai suoi due gruppi funzionali primari. L’amminoacido ha un carbonio chirale centrale chiamato carbonio alfa (nero). Attaccato al carbonio centrale si ha un atomo di idrogeno (grigio), un gruppo amminico o NH2 (verde) e un gruppo COOH acido carbossilico (viola). Infine abbiamo il gruppo R (rosso), che è una catena laterale variabile.,
L’amminoacido prende il nome dai suoi due gruppi funzionali primari. L’amminoacido ha un carbonio chirale centrale chiamato carbonio alfa (nero). Attaccato al carbonio centrale si ha un atomo di idrogeno (grigio), un gruppo amminico o NH2 (verde) e un gruppo COOH acido carbossilico (viola). Infine abbiamo il gruppo R (rosso), che è una catena laterale variabile.,
Ci sono 20 diversi aminoacidi che si distinguono per le loro catene laterali uniche. Vanno da un semplice atomo di idrogeno (glicina) a un complesso sistema aromatico risonante a 2 anelli (triptofano).
Mentre la versione completamente neutra sopra è come la maggior parte degli studenti studia gli aminoacidi, e la forma che useremo in questo articolo, tieni presente che questo è tecnicamente errato.
Aminoacido in forma Zwitterion
Poiché il gruppo carbossilico è acido e il gruppo amminico di base, i due esisteranno come zwitterion nelle loro forme cariche coniugate in pH fisiologico., Maggiori informazioni su zwitterion e amminoacido cariche nel mio prossimo articolo (link a seguire).
Un concetto finale prima di abbattere i singoli aminoacidi, e che è la struttura della proteina 3-dimensionale. In una struttura del sistema biologico determina la funzione, quindi comprendere le caratteristiche degli amminoacidi è la chiave per comprendere la struttura e, in definitiva, la funzione proteica.
Struttura primaria di una proteina 3-D
Il primo e più importante fattore di determinazione della struttura proteica è la sequenza di aminoacidi., Se la catena polipeptidica è attaccata in un ordine diverso, si ottiene una struttura complessiva molto diversa.
Struttura secondaria di una proteina 3-D
La struttura secondaria deriva dalle interazioni di legame dell’idrogeno della spina dorsale. Il legame peptidico trasforma ogni ex gruppo carbossilico e amminico in un gruppo funzionale ammidico. La struttura secondaria di alfa elica e beta fogli pieghettati provengono da legame idrogeno tra l’ossigeno parzialmente negativo sul carbonile e l’idrogeno parzialmente positivo sull’azoto.,
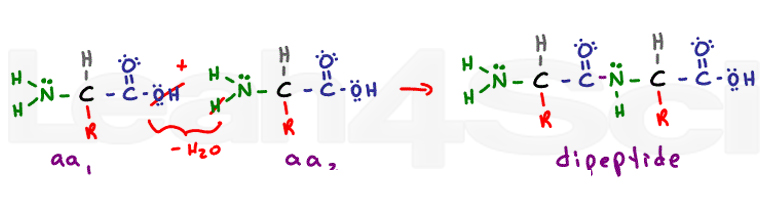
Struttura terziaria di una proteina 3-D
La struttura terziaria è dove viene introdotta la vera piegatura 3-dimensionale, e questa è la prima volta che noterai interazioni a catena laterale. QUESTO è dove la conoscenza e la comprensione delle catene laterali degli aminoacidi sono fondamentali.
Permettetemi di ripetermi, la struttura terziaria è la prima volta che vedrete interazioni variabili della catena laterale del gruppo R sulla catena polipeptidica. Molti studenti confondono questo con la struttura secondaria, che è solo interazioni backbone.,
Struttura quaternaria di una proteina multi-polipeptide 3-D
La struttura quaternaria si riferisce alle interazioni di gruppo variabili tra diversi polipeptidi per formare una singola proteina più grande.
Le strutture quaternarie non si trovano in tutte le proteine. Se la proteina contiene solo un singolo filamento di aminoacidi, il più alto livello di piegatura è la sua struttura terziaria. Tuttavia, se la proteina è costituita da più subunità polipeptidiche, allora la struttura quaternaria è ciò che tiene insieme i diversi polipeptidi.,
Ora che capisci il significato delle caratteristiche della catena laterale, tuffiamoci negli aminoacidi. Tieni presente che poiché i gruppi amminici e carbossilici genitori sono “occupati” con la struttura primaria/secondaria, NON vengono analizzati quando si studiano le proprietà e le caratteristiche della catena laterale.
Questo significa che si ignora qualsiasi potenziale polarità su entrambi i gruppi carbossile e amminico e solo guardare le catene laterali.
Aminoacidi idrofobici non polari
Idrofobo, come suggerisce il nome è idro – acqua, fobico – temendo., Gli amminoacidi idrofobi hanno poca o nessuna polarità nelle loro catene laterali. La mancanza di polarità significa che non hanno modo di interagire con molecole d’acqua altamente polari, rendendole temute dall’acqua.
Ci sono solo cinque atomi che appariranno nei gruppi variabili di aminoacidi: H, C, N, O e S.
Considera la polarità solo quando hai N, O, S come fattore di “maggioranza”. Indicherò questi come si verificano. Tuttavia, se tutto quello che vedi sono Cs e Hs dovresti riconoscere automaticamente un amminoacido che teme l’acqua.,
GlycineGlyG
La glicina è un aminoacido unico in quanto in realtà non ha un gruppo R. Quando pensi al ‘gruppo R variabile’, dovresti pensare al carbonio attaccato ad altri atomi. Ma la glicina ha solo un idrogeno nella sua posizione della catena laterale. Poiché la glicina ha 2 atomi di idrogeno, uno ciascuno sulla catena genitore e laterale, è l’unico amminoacido simmetrico e quindi achirale. Poiché l’idrogeno non è polare, la glicina è un amminoacido idrofobo. La catena laterale dell’idrogeno rende la glicina il più piccolo amminoacido.,
AlanineAlaA
L’alanina è un semplice amminoacido che ha solo un gruppo metilico o CH3 come catena laterale. Poiché non vedi altro che carbonio e idrogeno, l’alanina è un amminoacido idrofobo non polare. È importante riconoscere che questo è un amminoacido molto piccolo e in grado di essere ‘incuneato’ in anelli stretti o catene.
ValineValV
La valina è un altro aminoacido semplice con solo un gruppo variabile isopropile. Proprio come l’alanina, non vediamo altro che carbonio e idrogeno, rendendo la valina un amminoacido idrofobo non polare.,
LeucineLeuL
Puoi riconoscere che la leucina ha lo stesso gruppo variabile della valina ma con un gruppo CH2 in più. Oppure puoi semplicemente riconoscere la sua catena laterale isobutile.
Guarda questo video se non hai familiarità con catene laterali ramificate come isopropile o sec-butile. Poiché la leucina ha solo Cs e Hs, è un amminoacido non polare che teme l’acqua.
IsoleucineIleI
Isoleucina, come suggerisce il nome, è un isomero della leucina. La differenza è il posizionamento del CH3 per un sec-butile piuttosto che una catena laterale isobutile. Proprio come il suo isomero, isoleucina è non polare e idrofobica.,
Metioninemetm
La metionina è il primo amminoacido potenzialmente difficile. La sua catena laterale contiene principalmente Cs e HS ma con un atomo di zolfo incorporato. Mentre potresti pensare che sia idrofilo, presta molta attenzione alla posizione dell’atomo di zolfo. Incorporato nella catena e attaccato a soli atomi di carbonio, lo zolfo è parzialmente “nascosto” dall’ambiente esterno.
Mentre non è necessario conoscere i valori di elettronegatività per il MCAT, aiuta a capire che S = 2.58 e C = 2.55. Poiché la differenza di elettronegatività è inferiore a 0,5, NON c’è polarità su questo sidechain.,
Devi anche riconoscere la metionina come il codone di inizio AGOSTO nella traduzione dell’RNA in proteine.
Fenilalaninefef
Per aiutarla a ricordare che la fenilalanina è F, si ricordi che ‘ph’ è pronunciato come ‘F’. Non mescolare questo con P per prolina.
Prestare attenzione alla struttura della fenilalanina. Ha un singolo gruppo di carbonio con un anello di benzene collegato. Il fenile è il nome di un sostituente del benzene e questa molecola ha un benzene (fenile) attaccato alla struttura dell’alanina. Poiché la fenilalanina non ha altro che Cs e Hs nella sua catena laterale aromatica, è non polare e idrofobica.,
Triptofantrpw
Questo è difficile. Notare la NH in questa catena laterale. N-H dovrebbe essere polare e in grado di legame idrogeno. Tuttavia, ci sono due ragioni per cui questo amminoacido è ancora non polare e idrofobo.
- Il gruppo NH è una piccola porzione della catena laterale molto grande.
- Guarda attentamente l’azoto e, cosa più importante, le sue coppie solitarie. Gli elettroni dell’azoto sono parte integrante dell’aromaticità coniugata per la catena laterale del triptofano., In altre parole, pensa ai suoi elettroni come “troppo distratti” dalla risonanza per prestare molta attenzione all’ambiente idrico esterno.
Il MCAT richiede di riconoscere che si tratta di un amminoacido grande e voluminoso. Ma dal momento che è un esame a scelta multipla si può semplicemente memorizzare che il triptofano è l’UNICO amminoacido con DUE anelli fusi.
In effetti, è così grande che può INCIAMPARE (trp) su se stesso e gridare Waaaaaa (W)
(Nota sulla mnemonica: più divertente, più strano o più sporco è il mnemonico, più è probabile che lo ricorderai. Tienilo a mente per la scuola di medicina.,)
ProlineProP
La prolina è un aminoacido unico poiché è L’UNICO che incorpora la spina dorsale nella sua catena laterale. La catena laterale della prolina è una catena a 3 atomi di carbonio che si avvolge e si attacca al gruppo amminico genitore. Ciò significa che a differenza degli altri amminoacidi, la prolina NON ha un atomo di idrogeno sul suo azoto quando fa parte di una catena polipeptidica.
Tuttavia, non si può dimenticare che l’azoto NON fa REALMENTE parte del gruppo di variabili, il che significa che non può contribuire a nessuna polarità. Dato che abbiamo solo 3 gruppi CH2 da analizzare otteniamo una catena laterale idrofobica non polare., Questo ciclo genitore crea un rigonfiamento e non consente a una catena contenente prolina di essere lineare, il che significa che spesso la troverai nei loop e alla fine di un’elica alfa.
Polar Hydrophobic Amino Acids
*Questa è una sezione appiccicosa e, a seconda di dove si ricerca, è possibile trovare quanto segue classificato come polare o non polare, idrofilo o idrofobo. Prestare attenzione alla presenza di gruppi polari che sono piccoli rispetto al sidechain generale, o molto debolmente polari e quindi idrofobi.,
CisteineCysC
La cisteina ha un S-H leggermente polare, ma la sua polarità è così lieve che la cisteina non è in grado di interagire correttamente con l’acqua rendendola idrofobica.
La cisteina è un aminoacido molto importante quando si tratta di struttura terziaria e quaternaria. La maggior parte delle interazioni a catena laterale includono interazioni polari / cariche o dispersione non polare di Van Der Waals e London. Tuttavia, la catena laterale della cisteina è in grado di formare un ponte disolfuro, che è un legame covalente tra 2 atomi di zolfo attraverso l’ossidazione della catena laterale e la rimozione di 2 atomi di idrogeno., Questo legame covalente è molto più forte e più permanente rispetto alle interazioni terziarie e quaternarie standard.
Questa è anche la causa di un errore sperimentale nel determinare la dimensione/lunghezza della proteina per le proteine con più subunità.
TyrosineTyrY
Alcuni studenti vedono questo come OH che perde da un pneumatico (tyr).
Dai un’occhiata da vicino alla tirosina. Cosa vedi? Sembra la fenilalanina aromatica con un gruppo OH nella posizione para (ortho/meta/para 2nd video).,
Da un lato, abbiamo un gruppo OH molto polare e capace di legame idrogeno, ma d’altra parte, l’OH è piccolo rispetto alle dimensioni del gruppo benzilico (CH2-fenile). Questo enigma è una fonte comune di confusione, ma se lo capisci, riconoscerai che la tirosina, mentre polare, è ancora un amminoacido idrofobo.
Polar Hydrophilic Amino Acids
Hydrophilic come suggerisce il nome deriva da idro-acqua e filic-loving.
La polarità deriva da una differenza di 0,5-1,9 di elettronegatività tra atomi legati., Mentre non devi conoscere questi valori per il MCAT, dovresti riconoscere che i legami polari esisteranno quando N e O sono legati ad atomi non di carbonio.
La differenza di elettronegatività è sufficiente per creare una leggera separazione di carica o polarità. E poiché like attrae like, questi gruppi parzialmente caricati saranno attratti da gruppi caricati in modo opposto o parzialmente caricati come l’acqua. Questi gruppi torceranno la catena polipeptidica per interagire tra loro e con l’acqua.
Gruppi idrofobici si distorcono da queste catene laterali.,
SerineSerS
Pensa alla serina come all’alanina con un gruppo OH collegato. A differenza della tirosina, l’OH è la maggioranza in questa molecola e la sua polarità è sufficiente per influenzare l’intero gruppo. Questo rende la serie polare e molto idrofila.
ThreonineThrT
Ci sono diversi modi per guardare questo gruppo. Si può pensare ad esso come serina con un gruppo metilico in più, o come valina, ma con un OH sostituzione di uno dei gruppi metilici. Ricordo che THREEonine ha 3 gruppi diversi: CH, CH3 e OH.
Come la serina, questo gruppo variabile è polare e idrofilo.,
AsparagineAsnN
Prova questo: Slur il tuo discorso come si dice ‘asparagine’ molto veloce. Sembra che tu stia dicendo COME N N, che è come ricordo l’abbreviazione di 3 lettere per questo amminoacido. L’NH2 alla fine di questa molecola ti fa pensare “base”, ma guarda il suo vicino. NH2 vicino a un carbonile forma un’ammide, che non ama agire come acido o base in condizioni fisiologiche standard. Tuttavia, con cariche parziali e capacità di legame H sia all’ossigeno carbonilico che ai gruppi NH2, otteniamo un amminoacido idrofilo polare.,
GlutamineGlnQ
Penso ad entrambi gli amminoacidi “glut” come ghiottoni che hanno “consumato” un gruppo CH2 in più. La glutammina ha la stessa struttura dell’asparagina ma con un CH2 extra goloso nella sua catena. Proprio come l’asparagina, è polare e idrofila.
Catene laterali degli amminoacidi acidi e basici
L’acidità e la basicità negli amminoacidi sono un’altra fonte di confusione tra gli studenti. Se inizia come un acido, diventa una base? Come faccio a trovare la carica? E così via.
Ecco il trucco: un ACIDO carbossilico nella catena laterale ti darà un amminoacido acido., Quando un gruppo carbossilico è deprotonato, si ottiene un sale base coniugato. Quindi, se vedi la versione salina di una catena laterale dell’acido carbossilico, mentre è TECNICAMENTE una “base coniugata”, ci riferiremo semplicemente ad essa come la versione salina dell’amminoacido acido. Lo stesso per la base. Guardare fuori per’ non distratto ‘ atomi di azoto nella catena laterale.
Aminoacidi acidi
Gli aminoacidi acidi dovrebbero avere un aspetto molto familiare rispetto all’asparagina e alla glutammina. E questo perché tutto su di loro è lo stesso tranne che per il gruppo funzionale terminale., Le ammidi (discusse sopra) sono polari, ma se l’NH2 viene scambiato per un gruppo OH, si ottiene un gruppo carbossilico acido.
Acido aspartico/AspartatoAspD
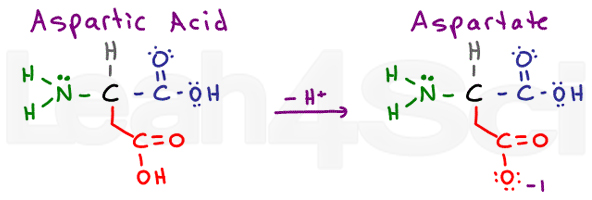
L’acido aspartico si riferisce alla forma acida protonata dell’amminoacido. Quando deprotonato, vedrai spesso il sale di base coniugato indicato come aspartato. Questa è la nomenclatura standard per gli acidi carbossilici.
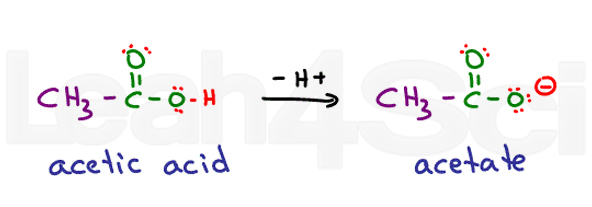
Pensa all’acido etanoico. Il suo nome comune è acido acetico. Quando deprotonato si ottiene acetato., Gli acidi sono molto stabili in acqua poiché sono parzialmente caricati nella loro forma protonata e completamente caricati nella loro forma deprotonata. Questo li rende altamente idrofili.
Acido glutammico / GlutamateGluE
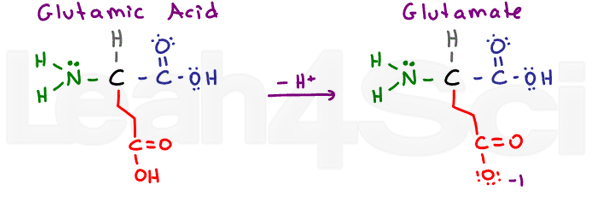
Ancora una volta abbiamo un amminoacido ‘ghiottone’ con un gruppo CH2 in più. L’acido glutammico si riferisce alla forma acida protonata e il glutammato si riferisce alla forma di base/sale coniugato deprotonato.
Come l’acido aspartico, l’acido glutammico è molto stabile in acqua e quindi idrofilo.,
Amminoacidi basici
Gli amminoacidi basici contengono un atomo di azoto con una coppia di elettroni sola in grado di attaccare un atomo di idrogeno. Quando un amminoacido basico è sottoposto ad un pH basso (acido), afferrerà uno dei protoni liberi in soluzione per formare un sale acido coniugato. Questi sono facilmente riconoscibili dall’azoto positivo nella catena laterale. A differenza degli amminoacidi acidi, non ci sono “nomi comunemente usati” da memorizzare per questi sali coniugati.
LysineLysK
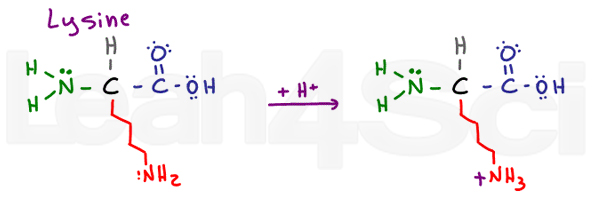
La lisina è un semplice amminoacido basico., Nonostante una catena lunga e potenzialmente idrofobica, ha un NH2 di base alla fine. Nella sua forma deprotonata di base, la lisina è neutra e idrofila; tuttavia, se trovata nel pH fisiologico, la lisina raccoglierà un H + dalla soluzione per formare un sale NH3+. I sali sono carichi e quindi sicuramente idrofili
ArginineArgR
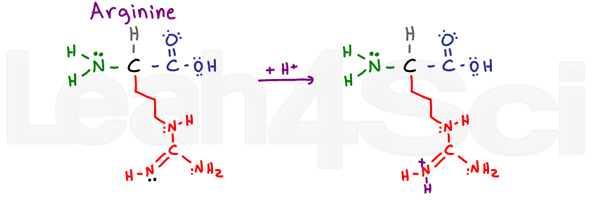
L’arginina è confusa e mi fa dire ARGh o R in breve. Perché? La porzione di base di questo gruppo di variabili è costituita da un NH, C = N-H e NH2.,
I 2 atomi di azoto a legame singolo possono usare le loro coppie solitarie per risuonare con l’atomo di azoto a legame doppio e carbonio. Questo rende i loro elettroni NON DISPONIBILI per agire come base. Tuttavia, l’azoto a doppio legame usa il suo legame pi per risuonare, lasciando la sua coppia solitaria libera (mostrata in nero) ad agire come azoto di base su questo gruppo.
Argh!
Istidinehish

L’istidina è un’altra base difficile per lo stesso motivo dell’arginina. QUALE azoto è quello di base? Guarda il disegno qui, in particolare le coppie solitarie sui 2 atomi di azoto., L’anello di istidina è un composto aromatico eterociclico. L’atomo di azoto superiore non ha un legame pi. Ciò significa che deve usare le sue coppie solitarie per partecipare alla risonanza.
L’atomo di azoto inferiore ha già un legame pi risonante. Questo lascia i suoi elettroni solitari (mostrati in nero) liberi di afferrare un protone, rendendo questo l’atomo di base.
In conclusione
Gli amminoacidi sono una componente critica per le strutture biologiche e per la comprensione della biologia e della biochimica sul MCAT., E così, mentre si tenta di memorizzare tutto su questi 20 aminoacidi, è importante che si capisca anche perché si hanno aminoacidi polari e non polari, ciò che rende il gruppo variabile idrofobo o idrofilo e, naturalmente, la logica dietro gli amminoacidi acidi e basici protonati/deprotonati.