 aminosyror är byggstenarna i levande saker. Långa kedjor av aminosyror utgör proteiner, som i sin tur utgör många strukturella och funktionella cellkomponenter.
aminosyror är byggstenarna i levande saker. Långa kedjor av aminosyror utgör proteiner, som i sin tur utgör många strukturella och funktionella cellkomponenter.
Jag gillar att tänka på cellen som en fristående stad där kärnan är huvudstaden, mitokondrierna är kraftverket och så vidare. Men då har du dina arbetare, transportsystem och själva strukturen i cellstaden, som alla är gjorda av proteiner – som i sin tur är gjorda av aminosyror.,
komplexiteten hos en proteinstruktur bestäms av dess sekvens av aminosyror och den kemiska karaktären hos deras variabla gruppsidkedjor. MCAT kräver förståelse av polära och icke-polära sidokedjor och vridning och konformationer orsakade av hydrofoba och hydrofila interaktioner
och ja, du bör memorera varje aminosyra för MCAT. Detta inkluderar sidokedjan, fullständigt namn, 3-letter namn och enda bokstav förkortning. Men inte bara hålla ord och strukturer på bildkort i hopp om att tvinga det i ditt minne., Du måste aktivt ta itu med varje aminosyra individuellt.
för en snabb referenslista ladda ner min gratis aminosyra Cheat Sheet Study Guide
- Skriv ut det fullständiga namnet
- Rita aminosyrastrukturen och variabel grupp
- Skriv ut 3-bokstaven och enda bokstavsförkortningar
- Verbalize något unikt om denna specifika sidokedja högt! Ju mer rolig och galen anslutningen desto lättare kommer du att komma ihåg det.,
- upprepa namngivningen / ritningsprocessen en gång direkt
- upprepa varje vecka tills du känner dig SOLID med denna information
den grundläggande strukturen hos en aminosyra
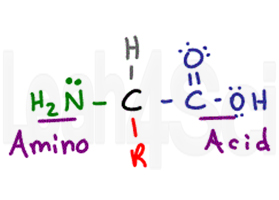 aminosyran får sitt namn från sina två primära funktionella grupper. Aminosyran har ett centralt kiralt kol som kallas alfa-kolet (svart). Ansluten till det centrala kolet har du en väteatom (grå), en amino eller NH2-grupp (grön) och en karboxylsyra COOH-grupp (lila). Slutligen har vi r-gruppen (röd), som är en variabel sidokedja.,
aminosyran får sitt namn från sina två primära funktionella grupper. Aminosyran har ett centralt kiralt kol som kallas alfa-kolet (svart). Ansluten till det centrala kolet har du en väteatom (grå), en amino eller NH2-grupp (grön) och en karboxylsyra COOH-grupp (lila). Slutligen har vi r-gruppen (röd), som är en variabel sidokedja.,
det finns 20 olika aminosyror som utmärks av deras unika sidokedjor. De sträcker sig från en enkel väteatom (glycin) till ett komplext 2-ring resonerande aromatiskt system (tryptofan).
medan den helt neutrala versionen ovan är hur de flesta studenter studerar aminosyror, och formuläret vi använder i den här artikeln, kom ihåg att detta är tekniskt felaktigt.
aminosyra i Zwitterionform
eftersom karboxylgruppen är sur och aminogruppen grundläggande, kommer de två att existera som en zwitterion i deras konjugerade laddade former i Fysiologiskt pH., Mer om zwitterion och aminosyraavgifter i min nästa artikel (länk för att följa).
ett slutkoncept innan vi bryter ner de enskilda aminosyrorna, och det är den tredimensionella proteinstrukturen. I en biologisk systemstruktur bestämmer funktion, så förstå aminosyraegenskaper är nyckeln till att förstå struktur och slutligen proteinfunktion.
primär struktur av ett 3-D-Protein
den första och viktigare bestämningsfaktorn för proteinstruktur är sekvensen av aminosyror., Om polypeptidkedjan är fastsatt i en annan ordning får du en helt annan övergripande struktur.
sekundär struktur av ett 3-D-Protein
den sekundära strukturen kommer från interaktioner mellan ryggraden för vätebindning. Peptidbindningen förvandlar varje tidigare karboxyl-och aminogrupp till en amid funktionell grupp. Den sekundära strukturen av alfa helix och beta Veckade Ark kommer från väte bindning mellan den delvis negativa syre på karbonyl och den delvis positiva väte på kväve.,
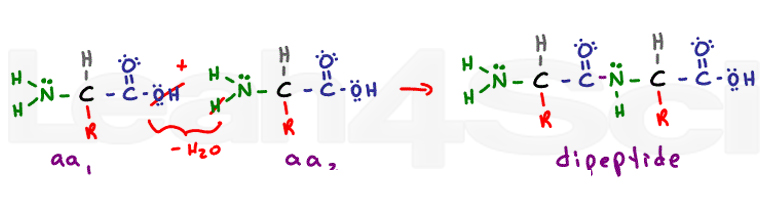
tertiär struktur av ett 3-D-Protein
den tertiära strukturen är där den verkliga 3-dimensionella vikningen introduceras, och det här är första gången du märker sidokedjans interaktioner. Det är där kunskap och förståelse av aminosyra sidokedjor är kritiska.
låt mig upprepa mig själv, tertiär struktur är första gången du ser variabel r-grupp sidokedjeinteraktioner på polypeptidkedjan. Många studenter förvirrar detta med sekundär struktur, som bara är ryggrad interaktioner.,
Quaternary struktur av ett 3-D Multi-Polypeptidprotein
Quaternary struktur avser de variabla gruppinteraktionerna mellan olika polypeptider för att bilda ett enda större protein.
kvartära strukturer finns inte i varje protein. Om proteinet bara innehåller en enda aminosyrasträng, är den högsta vikningsnivån dess tertiära struktur. Men om proteinet består av flera polypeptid subenheter, då kvartära strukturen är vad som håller de olika polypeptider tillsammans.,
nu när du förstår betydelsen av sidokedjeegenskaper, låt oss dyka in i aminosyror. Tänk på att eftersom moderamino-och karboxylgrupperna är ”upptagna” med primär/sekundär struktur, analyseras de inte när de studerar sidokedjeegenskaper och egenskaper.
det betyder att du ignorerar eventuell polaritet på både karboxyl-och aminogrupperna och bara tittar på sidokedjorna.
icke-polära hydrofoba aminosyror
hydrofoba, som namnet antyder är hydro – vatten, fobi – rädsla., Hydrofoba aminosyror har liten eller ingen polaritet i sina sidokedjor. Bristen på polaritet innebär att de inte har något sätt att interagera med mycket polära vattenmolekyler, vilket gör dem vatten rädsla.
det finns bara fem atomer som kommer att visas i dina aminosyravariabelgrupper: H, c, n, o och S.
tänk bara på polaritet när du har N, o, s som ”majoritetsfaktorn”. Jag ska påpeka detta när de inträffar. Men om allt du ser är Cs och Hs bör du automatiskt känna igen en vattenskrämmande aminosyra.,
GlycineGlyG
glycin är en unik aminosyra eftersom den egentligen inte har en R-grupp. När du tänker ”variabel r-grupp,” bör du tänka på kol fäst vid andra atomer. Men glycin har bara ett väte i sidokedjans position. Eftersom glycin har 2 väteatomer, en vardera på moder-och sidokedjan, är det den enda symmetriska och därmed achirala aminosyran. Eftersom väte är icke-polärt är glycin en hydrofob aminosyra. Vätesidan gör glycin till den minsta aminosyran.,
AlanineAlaA
Alanin är en enkel aminosyra som bara har en metyl-eller CH3-grupp som sidokedja. Eftersom du inte ser något annat än kol och väte är alanin en icke-polär hydrofob aminosyra. Det är viktigt att erkänna att detta är en mycket liten aminosyra och kan vara ”inklämd” i snäva loopar eller kedjor.
ValineValV
valin är en annan enkel aminosyra med bara en isopropylvariabel grupp. Precis som alanin ser vi ingenting annat än kol och väte, vilket gör valin till en icke-polär hydrofob aminosyra.,
LeucineLeuL
Du kan känna igen leucin som samma variabla grupp som valin men med en extra CH2-grupp. Eller du kan helt enkelt känna igen dess isobutyl sidokedja.
se den här videon om du inte är bekant med grenade sidokedjor som isopropyl eller sec-butyl. Eftersom leucin bara har Cs och Hs är det en vatten som fruktar icke-polär aminosyra.
IsoleucineIleI
isoleucin, som namnet antyder, är en isomer av leucin. Skillnaden är placeringen av CH3 för en SEK-butyl snarare än en isobutyl sidokedja. Precis som dess isomer är isoleucin nonpolär och hydrofob.,
Metioninemetm
metionin är den första potentiellt knepiga aminosyran. Det är sidokedjan innehåller mestadels Cs och Hs men med en inbäddad svavelatom. Medan du kanske tror att det är hydrofilt, var uppmärksam på svavelatomens placering. Inbäddad i kedjan och fäst vid bara kolatomer, är svavel delvis ”dold” från omgivningen.
medan du inte behöver känna till elektronegativitetsvärden för MCAT hjälper det att förstå att s = 2.58 och C = 2.55. Eftersom skillnaden i elektronegativitet är mindre än 0,5 finns det ingen polaritet på denna sidechain.,
Du måste också känna igen metionin som start kodon AUG i RNA översättning till proteiner.
Fenylalaninephef
för att hjälpa dig att komma ihåg att fenylalanin är f kom ihåg att ” ph ”uttalas som ett ”F”. Blanda inte detta med P för proline.
Var uppmärksam på strukturen av fenylalanin. Den har en enda kolgrupp med en fäst bensenring. Fenyl är namnet på en bensensubstituent, och denna molekyl har en bensen (fenyl) fäst vid alanins struktur. Eftersom fenylalanin har ingenting annat än Cs och Hs i sin aromatiska sidokedja, är det nonpolär och hydrofob.,
Tryptofantrpw
detta är en knepig. Lägg märke till n-H i denna sidokedja. N-h ska vara polär och kunna väte bindning. Det finns dock två anledningar till att denna aminosyra fortfarande är icke-polär och hydrofob.
- n-h-gruppen är en liten del av den mycket stora sidokedjan.
- titta noga på kväve, och ännu viktigare, på sina ensamma par. Kväveens elektroner är integrerade i den konjugerade aromaticiteten för tryptofan-sidokedjan., Med andra ord, Tänk på dess elektroner som ”alltför distraherad” av resonans att ägna stor uppmärksamhet åt den yttre vattenmiljön.
MCAT kräver att du känner igen att detta är en stor och skrymmande aminosyra. Men eftersom det är en flervalsprov kan du helt enkelt memorera att tryptofan är den enda aminosyran med två smälta ringar.
det är faktiskt så stort att det kan resa (trp) över sig själv och gråta ut Waaaaa(W)
(notera på mnemonics: det roligare, konstigare eller smutsigare mnemonic, desto mer sannolikt kommer du att komma ihåg det. Tänk på det här för läkarutbildningen.,)
ProlineProP
prolin är en unik aminosyra eftersom det är den enda som innehåller ryggraden i sin sidokedja. Proline sidokedjan är en 3-kolkedja som loopar runt och fäster tillbaka till moder aminogruppen. Detta innebär att prolin, till skillnad från de andra aminosyrorna, inte har en väteatom på dess kväve när en del av en polypeptidkedja.
Du kan dock inte glömma att kväve egentligen inte ingår i variabelgruppen, vilket innebär att det inte kan bidra med någon polaritet. Eftersom vi bara har 3 CH2-grupper att analysera får vi en icke-polär hydrofob sidokedja., Denna överordnade slinga skapar en bulge och tillåter inte en prolininnehållande kedja att vara linjär, vilket innebär att du ofta hittar den i loopar och i slutet av en alfa helix.
polära hydrofoba aminosyror
*detta är en klibbig sektion, och beroende på var du forskning kan du hitta följande kategoriseras som polära eller icke-polära, hydrofila eller hydrofoba. Var uppmärksam på närvaron av polära grupper som är små jämfört med den övergripande sidechain, eller mycket svagt polära och därför hydrofoba.,
CysteineCysC
cystein har en något polär s-h, men dess polaritet är så mild att cystein inte kan interagera ordentligt med vatten vilket gör det hydrofobiskt.
cystein är en mycket viktig aminosyra när det gäller tertiär och kvaternär struktur. De flesta sidokedjeinteraktioner inkluderar polära / laddade interaktioner eller icke-polära Van Der Waals och London dispersion. Cysteins sidokedja kan emellertid bilda en disulfidbro, som är en kovalent bindning mellan 2 svavelatomer genom sidokedja oxidation och avlägsnande av 2 väteatomer., Denna kovalenta bindning är mycket starkare och mer permanent jämfört med de vanliga tertiära och kvartära interaktionerna.
Detta är också orsaken till experimentellt fel vid bestämning av proteinstorlek/längd för proteiner med flera subenheter.
TyrosineTyrY
vissa studenter ser detta som OH läcker från ett däck (tyr).
ta en närmare titt på tyrosin. Vad ser du? Det ser ut som den aromatiska fenylalaninen med en OH-grupp vid para-positionen (ortho/meta/para 2nd video).,
å ena sidan har vi en mycket polär och vätebindande kapabel OH-grupp, men å andra sidan är OH liten jämfört med bensylgruppens storlek (CH2-fenyl). Detta conundrum är en vanlig källa till förvirring, men om du förstår detta, kommer du att känna igen att tyrosin, medan polar, fortfarande är en hydrofob aminosyra.
polära hydrofila aminosyror
hydrofila som namnet antyder kommer från hydro-vatten och filinälskande.
polaritet kommer från en 0.5-1.9 skillnad i elektronegativitet mellan bundna atomer., Även om du inte behöver veta dessa värden för MCAT, bör du känna igen att polära bindningar kommer att existera när N och O är bundna till icke-kolatomer.
elektronegativitetsskillnaden är tillräcklig för att skapa en liten separation av laddning eller polaritet. Och eftersom som lockar som, dessa delvis laddade grupper kommer att lockas till motsatt laddade eller delvis laddade grupper som vatten. Dessa grupper kommer att vrida polypeptidkedjan för att interagera med varandra och med vatten.
hydrofoba grupper kommer att vrida sig bort från dessa sidokedjor.,
SerineSerS
Tänk på serin som alanin med en OH-grupp bifogad. Till skillnad från tyrosin är OH majoriteten i denna molekyl och dess polaritet är tillräcklig för att påverka hela gruppen. Detta gör serien polar och mycket hydrofila.
ThreonineThrT
det finns flera sätt att titta på denna grupp. Du kan tänka på det som serin med en extra metylgrupp, eller som valin men med en OH som ersätter en av metylgrupperna. Jag minns THREEonine som har 3 olika grupper: CH, CH3, och ÅH.
liksom serin är denna variabla grupp polär och hydrofil.,
AsparagineAsnN
prova detta: Slur ditt tal som du säger ”asparagin” riktigt snabbt. Det låter som du säger som…N, vilket är hur jag kommer ihåg 3-bokstaven förkortningen för denna aminosyra. NH2 i slutet av denna molekyl får dig att tänka ”bas”, men titta på det är granne. NH2 nära en karbonyl bildar en amid, som inte gillar att fungera som en syra eller bas under normala fysiologiska förhållanden. Men med partiella laddningar och h-bindningskapacitet vid både karbonylsyret och NH2-grupperna får vi en polär hydrofil aminosyra.,
GlutamineGlnQ
Jag tänker på båda ”glut” aminosyror som gluttons som har ”konsumerat” en extra CH2-grupp. Glutamin har samma struktur som asparagin men med en extra gluttonös CH2 i sin kedja. Precis som asparagin är det polärt och hydrofilt.
sura och basiska aminosyra sidokedjor
surhet och basicitet i aminosyror är ännu en källa till förvirring bland eleverna. Om det börjar som en syra, blir det en bas? Hur hittar jag avgiften? Och så vidare.
här är tricket: en karboxylsyra i sidokedjan ger dig en sur aminosyra., När en karboxylgrupp deprotoneras får du ett konjugat BASSALT. Så om du ser saltversionen av en karboxylsyra sidokedja, medan det är tekniskt en ”konjugatbas”, hänvisar vi helt enkelt till den som saltversionen av den sura aminosyran. Samma för basen. Håll utkik efter ”icke-distraherade” kväveatomer i sidokedjan.
Sura aminosyror
de sura aminosyrorna ska se mycket bekanta ut jämfört med asparagin och glutamin. Och det beror på att allt om dem är detsamma förutom den terminala funktionella gruppen., Amider (diskuterat ovan) är polära, men om NH2 byts ut för en OH-grupp får du en sur karboxylgrupp.
asparaginsyra/AspartateAspD
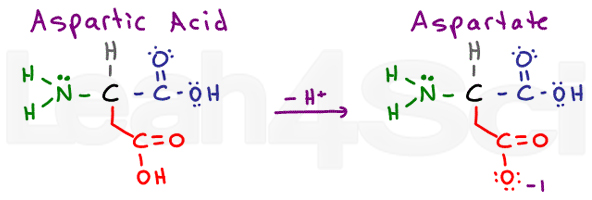
asparaginsyra avser aminosyrans protonerade sura form. När deprotonerade ser du ofta det konjugerade bassaltet som kallas aspartat. Detta är standardnomenklaturen för karboxylsyror.
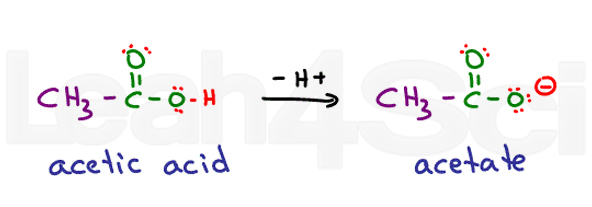
Tänk på etansyra. Dess vanliga namn är ättiksyra. När deprotonerade får du acetat., Syror är mycket stabila i vatten eftersom de är delvis laddade i sin protonerade form och fulladdade i sin deprotonerade form. Detta gör dem mycket hydrofila.
glutaminsyra/GlutamateGluE
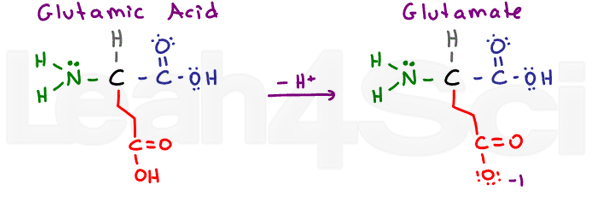
än en gång har vi en ”glutton” aminosyra med en extra CH2-grupp. Glutaminsyra avser den protonerade sura formen, och glutamat refererar till den deprotonerade konjugatbasen/saltformen.
liksom asparaginsyra är glutaminsyra mycket stabil i vatten och därmed hydrofil.,
basiska aminosyror
basiska aminosyror innehåller en kväveatom med ett ensam elektronpar som kan attackera en väteatom. När en basisk aminosyra utsätts för ett lågt (surt) pH, kommer det att ta tag i en av de fria protonerna i lösning för att bilda ett konjugatsyrasalt. Dessa känns lätt igen av det positiva kvävet i sidokedjan. Till skillnad från de sura aminosyrorna finns det inga ”vanliga namn” för att memorera för dessa konjugatsalter.
LysineLysK
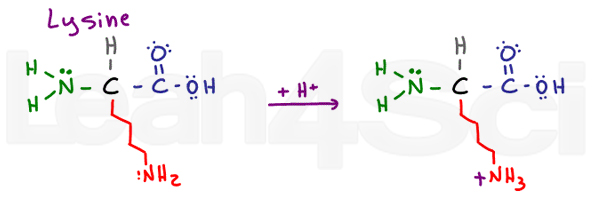
Lysin är en enkel grundläggande aminosyra., Trots en lång och potentiellt hydrofob kedja har den en grundläggande NH2 i slutet. I sin grundläggande deprotonerade form är lysin neutral och hydrofil; om det finns i Fysiologiskt pH, kommer lysin att hämta en h+ Från lösning för att bilda ett NH3+ salt. Salter debiteras och därför definitivt hydrofil
ArginineArgR
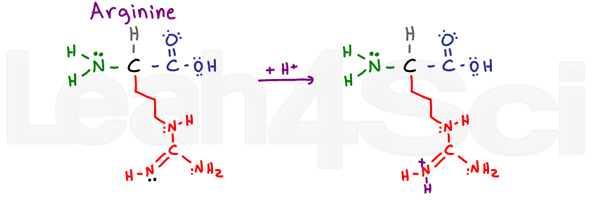
arginin är förvirrande och får mig att säga ARGh eller R för kort. Varför? Den grundläggande delen av denna variabla grupp består av en NH, c=N-h och NH2.,
de 2 enkelbundna kväveatomerna kan använda sina ensamma par för att resonera med kol-och dubbelbunden kväveatom. Detta gör att deras elektroner inte är tillgängliga för att fungera som bas. Det dubbelbundna kvävet använder emellertid sin pi-bindning för att resonera och lämnar sitt fria Lone-par (visas i svart) för att fungera som grundkväve på denna grupp.
Argh!
HistidineHisH

histidin är en annan knepig bas av samma anledning som arginin. Vilket kväve är det grundläggande? Titta på ritningen här, särskilt på de ensamma paren på de 2 kväveatomerna., Histidinringen är en heterocyklisk aromatisk förening. Den övre kväveatomen har inte en pi-bindning. Det betyder att det måste använda sina ensamma par för att delta i resonans.
den lägre kväveatomen har redan en resonans pi-bindning. Detta lämnar sina ensamma elektroner (visas i svart) fri att ta en proton, vilket gör detta till den grundläggande atomen.
Sammanfattningsvis
aminosyror är en kritisk komponent till biologiska strukturer och att du förstår biologi och biokemi på MCAT., Och så, när du försöker memorera allt om dessa 20 aminosyror, är det viktigt att du också förstår varför du har polära och icke-polära aminosyror, vad gör variabelgruppen hydrofoba eller hydrofila, och naturligtvis logiken bakom protonerade / deprotonerade sura och grundläggande aminosyror.