 Aminohapot ovat rakennuspalikoita elävät olennot. Aminohapoista muodostuvat pitkät ketjut muodostavat proteiineja, jotka puolestaan muodostavat monia rakenteellisia ja toiminnallisia solukomponentteja.
Aminohapot ovat rakennuspalikoita elävät olennot. Aminohapoista muodostuvat pitkät ketjut muodostavat proteiineja, jotka puolestaan muodostavat monia rakenteellisia ja toiminnallisia solukomponentteja.
haluan ajatella, että solun itsenäinen kaupunki, jossa ydin on pääkaupunki, mitokondrioita on voimalaitos ja niin edelleen. Mutta sitten on työläiset, kuljetusjärjestelmä ja koko solukaupungin rakenne, jotka kaikki on tehty proteiineista-jotka puolestaan on tehty aminohapoista.,
monimutkaisuus proteiinin rakenne määräytyy sen sekvenssin aminohappoja ja kemiallisen luonteen muuttujaryhmä puolella ketjut. MCAT vaatii ymmärrystä luonne polaarisia ja polaarittomia puolella ketjut ja kiertämällä ja conformations aiheuttama hydrofobinen ja hydrofiilinen vuorovaikutus
Ja kyllä, sinun pitäisi olla ulkoa jokainen aminohappo MCAT. Tähän sisältyy sivuketju, koko Nimi, 3-kirjaiminen nimi ja yhden kirjaimen lyhenne. Mutta älä vain työnnä sanoja ja rakenteita flashcards toivoen pakottaa sen muistiin., Sinun täytyy aktiivisesti puuttua jokaisen aminohapon erikseen.
pikaopas lista ladata vapaa Aminohappo Cheat Sheet Opinto-Opas
- Kirjoita ulos koko nimi
- Piirrä aminohapon rakenne ja muuttuva-ryhmä
- Kirjoita ulos 3-kirjain ja yhden kirjaimen lyhenteitä
- pukemaan Sanoiksi jotain ainutlaatuista tämä erityinen puoli-ketju – ääneen! Mitä hauskempi ja hullumpi yhteys, sitä helpommin sen muistaa.,
- Toista uudelleen nimeäminen/piirustus prosessi, kun HETI
- Toistetaan viikoittain, kunnes tunnet VANKKA tieto
perusrakenne Aminohappo
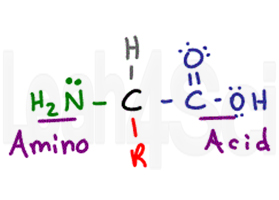 aminohappo saa nimensä sen kaksi ensisijainen toiminnallisia ryhmiä. Aminohapolla on keskeinen kiraalinen hiili, jota kutsutaan alfahiileksi (mustaksi). Keskeiseen hiileen on kiinnitetty vetyatomi (harmaa), amino-tai NH2-ryhmä (vihreä) ja karboksyylihapporyhmä (violetti). Lopuksi meillä on R-ryhmä (punainen), joka on vaihteleva sivuketju.,
aminohappo saa nimensä sen kaksi ensisijainen toiminnallisia ryhmiä. Aminohapolla on keskeinen kiraalinen hiili, jota kutsutaan alfahiileksi (mustaksi). Keskeiseen hiileen on kiinnitetty vetyatomi (harmaa), amino-tai NH2-ryhmä (vihreä) ja karboksyylihapporyhmä (violetti). Lopuksi meillä on R-ryhmä (punainen), joka on vaihteleva sivuketju.,
On olemassa 20 erilaista aminohappoa ominaista niiden ainutlaatuinen puolella ketjut. Ne vaihtelevat yksinkertaisesta vetyatomista (glysiini) monimutkaiseen 2-rengasresonoivaan aromaattiseen järjestelmään (tryptofaani).
Vaikka täysin neutraali versio edellä on miten useimmat opiskelijat opiskelevat aminohappoja, ja muoto käytämme tässä artikkelissa, pitää mielessä, että tämä on teknisesti virheellinen.
Aminohappo Zwitterion Muodossa
Koska karboksyyliryhmä on hapan ja amino-ryhmä basic, kaksi on olemassa zwitterion niiden konjugoitu ladattu muotoja fysiologinen pH., Lisää zwitterion ja aminohappo maksut minun seuraava artikkeli (linkki seurata).
yksi lopullinen käsite ennen kuin hajotamme yksittäiset aminohapot, ja se on 3-ulotteinen proteiinirakenne. Biologisessa järjestelmässä rakenne määrittää toiminto, joten ymmärrystä aminohappo ominaisuudet on avain ymmärtää rakenteen ja lopulta proteiinin toiminnan.
Ensisijainen Rakenne 3-D-Proteiini
ensimmäinen ja tärkeämpi määrittäminen tekijä proteiinin rakenne on sekvenssin aminohappoja., Jos polypeptidiketju kiinnitetään eri järjestyksessä, saadaan hyvin erilainen Kokonaisrakenne.
3-D-proteiinin toissijainen rakenne
toissijainen rakenne tulee runkovetysidosinteraktioista. Peptidisidos muuttaa jokaisen entisen karboksyyli-ja aminoryhmän amidin funktionaaliseksi ryhmäksi. Toissijainen rakenne alfa-helix ja beta laskostettu levyt tulevat vety liimaus välillä osittain negatiivinen happi on karbonyyli ja osittain positiivisia vety on typpeä.,
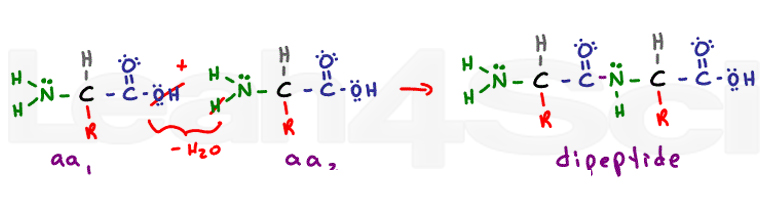
korkea-Asteen Rakenne 3-D-Proteiini
korkea-asteen rakenne on todellinen 3-ulotteinen taitto on otettu käyttöön, ja tämä on ensimmäinen kerta, kun huomaat, side-ketju vuorovaikutusta. Tässä aminohappojen sivuketjujen tuntemus ja ymmärtäminen ovat kriittisiä.
toistan itseäni, korkea-asteen rakenne on ensimmäinen kerta, kun näet muuttuja R-ryhmän puolella ketju vuorovaikutusta polypeptidi ketju. Monet opiskelijat sekoittavat tämän toissijaiseen rakenteeseen, joka on vain selkärangan vuorovaikutusta.,
Kvaternaarinen Rakenne 3-D-Multi-Polypeptidi Proteiinia
Kvaternaarinen rakenne viittaa muuttujan ryhmän vuorovaikutusta eri polypeptidit muodostavat yhden suuremman proteiinia.
kvaternaarisia rakenteita ei löydy jokaisesta proteiinista. Jos proteiini sisältää vain yhden aminohapon juosteen, niin korkein taitto on sen tertiäärinen rakenne. Jos proteiini kuitenkin koostuu useista polypeptidialayksiköistä, kvaternaarinen rakenne pitää eri polypeptidit koossa.,
nyt kun ymmärrät sivuketjun ominaisuuksien merkityksen, sukelletaan aminohappoihin. Pidä mielessä, että koska vanhempi amino-ja karboksyyliryhmiä ovat ’kiireinen’ kanssa ensisijainen/toissijainen rakenne, ne ovat EI analysoidaan, kun opiskelu puoli-ketjun ominaisuudet ja ominaispiirteet.
tämä tarkoittaa, että jätät huomiotta mahdollisen polariteetin sekä karboksyyli-että aminoryhmissä ja katsot vain sivuketjuja.
ei-polaariset hydrofobiset aminohapot
hydrofobinen, kuten nimestä voi päätellä, on vesi, fobiaa pelkäävä., Hydrofobisilla aminohapoilla on vain vähän tai ei lainkaan napaisuutta sivuketjuissaan. Napaisuuden puute tarkoittaa, että niillä ei ole mitään keinoa vuorovaikutuksessa erittäin polaaristen vesimolekyylien kanssa, mikä tekee niistä vettä pelkääviä.
On olemassa vain viisi atomit, jotka näkyvät aminohappo muuttujan ryhmät: H, C, N, O, ja S.
Vain harkita napaisuus, kun sinulla on N, O, S ’enemmistö’ tekijä. Osoitan nämä, kun niitä tapahtuu. Kuitenkin, jos kaikki näet ovat Cs ja Hs sinun pitäisi automaattisesti tunnistaa vettä pelkäävä aminohappo.,
GlycineGlyG
Glysiini on ainutlaatuinen aminohappo, että se ei ole R-ryhmän. Kun ajattelee ’muuttuvaa R-ryhmää’, pitäisi ajatella hiiliä, joka on kiinnittynyt muihin atomeihin. Glysiinillä on kuitenkin vain vety sivuketjuasennossaan. Koska glysiini on 2 vetyatomia, yksi jokaisen vanhemman ja puolella ketju, se on vain symmetrinen ja siten achiral aminohappo. Koska vety ei ole polaarinen, glysiini on hydrofobinen aminohappo. Vedyn sivuketju tekee glysiinistä pienimmän aminohapon.,
AlanineAlaA
Alaniini on yksinkertainen aminohappo, joka on vain metyyli-tai CH3-ryhmän kuin sen puolella ketju. Koska näet vain hiiltä ja vetyä, alaniini on ei-polaarinen hydrofobinen aminohappo. On tärkeää tunnistaa, että kyseessä on hyvin pieni aminohappo, joka pystyy ”kiilaamaan” tiukkoihin silmukoihin tai ketjuihin.
ValineValV
Valiini on toinen yksinkertainen aminohappo vain isopropyyli muuttujan ryhmä. Aivan kuten alanine, emme näe muuta kuin hiiltä ja vetyä, mikä tekee valinesta ei-polaarisen hydrofobisen aminohapon.,
LeucineLeuL
Voit tunnistaa leusiini kuin ottaa sama muuttuja ryhmä kuten valiini, mutta ylimääräinen CH2-ryhmä. Tai voit yksinkertaisesti tunnistaa sen isobutyylin sivuketjun.
Katso video, jos haarautuneet sivuketjut, kuten isopropyyli tai sek-butyyli, eivät ole sinulle tuttuja. Koska leusiinilla on vain Cs ja Hs, se on vettä pelkäävä ei-polaarinen aminohappo.
isoleusiini
isoleusiini on nimensä mukaisesti leusiinin isomeeri. Erona on CH3: n sijoitus sek-butyylille isobutyylin sivuketjun sijaan. Isomeerinsa tavoin isoleusiini on nonpolaarinen ja hydrofobinen.,
MethionineMetM
Metioniini on ensimmäinen mahdollisesti hankala aminohappo. Sen sivuketjussa on enimmäkseen Cs: ää ja Hs: tä, mutta siihen on upotettu rikkiatomi. Vaikka saatat pitää sitä hydrofiilisenä, kiinnitä tarkkaa huomiota rikkiatomin sijaintiin. Upotettu ketju ja kiinnitetty vain hiiliatomia, rikki on osittain ”piilossa” ulkopuolelta ympäristöstä.
Vaikka sinun ei tarvitse tietää, elektronegatiivisuus arvot MCAT se auttaa ymmärtämään, että S = 2.58 ja C = 2.55. Koska elektronegatiivisuus ero on alle 0.5, EI napaisuus tämän sidechain.,
Sinun on myös tunnustavat, metioniini alku kodonissa ELOKUU RNA käännös proteiineja.
Fenyylialaninephef
auttaa muistamaan, että fenyylialaniini on F muista, että ” ph ”äännetään ” F”. Älä sekoita tätä P for prolineen.
kiinnitä huomiota fenyylialaniinin rakenteeseen. Sillä on yksi hiiliryhmä, johon on kiinnitetty bentseenirengas. Fenyyli on nimi bentseeni substituentin, ja tämä molekyyli on bentseeni (fenyyli), joka on kiinnitetty rakenteeseen alaniini. Koska fenyylialaniini on mitään, mutta Cs ja Hs-sen aromaattinen sivuketju, se on ei-polaarisia ja hydrofobinen.,
Tryptofantrpw
Tämä on hankala. Huomaa n-H tässä sivuketjussa. N-H: n tulisi olla polaarinen ja kyetä sitoutumaan vetyyn. On kuitenkin kaksi syytä, miksi tämä aminohappo on edelleen ei-polaarinen ja hydrofobinen.
- N-H-ryhmä on pieni osa hyvin suuresta sivuketjusta.
- katso tarkasti typpeä ja ennen kaikkea sen yksinäisiä pareja. Typen elektronit ovat erottamaton osa tryptofaanin sivuketjun konjugoitunutta aromaattisuutta., Toisin sanoen, ajattele sen elektronit ”liian hajamielinen” resonanssi kiinnittää paljon huomiota ulkoiseen vesiympäristöön.
MCAT vaatii sinua tunnistamaan, että kyseessä on suuri ja tilaa vievä aminohappo. Mutta koska se on monivalintakoe voit yksinkertaisesti muistaa, että tryptofaani on ainoa aminohappo, jossa on kaksi sulatettua rengasta.
Itse asiassa, se on niin iso, se voi MATKAN (trp) yli itse ja itkeä ulos Waaaaaa (W)
(Huom muistitekniikka: hauskempi, oudompaa, tai likaisempaa muistisääntö, sitä todennäköisemmin muistat sen. Pidä tämä mielessä lääkiksessä.,)
ProlineProP
Proline on ainutlaatuinen aminohappo, koska se on AINOA, joka sisältää selkäranka sen puolella ketju. Proliinin sivuketju on 3-Hiilinen ketju, joka kiertää ja kiinnittyy takaisin emoaminoryhmään. Tämä tarkoittaa sitä, että toisin kuin muut aminohapot, proliini ei OLE vetyatomi sen typen kun osa polypeptidi ketju.
ei kuitenkaan voi unohtaa, että typpi ei todellisuudessa kuulu muuttujan ryhmään, eli se ei voi edistää mitään napaisuutta. Koska meillä on vain 3 CH2 ryhmää analysoitavana, saamme ei-solaarisen hydrofobisen sivuketjun., Tämä vanhempi-silmukka luo pullistuma ja ei salli proliini sisältävä ketju on lineaarinen, mikä tarkoittaa, voit usein löytää sen silmukoita ja lopussa alfa-helix.
Polar Hydrofobisia Aminohappoja
*Tämä on tahmea jakso, ja riippuen siitä, missä tutkimus, saatat löytää seuraavia luokiteltu polar tai ei-polaarisia, hydrofiilinen tai hydrofobinen. Kiinnitä huomiota läsnäolo polar ryhmiä, jotka ovat pieniä verrattuna koko sidechain, tai hyvin heikosti polaarinen ja siksi hydrofobinen.,
CysteineCysC
Kysteiini on hieman polar S-S, mutta sen napaisuus on niin lievä, että kysteiini ei pysty kunnolla vuorovaikutuksessa veden kanssa, jolloin se on hydrofobinen.
kysteiini on erittäin tärkeä aminohappo tertiäärisen ja kvaternaarisen rakenteen suhteen. Useimmat sivuketjujen vuorovaikutukset ovat polaarisia / varautuneita vuorovaikutuksia tai ei-polaarisia Van Der Waalsia ja Lontoon dispersiota. Kuitenkin, kysteiini puolella ketju pystyy muodostamaan disulfidi silta, joka on kovalenttisten joukkovelkakirjojen välillä 2 rikki atomit kautta sivuketjun hapettumista ja poisto 2 vetyatomia., Tämä kovalenttinen sidos on paljon vahvempi ja pysyvämpi verrattuna standardi korkea-asteen ja kvaternaariset vuorovaikutusta.
Tämä on myös syynä kokeelliseen virheeseen määritettäessä proteiinin kokoa / pituutta proteiineille, joilla on useita alayksiköitä.
TyrosineTyrY
Jotkut opiskelijat näkevät tämän VOI vuotaa renkaan (tyr).
katso tyrosiinia tarkasti. Mitä näet? Se näyttää aromaattiselta fenyylialaniinilta, jolla on OH-ryhmä para-asennossa (Orto/meta/para 2nd video).,
toisaalta, meillä on hyvin napa-ja vety-bond pystyy OH-ryhmä, mutta toisaalta, tuo on pieni verrattuna koko bentsyyli-ryhmä (CH 2-fenyyli). Tämä arvoitus on yleinen sekaannuksen lähde, mutta jos ymmärrät tämän, tunnistat, että tyrosiini, kun taas polar, on yhä hydrofobinen aminohappo.
polaariset hydrofiiliset aminohapot
hydrofiilinen nimensä mukaisesti tulee vesivoimasta ja filisestä.
polaarisuus tulee 0,5-1,9 erotuksesta elektronegatiivisuudessa sidottujen atomien välillä., Vaikka sinun ei tarvitse tietää nämä arvot MCAT, sinun pitäisi tunnustavat, että polar joukkovelkakirjalainat ovat olemassa, kun N-ja O ovat varmasti ei-hiiliatomia.
elektronegatiivisuusero riittää loivaan varauksen tai napaisuuden erotteluun. Ja koska kuten houkuttelee kuten, nämä osittain varautuneita ryhmiä puoleensa vastakkaisesti varautuneita tai osittain varautuneita ryhmiä, kuten vettä. Nämä ryhmät kiertävät polypeptidiketjua vuorovaikutuksessa toistensa ja veden kanssa.
hydrofobiset ryhmät kiertyvät pois näistä sivuketjuista.,
SerineSerS
Ajattele seriini kuten alaniini, joissa OH-ryhmä liitteenä. Toisin kuin tyrosiini, OH on suurin osa tästä molekyylistä ja sen napaisuus riittää vaikuttamaan koko ryhmään. Tämä tekee sarjoista polaarisia ja erittäin hydrofiilisiä.
Treoninetrt
on olemassa useita tapoja tarkastella tätä ryhmää. Voit ajatella sitä kuin seriini ylimääräinen metyyli-ryhmä, tai kuten valiini, mutta ÄLÄ korvaa yksi metyyli-ryhmiä. Muistan, että Threeoninella oli 3 eri ryhmää: CH, CH3 ja OH.
seriinin tavoin tämä muuttuva ryhmä on polaarinen ja hydrofiilinen.,
AsparagineAsnN
Kokeile tätä: Sammaltaa puhe kuten sanot ’asparagiini’ todella nopeasti. Kuulostaa siltä, että sanot ”N”, josta muistan tämän aminohapon 3-kirjaimen lyhenteen. Tämän molekyylin päässä oleva NH2 saa sinut ajattelemaan ’emästä’, Mutta katso, se on naapuri. NH2 karbonyylin lähellä muodostaa amidin, joka ei halua toimia happona tai emäksenä normaaleissa fysiologisissa olosuhteissa. Kuitenkin, osittainen maksut ja H-liimaus valmiudet sekä karbonyyli happea JA NH2-ryhmiä, saamme polar hydrofiilinen aminohappo.,
GlutamineGlnQ
uskon, että sekä ’glut’ aminohappoja kuten gluttons ottaa ’kulutetaan’ ylimääräistä CH2-ryhmä. Glutamiinilla on sama rakenne kuin asparagiinilla, mutta sen ketjussa on ylimääräinen ahmattimainen CH2. Asparagiinin tavoin se on polaarinen ja hydrofiilinen.
happamat ja emäksiset aminohappojen sivuketjut
aminohappojen happamuus ja emäksisyys ovat jälleen yksi hämmennyksen aiheuttaja opiskelijoiden keskuudessa. Jos se alkaa happona, tuleeko siitä emäs? Miten löydän syytteen? Ja niin edelleen.
tässä juju: sivuketjun karboksyylihappo antaa happaman aminohapon., Kun karboksyyliryhmä deprotonoidaan, saadaan konjugaattiemäsuolaa. Joten jos näet, suola versio karboksyylihappo puolella ketju, kun se on TEKNISESTI ’konjugaatti, pohja,’ me yksinkertaisesti kutsuvat sitä suolaa versio hapan aminohappo. Sama tukikohdalle. Varo sivuketjun ”hajamielisiä” typpiatomeja.
happamat aminohapot
happamien aminohappojen tulisi näyttää hyvin tutuilta verrattuna asparagiiniin ja glutamiiniin. Ja se johtuu siitä, että kaikki niissä on sama paitsi terminaalinen funktionaalinen ryhmä., Amidit (edellä mainittu) ovat polaarisia, mutta jos NH2 vaihtuu OH-ryhmään, saat happaman karboksyyliryhmän.
Asparagiinihappo / AspartateAspD
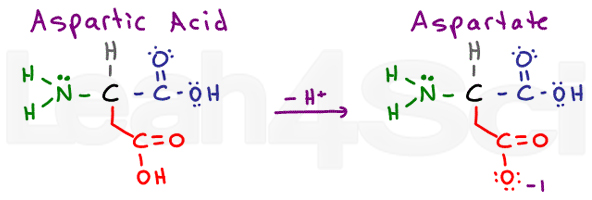
Asparagiinihappo viittaa protonoidut happamassa muodossa aminohappo. Deprotonoituna näet usein konjugaattiemäsuolan, jota kutsutaan aspartaatiksi. Tämä on karboksyylihappojen standardinimikkeistö.
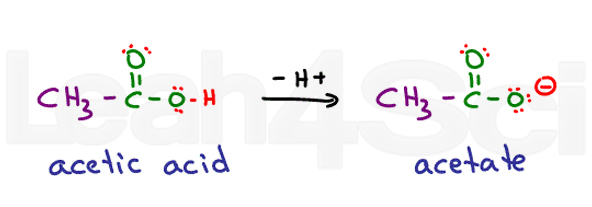
Ajattele ethanoic happoa. Sen yleisnimi on etikkahappo. Deprotonoituna saat asetaattia., Hapot ovat hyvin stabiileja vedessä, koska ne ovat osittain ladattu niiden protonoidut muodossa ja täysin ladattu niiden deprotonated muodossa. Tämä tekee niistä erittäin hydrofiilisiä.
Glutamiinihappo / GlutamateGluE
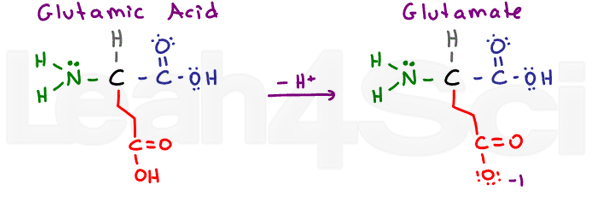
jälleen Kerran meillä on ’ahmatti’ aminohappo ylimääräinen CH2-ryhmä. Glutamiinihappo viittaa protonoituun happamaan muotoon ja glutamaatti deprotonoituun konjugaattiemäkseen / suolamuotoon.
asparagiinihapon tavoin glutamiinihappo on hyvin stabiili vedessä ja siten hydrofiilinen.,
Perusaminohapot
perusaminohapot sisältävät typpiatomin, jonka yksinäinen elektronipari kykenee hyökkäämään vetyatomin kimppuun. Kun perus aminohappo on tehty matala (hapan) pH, se on napata yksi ilmainen protonien ratkaisu muodostaa konjugaatti happo suolaa. Nämä tunnistaa helposti sivuketjun positiivisesta typestä. Toisin happamia aminohappoja, ei ole ’yleisesti käytettyjä nimiä’ muistaa nämä konjugaatti suolat.
LysineLysK
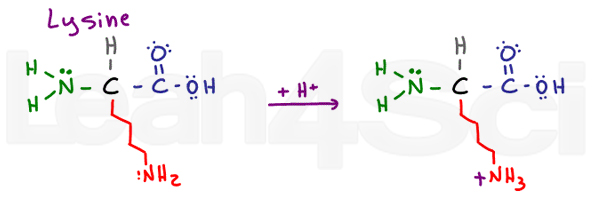
Lysiini on yksinkertainen perus aminohappo., Pitkästä ja mahdollisesti hydrofobisesta ketjusta huolimatta sen päässä on perusnh2. Sen perus deprotonated muodossa, lysiini on neutraali ja hydrofiilinen; kuitenkin, jos se esiintyy fysiologisessa pH, lysiini poimia H+ ratkaisu muodostaa NH3+ suolaa. Suolat ovat ladattu ja siksi ehdottomasti hydrofiilinen
ArginineArgR
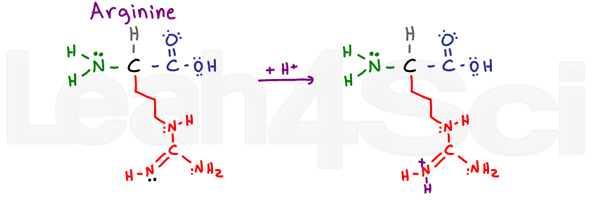
Arginiini on sekava ja tekee minut sanoa ARGh tai R lyhyen. Miksi? Perus osa tämän muuttujan ryhmä koostuu NH, C=N-S ja NH2.,
2 yhden sidottu typpi-atomeja voi käyttää heidän lone paria tehoavat hiilen ja kaksinkertainen sidottu typpi-atomi. Tämän vuoksi niiden elektroneja ei voida käyttää emäsinä toimimiseen. Kuitenkin, double-sidottu typpi käyttää sen pi bond resonoimaan, jolloin sen ilmaiseksi yksinäinen pari (kuvassa musta) toimia perus-typen tähän ryhmään.
Argh!
HistidineHisH

Histidiini on toinen hankala pohja samasta syystä kuin arginiini. Mikä typpi on perus? Katso piirustus tässä, erityisesti yksinäinen paria 2 typpiatomia., Histidiinirengas on heterosyklinen aromaattinen yhdiste. Ylemmässä typpiatomissa ei ole pii-sidosta. Tämä tarkoittaa, että sen on käytettävä yksinäisiä parejaan osallistuakseen resonanssiin.
matalammassa typpiatomissa on jo resonoiva pii-sidos. Tämä jättää yksinäiset elektroninsa (jotka näkyvät mustana) vapaiksi tarttumaan protoniin, mikä tekee tästä perusatomin.
lopuksi
Aminohapot ovat kriittinen komponentti biologisia rakenteita ja sinun ymmärtää, biologian ja biokemian MCAT., Ja niin, kuin sinä yrittää muistaa kaikki näistä 20 aminohappoja, se on tärkeää, että ymmärrät myös, miksi sinulla on polaarisia ja polaarittomia aminohappoja, mikä tekee muuttujaryhmä hydrofobinen tai hydrofiilinen, ja tietenkin, logiikka protonoidut/deprotonated happamia ja emäksisiä aminohappoja.