 los aminoácidos son los bloques de construcción de los seres vivos. Las cadenas largas de aminoácidos forman las proteínas, que a su vez forman muchos componentes estructurales y funcionales de las células.
los aminoácidos son los bloques de construcción de los seres vivos. Las cadenas largas de aminoácidos forman las proteínas, que a su vez forman muchos componentes estructurales y funcionales de las células.
Me gusta pensar en la célula como una ciudad autónoma donde el núcleo es la capital, la mitocondria es la planta de energía y así sucesivamente. Pero luego están los trabajadores, el sistema de transporte y la estructura misma de la ciudad celular, que están hechos de proteínas, que a su vez están hechos de aminoácidos.,
la complejidad de una estructura proteica está determinada por su secuencia de aminoácidos y la naturaleza química de sus cadenas laterales de grupos variables. El MCAT requiere comprender la naturaleza de las cadenas laterales polares y no polares y la torsión y las conformaciones causadas por interacciones hidrofóbicas e hidrofílicas
y sí, debe memorizar cada aminoácido para el MCAT. Esto incluye la cadena lateral, el nombre completo, el nombre de 3 letras y la abreviatura de una sola letra. Pero no se limite a pegar las palabras y estructuras en tarjetas de memoria con la esperanza de forzar en su memoria., Es necesario abordar activamente cada aminoácido individualmente.
para obtener una lista de referencia rápida, descargue mi guía de estudio de la hoja de trucos de aminoácidos
- escriba el nombre completo
- dibuje la estructura de aminoácidos y el grupo variable
- escriba las abreviaturas de 3 letras y una sola letra
- Verbalice algo único sobre esta cadena lateral específica: ¡en voz alta! Cuanto más divertida y loca sea la conexión, más fácil será recordarla.,
- repita el proceso de nombrar/dibujar una vez de inmediato
- repita semanalmente hasta que se sienta sólido con esta información
la estructura básica de un aminoácido
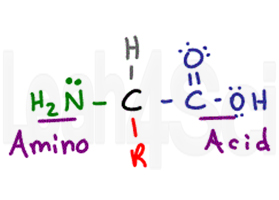 el aminoácido recibe su nombre de sus dos grupos funcionales primarios. El aminoácido tiene un carbono quiral central llamado carbono alfa (negro). Unido al carbono central tiene un átomo de hidrógeno (gris), un grupo amino o NH2 (verde), y un grupo COOH ácido carboxílico (púrpura). Finalmente tenemos el grupo R (rojo), que es una cadena lateral variable.,
el aminoácido recibe su nombre de sus dos grupos funcionales primarios. El aminoácido tiene un carbono quiral central llamado carbono alfa (negro). Unido al carbono central tiene un átomo de hidrógeno (gris), un grupo amino o NH2 (verde), y un grupo COOH ácido carboxílico (púrpura). Finalmente tenemos el grupo R (rojo), que es una cadena lateral variable.,
hay 20 aminoácidos diferentes que se distinguen por sus cadenas laterales únicas. Van desde un simple átomo de hidrógeno (glicina) hasta un complejo sistema aromático resonante de 2 anillos (triptófano).
mientras que la versión completamente neutral anterior es cómo la mayoría de los estudiantes estudian los aminoácidos, y la forma que usaremos en este artículo, tenga en cuenta que esto es técnicamente incorrecto.
aminoácido en forma de Zwitterion
dado que el grupo carboxilo es ácido y el grupo amino básico, los dos existirán como zwitterion en sus formas cargadas conjugadas en pH fisiológico., Más sobre zwitterion y las cargas de aminoácidos en mi próximo artículo (enlace a seguir).
un concepto final antes de descomponer los aminoácidos individuales, y que es la estructura de la proteína de 3 dimensiones. En un sistema biológico, la estructura determina la función, por lo que comprender las características de los aminoácidos es clave para comprender la estructura y, en última instancia, la función de las proteínas.
estructura primaria de una proteína 3-D
el primer y más importante factor de determinación de la estructura de la proteína es la secuencia de aminoácidos., Si la cadena del polipéptido está unida en un orden diferente, se obtiene una estructura general muy diferente.
estructura secundaria de una proteína 3-D
La estructura secundaria proviene de las interacciones de enlace de hidrógeno de la columna vertebral. El enlace peptídico convierte cada grupo carboxilo y amino anterior en un grupo funcional de amida. La estructura secundaria de la hélice alfa y las láminas plisadas beta provienen de la Unión de hidrógeno entre el oxígeno parcialmente negativo en el carbonilo y el hidrógeno parcialmente positivo en el nitrógeno.,
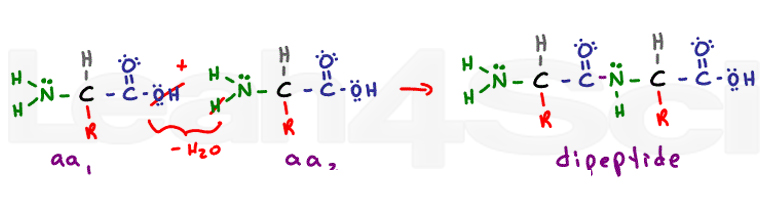
estructura terciaria de una proteína 3-D
La estructura terciaria es donde se introduce el plegado real de 3 dimensiones, y esta es la primera vez que notará interacciones de cadena lateral. Aquí es donde el conocimiento y la comprensión de las cadenas laterales de aminoácidos son críticos.
permítanme repetirme, la estructura terciaria es la primera vez que verá interacciones variables de la cadena lateral del grupo R en la cadena polipeptídica. Muchos ESTUDIANTES Confunden esto con la estructura secundaria, que es solo interacciones troncales.,
estructura cuaternaria de una proteína Multi-Polipéptida 3-D
La estructura cuaternaria se refiere a las interacciones de grupos variables entre diferentes polipéptidos para formar una sola proteína más grande.
las estructuras cuaternarias no se encuentran en todas las proteínas. Si la proteína contiene solo una sola cadena de aminoácidos, entonces el nivel más alto de plegamiento es su estructura terciaria. Sin embargo, si la proteína se compone de subunidades múltiples del polipéptido, entonces la estructura cuaternaria es qué sostiene a los diversos polipéptidos juntos.,
ahora que entiendes el significado de las características de la cadena lateral, vamos a sumergirnos en los aminoácidos. Tenga en cuenta que dado que los grupos amino y carboxilo están ‘ocupados’ con la estructura primaria/secundaria, no se analizan al estudiar las propiedades y características de la cadena lateral.esto significa que ignoras cualquier polaridad potencial en ambos grupos carboxilo y amino y solo miras las cadenas laterales.
aminoácidos hidrofóbicos no polares
hidrofóbicos, como su nombre lo indica, son hidrofóbicos., Los aminoácidos hidrofóbicos tienen poca o ninguna polaridad en sus cadenas laterales. La falta de polaridad significa que no tienen forma de interactuar con moléculas de agua altamente polares, lo que las hace temer al agua.
solo hay cinco átomos que aparecerán en sus grupos de variables de aminoácidos: H, C, N, O y S.
solo considere la polaridad cuando tenga N, O, S como el factor ‘mayoritario’. Los señalaré a medida que ocurran. Sin embargo, si todo lo que ve es Cs y Hs, debe reconocer automáticamente un aminoácido que teme al agua.,
Glicineglyg
La glicina es un aminoácido único en el que realmente no tiene un grupo R. Cuando piensas en ‘grupo R variable’, deberías pensar en carbono unido a otros átomos. Pero la glicina solo tiene un hidrógeno en su posición de cadena lateral. Dado que la glicina tiene 2 átomos de hidrógeno, uno cada uno en la cadena principal y lateral, es el único aminoácido simétrico y por lo tanto aquiral. Dado que el hidrógeno no es polar, la glicina es un aminoácido hidrofóbico. La cadena lateral del hidrógeno hace que la glicina sea el aminoácido más pequeño.,
AlanineAlaA
la alanina es un aminoácido simple que tiene solo un grupo metilo O CH3 como su cadena lateral. Como no ves nada más que carbono e hidrógeno, la alanina es un aminoácido hidrofóbico no polar. Es importante reconocer que este es un aminoácido muy pequeño y capaz de ser «encajado» en bucles o cadenas apretadas.
ValineValV
la valina es otro aminoácido simple con solo un grupo variable isopropilo. Al igual que la alanina, no vemos nada más que carbono e hidrógeno, haciendo de la valina un aminoácido hidrofóbico no polar.,
LeucineLeuL
puede reconocer que la leucina tiene el mismo grupo variable que la valina, pero con un grupo adicional de CH2. O simplemente puede reconocer su cadena lateral isobutilo.
vea este video si no está familiarizado con las cadenas laterales ramificadas como isopropilo o sec-butilo. Dado que la leucina solo tiene Cs y Hs, es un aminoácido no polar que teme al agua.
IsoleucineIleI
isoleucina, como su nombre lo indica, es un isómero de leucina. La diferencia es la colocación del CH3 para una cadena lateral sec-butilo en lugar de una isobutilo. Al igual que su isómero, la isoleucina es no polar e hidrofóbica.,
Metioninemetm
la metionina es el primer aminoácido potencialmente complicado. Su cadena lateral contiene principalmente Cs y Hs pero con un átomo de azufre incrustado. Si bien puede pensar que es hidrofílico, preste atención cuidadosa a la ubicación del átomo de azufre. Incrustado en la cadena y unido solo a los átomos de carbono, el azufre está parcialmente ‘oculto’ del entorno exterior.
si bien no es necesario conocer los valores de electronegatividad para el MCAT, ayuda a entender que S = 2.58 y C = 2.55. Dado que la diferencia en electronegatividad es inferior a 0.5, no hay polaridad en esta cadena lateral.,también debe reconocer la metionina como el codón de inicio AUG en la traducción de ARN a proteínas.
Fenilalaninefef
para ayudarle a recordar que la fenilalanina es F recuerde que ‘ph’ se pronuncia como una ‘F’. No mezcles esto con P de prolina.prestar atención a la estructura de la fenilalanina. Tiene un solo grupo de carbono con un anillo de benceno Unido. Fenilo es el nombre de un sustituyente de benceno, y esta molécula tiene un benceno (fenilo) unido a la estructura de la alanina. Dado que la fenilalanina no tiene nada más que Cs y Hs en su cadena lateral aromática, es no polar e hidrofóbica.,
TryptophanTrpW
esto es complicado. Observe la N-H en esta cadena lateral. N-H debe ser polar y capaz de enlace de hidrógeno. Sin embargo, hay dos razones por las que este aminoácido sigue siendo no polar e hidrofóbico.
- El Grupo N-H es una pequeña porción de la cadena lateral muy grande.
- Mire cuidadosamente el nitrógeno y, lo que es más importante, sus pares solitarios. Los electrones del nitrógeno son integrales a la aromaticidad conjugada para la cadena lateral del triptófano., En otras palabras, piense en sus electrones como ‘demasiado distraídos’ por resonancia para prestar mucha atención al entorno externo del agua.
el MCAT requiere que reconozca que este es un aminoácido grande y voluminoso. Pero como es un examen de opción múltiple, simplemente puedes memorizar que el triptófano es el único aminoácido con dos anillos fusionados.
de hecho, es tan grande que puede tropezar (trp) sobre sí mismo y gritar Waaaaaa(W)
(nota sobre mnemotécnica: cuanto más divertida, extraña o sucia la mnemotécnica, más probable es que la recuerdes. Ten esto en cuenta para la escuela de Medicina.,)
ProlineProP
prolina es un aminoácido único ya que es el único que incorpora la columna vertebral en su cadena lateral. La cadena lateral proline es una cadena de 3 carbonos que gira y se une al grupo amino original. Esto significa que a diferencia de los otros aminoácidos, la prolina no tiene un átomo de hidrógeno en su nitrógeno cuando forma parte de una cadena polipeptídica.
sin embargo, no se puede olvidar que el nitrógeno no es realmente parte del grupo de variables, lo que significa que no puede aportar ninguna polaridad. Ya que solo tenemos 3 grupos CH2 para analizar obtenemos una cadena lateral hidrofóbica no polar., Este bucle padre crea un bulto y no permite que una cadena que contiene prolina sea lineal, lo que significa que a menudo la encontrará en bucles y al final de una hélice alfa.
aminoácidos hidrofóbicos polares
*Esta es una sección pegajosa, y dependiendo de dónde investigue, puede encontrar los siguientes clasificados como polares o no polares, hidrofílicos o hidrofóbicos. Preste atención a la presencia de grupos polares que son pequeños en comparación con la cadena lateral general, o muy débilmente polares y, por lo tanto, hidrofóbicos.,
CysteineCysC
la cisteína tiene un S-H ligeramente polar, pero su polaridad es tan suave que la cisteína no puede interactuar adecuadamente con el agua, lo que la hace hidrofóbica.
la cisteína es un aminoácido muy importante cuando se trata de estructura terciaria y cuaternaria. La mayoría de las interacciones de cadena lateral incluyen interacciones polares / cargadas o dispersión no polar de Van Der Waals y London. Sin embargo, la cadena lateral de cisteína es capaz de formar un puente disulfuro, que es un enlace covalente entre 2 átomos de azufre a través de la oxidación de la cadena lateral y la eliminación de 2 átomos de hidrógeno., Este enlace covalente es mucho más fuerte y más permanente en comparación con las interacciones terciarias y cuaternarias estándar.
Esta es también la causa del error experimental en la determinación del tamaño/longitud de la proteína para proteínas con múltiples subunidades.
TyrosineTyrY
algunos estudiantes ven esto como una fuga de OH de un neumático (tyr).
eche un vistazo de cerca a la tirosina. ¿Qué ves? Se parece a la fenilalanina aromática con un grupo OH en la posición para (Orto/meta/para 2do video).,
por un lado, tenemos un grupo OH muy polar y con capacidad de enlace de hidrógeno, pero por otro lado, el OH es pequeño en comparación con el tamaño del grupo bencílico (CH2-fenilo). Este enigma es una fuente común de confusión, pero si entiendes esto, reconocerás que la tirosina, aunque polar, sigue siendo un aminoácido hidrofóbico.
aminoácidos hidrofílicos polares
hidrofílicos como su nombre lo indica proviene del agua hidráulica y amante de la filología.la polaridad proviene de una diferencia de 0.5-1.9 en electronegatividad entre átomos unidos., Mientras que usted no tiene que conocer estos valores para el MCAT, usted debe reconocer que los enlaces polares existirán cuando N y O están unidos a átomos no carbónicos.la diferencia de electronegatividad es suficiente para crear una ligera separación de carga o polaridad. Y dado que lo similar atrae a lo similar, estos grupos parcialmente cargados serán atraídos a grupos con carga opuesta o parcialmente cargada, como el agua. Estos grupos torcerán la cadena de polipéptidos para interactuar entre sí y con el agua.los grupos hidrofóbicos se retuercen de estas cadenas laterales.,
SerineSerS
piense en la serina como alanina con un grupo OH Unido. A diferencia de la tirosina, el OH es la mayoría en esta molécula y su polaridad es suficiente para influir en todo el grupo. Esto hace que las series sean polares y muy hidrofílicas.
ThreonineThrT
hay varias maneras de ver este grupo. Se puede pensar en ella como serina con un grupo metilo extra, o como valina pero con un OH reemplazando uno de los grupos metilo. Recuerdo que THREEonine tenía 3 grupos diferentes: CH, CH3 y OH.al igual que la serina, este grupo variable es polar e hidrofílico.,
AsparagineAsnN
Pruebe esto: Ligadura de su discurso como ustedes dicen, «asparagina’ muy rápido. Suena como si estuvieras diciendo como N N, que es como recuerdo la abreviatura de 3 letras para este aminoácido. El NH2 al final de esta molécula te hace pensar ‘base’, pero mira su vecino. NH2 cerca de un carbonilo forma una amida, que no le gusta actuar como un ácido o base en condiciones fisiológicas estándar. Sin embargo, con cargas parciales y capacidad de unión H tanto en el oxígeno carbonilo como en los grupos NH2, obtenemos un aminoácido hidrofílico polar.,
GlutamineGlnQ
pienso en ambos aminoácidos’ glut ‘como glotones que han ‘consumido’ un grupo extra de CH2. La glutamina tiene la misma estructura que la asparagina pero con un CH2 extra glotón en su cadena. Al igual que la asparagina, es polar e hidrofílica.
cadenas laterales de aminoácidos ácidos y Básicos
la acidez y la basicidad en los aminoácidos es otra fuente de confusión entre los estudiantes. Si comienza como un ácido, ¿se convierte en una base? ¿Cómo encuentro el cargo? Y así sucesivamente.
Este es el truco: un ácido carboxílico en la cadena lateral te dará un aminoácido ácido., Cuando se desprotona un grupo carboxilo, se obtiene una sal base conjugada. Así que si ves la versión salina de una cadena lateral de ácido carboxílico, mientras que técnicamente es una «base conjugada», simplemente nos referiremos a ella como la versión salina del aminoácido ácido. Mismo para la base. Busque átomos de nitrógeno ‘no distraídos’ en la cadena lateral.
aminoácidos ácidos
los aminoácidos ácidos deben parecer muy familiares en comparación con la asparagina y la glutamina. Y eso es porque todo acerca de ellos es el mismo excepto para el grupo funcional terminal., Las amidas (discutidas anteriormente) son polares, pero si el NH2 se intercambia por un grupo OH, se obtiene un grupo carboxilo ácido.
ácido aspártico / AspartateAspD
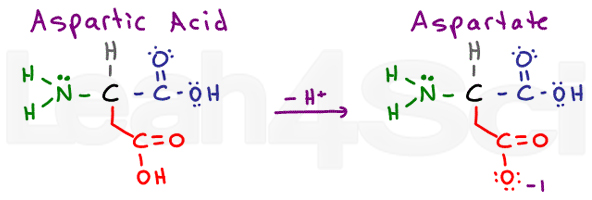
El ácido aspártico se refiere a la forma ácida protonada del aminoácido. Cuando se desprotona, a menudo verá la sal base conjugada conocida como aspartato. Esta es la nomenclatura estándar para los ácidos carboxílicos.
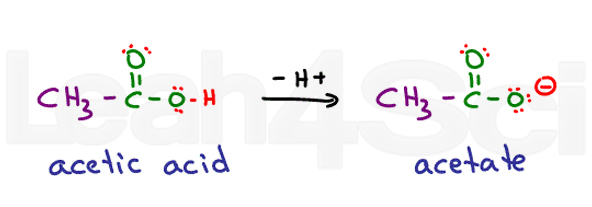
piense en el ácido etanoico. Su nombre común es ácido acético. Cuando se desprotona se obtiene acetato., Los ácidos son muy estables en agua ya que están parcialmente cargados en su forma protonada y completamente cargados en su forma desprotonada. Esto los hace altamente hidrofílicos.
ácido glutámico / GlutamateGluE
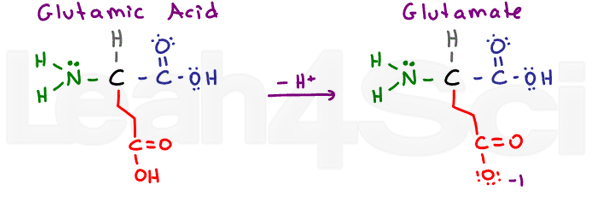
Una vez más tenemos un aminoácido ‘glotón’ con un grupo CH2 extra. El ácido glutámico se refiere a la forma ácida protonada, y el glutamato se refiere a la forma de base/sal conjugada desprotonada.al igual que el ácido aspártico, el ácido glutámico es muy estable en agua y por lo tanto hidrófilo.,
aminoácidos básicos
los aminoácidos básicos contienen un átomo de nitrógeno con un par de electrones solitario capaz de atacar a un átomo de hidrógeno. Cuando un aminoácido básico se somete a un pH bajo (ácido), agarrará uno de los protones libres en solución para formar una sal ácida conjugada. Estos son fácilmente reconocidos por el nitrógeno positivo en la cadena lateral. A diferencia de los aminoácidos ácidos, no hay ‘nombres comúnmente utilizados’ para memorizar estas sales conjugadas.
LysineLysK
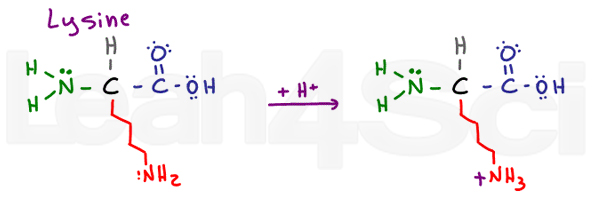
la Lisina es un simple aminoácido básico., A pesar de una cadena larga y potencialmente hidrofóbica, tiene un NH2 básico al final. En su forma básica desprotonada, la lisina es neutra e hidrófila; sin embargo, si se encuentra en pH fisiológico, la lisina recogerá un H+ de la solución para formar una sal NH3+. Las sales están cargadas y, por lo tanto, definitivamente hidrofílicas
ArginineArgR
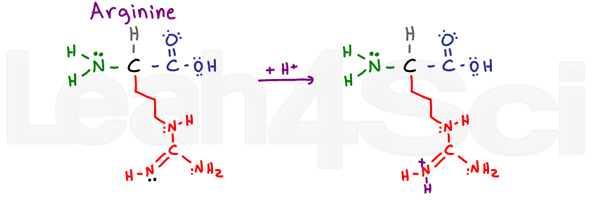
La arginina es confusa y me hace decir ARGh O R para abreviar. ¿Por qué? La porción básica de este grupo de variables consiste en un NH, C=n-H y NH2.,
los 2 átomos de nitrógeno de enlace simple pueden usar sus pares solitarios para resonar con el carbono y el átomo de nitrógeno de enlace doble. Esto hace que sus electrones no estén disponibles para actuar como base. Sin embargo, el nitrógeno de doble enlace utiliza su enlace pi para resonar, dejando su par solitario libre (mostrado en negro) para actuar como el nitrógeno básico en este grupo.Argh!
HistidineHisH

la histidina es otra base complicada por la misma razón que la arginina. ¿Qué nitrógeno es el básico? Mira el dibujo aquí, particularmente en los pares solitarios en los 2 átomos de nitrógeno., El anillo de histidina es un compuesto aromático heterocíclico. El átomo de nitrógeno superior no tiene un enlace pi. Esto significa que debe usar sus pares solitarios para participar en la resonancia.
El átomo de nitrógeno inferior ya tiene un enlace pi resonante. Esto deja a sus electrones solitarios (mostrados en negro) libres para agarrar un protón, haciendo de este el átomo básico.
En conclusión
Los aminoácidos son un componente crítico para las estructuras biológicas y para su comprensión de la biología y la bioquímica en el MCAT., Y así, al intentar memorizar todo sobre estos 20 aminoácidos, es importante que también entiendan por qué tienen aminoácidos polares y no polares, qué hace que el grupo variable sea hidrofóbico o hidrofílico, y por supuesto, la lógica detrás de los aminoácidos ácidos y básicos protonados/desprotonados.