 aminoacizii sunt blocurile de construcție ale lucrurilor vii. Lanțurile lungi de aminoacizi alcătuiesc proteine, care la rândul lor alcătuiesc multe componente celulare structurale și funcționale.îmi place să mă gândesc la celulă ca la un oraș autonom în care nucleul este capitala, mitocondriile sunt centrala electrică și așa mai departe. Dar apoi avem muncitorii, sistemul de transport și însăși structura orașului celular, care sunt toate făcute din proteine-care la rândul lor sunt făcute din aminoacizi.,complexitatea unei structuri proteice este determinată de secvența sa de aminoacizi și de natura chimică a lanțurilor laterale ale grupului lor variabil. MCAT necesită înțelegerea naturii lanțurilor laterale polare și nepolare și răsucirea și conformațiile cauzate de interacțiunile hidrofobe și hidrofile
aminoacizii sunt blocurile de construcție ale lucrurilor vii. Lanțurile lungi de aminoacizi alcătuiesc proteine, care la rândul lor alcătuiesc multe componente celulare structurale și funcționale.îmi place să mă gândesc la celulă ca la un oraș autonom în care nucleul este capitala, mitocondriile sunt centrala electrică și așa mai departe. Dar apoi avem muncitorii, sistemul de transport și însăși structura orașului celular, care sunt toate făcute din proteine-care la rândul lor sunt făcute din aminoacizi.,complexitatea unei structuri proteice este determinată de secvența sa de aminoacizi și de natura chimică a lanțurilor laterale ale grupului lor variabil. MCAT necesită înțelegerea naturii lanțurilor laterale polare și nepolare și răsucirea și conformațiile cauzate de interacțiunile hidrofobe și hidrofile
și da, ar trebui să memorați fiecare aminoacid pentru MCAT. Aceasta include lanțul lateral, numele complet, numele de 3 litere și abrevierea cu o singură literă. Dar nu lipi pur și simplu cuvintele și structurile pe cartonașe în speranța de a forța în memorie., Trebuie să abordați în mod activ fiecare aminoacid individual.
Pentru o listă de referință rapidă descarcă gratuit mea de Aminoacizi Foaie de Ieftin Ghid de Studiu
- Scrie numele complet
- Trage de aminoacizi și structura variabilă de grup
- Scrie 3 litere și singură literă abrevieri
- Verbaliza ceva unic despre acest specific lanțului lateral – cu voce tare! Cu cât conexiunea este mai amuzantă și mai nebună, cu atât mai ușor vă veți aminti.,
- se Repetă denumirea/desen proces o dată IMEDIAT
- Repeta săptămânal, până când vă simțiți SOLID cu aceste informații
Structura de Bază a unui Amino-Acid
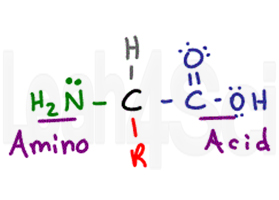 aminoacizi devine numele său de la două mari grupe funcționale. Aminoacidul are un carbon chiral central numit carbonul alfa (negru). Atașat la carbonul central aveți un atom de hidrogen (Gri), o grupare amino sau NH2 (verde) și o grupare COOH de acid carboxilic (violet). În cele din urmă avem grupul R (roșu), care este un lanț lateral variabil.,există 20 de aminoacizi diferiți care se disting prin lanțurile lor laterale unice. Acestea variază de la un atom de hidrogen simplu (glicină) la un sistem aromatic complex de rezonanță cu 2 inele (triptofan).în timp ce versiunea complet neutră de mai sus este modul în care majoritatea studenților studiază aminoacizii și forma pe care o vom folosi în acest articol, rețineți că acest lucru este incorect din punct de vedere tehnic.deoarece gruparea carboxil este acidă și gruparea amino bazică, cele două vor exista ca zwitterion în formele lor încărcate conjugate în pH fiziologic., Mai multe despre zwitterion și taxele de aminoacizi în următorul meu articol (link-ul de urmat).un concept final înainte de a descompune aminoacizii individuali și aceasta este structura proteică 3-dimensională. Într-o structură biologică a sistemului determină funcția, astfel încât înțelegerea caracteristicilor aminoacizilor este esențială pentru înțelegerea structurii și, în cele din urmă, a funcției proteinelor.structura primară a unei proteine 3-D
aminoacizi devine numele său de la două mari grupe funcționale. Aminoacidul are un carbon chiral central numit carbonul alfa (negru). Atașat la carbonul central aveți un atom de hidrogen (Gri), o grupare amino sau NH2 (verde) și o grupare COOH de acid carboxilic (violet). În cele din urmă avem grupul R (roșu), care este un lanț lateral variabil.,există 20 de aminoacizi diferiți care se disting prin lanțurile lor laterale unice. Acestea variază de la un atom de hidrogen simplu (glicină) la un sistem aromatic complex de rezonanță cu 2 inele (triptofan).în timp ce versiunea complet neutră de mai sus este modul în care majoritatea studenților studiază aminoacizii și forma pe care o vom folosi în acest articol, rețineți că acest lucru este incorect din punct de vedere tehnic.deoarece gruparea carboxil este acidă și gruparea amino bazică, cele două vor exista ca zwitterion în formele lor încărcate conjugate în pH fiziologic., Mai multe despre zwitterion și taxele de aminoacizi în următorul meu articol (link-ul de urmat).un concept final înainte de a descompune aminoacizii individuali și aceasta este structura proteică 3-dimensională. Într-o structură biologică a sistemului determină funcția, astfel încât înțelegerea caracteristicilor aminoacizilor este esențială pentru înțelegerea structurii și, în cele din urmă, a funcției proteinelor.structura primară a unei proteine 3-D
primul și mai important factor de determinare a structurii proteinei este secvența aminoacizilor., Dacă lanțul polipeptidic este atașat într-o ordine diferită, obțineți o structură generală foarte diferită.
structura secundară a unei proteine 3-D
structura secundară provine din interacțiunile de legare a hidrogenului din coloana vertebrală. Legătura peptidică transformă fiecare grupare carboxil și amino într-o grupare funcțională amidă. Structura secundară a helixului alfa și a foilor plisate beta provine din legarea hidrogenului între oxigenul parțial negativ de pe carbonil și hidrogenul parțial pozitiv de pe azot.,
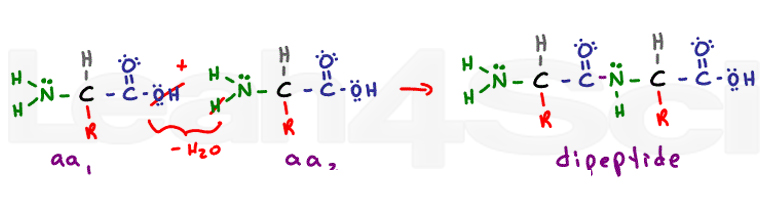
structura terțiară a unei proteine 3-D
structura terțiară este locul în care este introdusă plierea tridimensională reală și aceasta este prima dată când veți observa Interacțiuni cu lanț lateral. Acest lucru este în cazul în care cunoașterea și înțelegerea lanțurilor laterale de aminoacizi sunt critice.
permiteți-mi să repet, structura terțiară este prima dată când veți vedea interacțiuni variabile ale lanțului lateral al grupului R pe lanțul polipeptidic. Mulți studenți confundă acest lucru cu structura secundară, care este doar interacțiunile coloanei vertebrale.,structura cuaternară a unei proteine Multi-polipeptidice 3-D structura cuaternară se referă la interacțiunile de grup variabil între diferite polipeptide pentru a forma o singură proteină mai mare.structurile cuaternare nu se găsesc în fiecare proteină. Dacă proteina conține doar o singură bandă de aminoacizi, atunci cel mai înalt nivel de pliere este structura sa terțiară. Cu toate acestea, dacă proteina este alcătuită din mai multe subunități polipeptidice, atunci structura cuaternară este cea care ține diferitele polipeptide împreună.,acum, că înțelegeți semnificația caracteristicilor lanțului lateral, să ne scufundăm în aminoacizi. Rețineți că, deoarece grupările amino și carboxil părinte sunt „ocupate” cu structura primară/secundară, ele nu sunt analizate atunci când studiază proprietățile și caracteristicile lanțului lateral.
aceasta înseamnă că ignorați orice polaritate potențială atât pe grupurile carboxil, cât și pe cele amino și priviți doar lanțurile laterale.
aminoacizi hidrofobi nepolari
hidrofobi, așa cum sugerează și numele, este hidro – apă, frică de fobie., Aminoacizii hidrofobi au polaritate mică sau deloc în lanțurile lor laterale. Lipsa polarității înseamnă că nu au cum să interacționeze cu moleculele de apă foarte polare, făcându-le să se teamă de apă.există doar cinci atomi care vor apărea în grupurile variabile de aminoacizi: H, C, N, O și S.
luați în considerare polaritatea numai atunci când aveți N, O, S ca factor „majoritar”. Le voi arăta pe măsură ce apar. Cu toate acestea, dacă tot ce vedeți sunt Cs și Hs, ar trebui să recunoașteți automat un aminoacid temător de apă.,
GlycineGlyG
Glicina este un aminoacid unic prin faptul că nu are într-adevăr un grup R. Când vă gândiți la „grupa R variabilă”, ar trebui să vă gândiți la carbonul atașat la alți atomi. Dar glicina are doar un hidrogen în poziția sa de lanț lateral. Deoarece glicina are 2 atomi de hidrogen, câte unul pe lanțul părinte și lateral, este singurul aminoacid simetric și astfel achiral. Deoarece hidrogenul este nepolar, glicina este un aminoacid hidrofob. Lanțul lateral de hidrogen face ca glicina să fie cel mai mic aminoacid.,alanina este un aminoacid simplu care are doar o grupare metil sau CH3 ca lanț lateral. Deoarece nu vedeți altceva decât carbon și hidrogen, alanina este un aminoacid hidrofob nepolar. Este important să recunoaștem că acesta este un aminoacid foarte mic și capabil să fie „înțepenit” în bucle sau lanțuri strânse.
ValineValV
valina este un alt aminoacid simplu cu doar o grupare variabilă izopropil. La fel ca alanina, nu vedem altceva decât carbon și hidrogen, făcând valina un aminoacid hidrofob nepolar.,puteți recunoaște leucina ca având aceeași grupă variabilă ca valina, dar cu o grupă CH2 suplimentară. Sau puteți recunoaște pur și simplu lanțul său lateral izobutil.
vedeți acest videoclip dacă nu sunteți familiarizat cu lanțurile laterale ramificate, cum ar fi izopropilul sau sec-butilul. Deoarece leucina are doar Cs și Hs, este un aminoacid nepolar care se teme de apă.
Izoleucineilei
izoleucina, după cum sugerează și numele, este un izomer al leucinei. Diferența este plasarea CH3 pentru un lanț lateral sec-butil, mai degrabă decât un lanț lateral izobutil. La fel ca izomerul său, izoleucina este nepolară și hidrofobă.,
MethionineMetM
metionina este primul aminoacid potențial complicat. Lanțul lateral conține în mare parte Cs și Hs, dar cu un atom de sulf încorporat. În timp ce ați putea crede că este hidrofil, acordați o atenție deosebită locației atomului de sulf. Încorporat în lanț și atașat doar la atomi de carbon, sulful este parțial „ascuns” de mediul exterior.
deși nu trebuie să cunoașteți valorile electronegativității pentru MCAT, vă ajută să înțelegeți că S = 2.58 și C = 2.55. Deoarece diferența de electronegativitate este mai mică de 0,5, nu există polaritate pe această partelanț.,
De asemenea, trebuie să recunoașteți metionina ca codon de pornire AUG în traducerea ARN la proteine.pentru a vă ajuta să vă amintiți că fenilalanina este F amintiți-vă că ” ph „este pronunțat ca „F”. Nu amesteca asta cu P pentru prolină.
acordați atenție structurii fenilalaninei. Are un singur grup de carbon cu un inel benzenic atașat. Fenilul este numele unui substituent de benzen, iar această moleculă are un benzen (fenil) atașat la structura alaninei. Deoarece fenilalanina nu are altceva decât Cs și Hs în lanțul său lateral aromatic, este nepolară și hidrofobă.,
Triptofantrpw
acesta este unul complicat. Observați N-H în acest lanț lateral. N-H ar trebui să fie polar și capabil să lege hidrogenul. Cu toate acestea, există două motive pentru care acest aminoacid este încă nepolar și hidrofob.
- grupul N-H este o porțiune mică a lanțului lateral foarte mare.
- Uită-te cu atenție la azot și, mai important, la perechile sale singure. Electronii azotului sunt integrați în aromaticitatea conjugată pentru lanțul lateral triptofan., Cu alte cuvinte, gândiți-vă la electronii săi ca fiind „prea distrași” de rezonanță pentru a acorda multă atenție mediului exterior al apei.MCAT vă cere să recunoașteți că acesta este un aminoacid mare și voluminos. Dar din moment ce este un examen cu alegere multiplă, puteți memora pur și simplu că triptofanul este singurul aminoacid cu două inele topite.
de fapt, e atât de mare, încât pot EXCURSIE (trp) pe sine și striga Waaaaaa (W)
(Nota pe mnemonice: amuzant, ciudat, sau mai murdar mnemonic, cu atât mai probabil vă va aminti. Ține minte asta pentru med-school.,Prolina este un aminoacid unic, deoarece este singurul care încorporează coloana vertebrală în lanțul său lateral. Lanțul lateral proline este un lanț 3-carbon care se învârte și se atașează înapoi la grupul amino părinte. Aceasta înseamnă că, spre deosebire de ceilalți aminoacizi, prolina nu are un atom de hidrogen pe azotul său atunci când face parte dintr-un lanț polipeptidic.cu toate acestea, nu puteți uita că azotul nu face parte cu adevărat din grupul de variabile, ceea ce înseamnă că nu poate contribui la nicio polaritate. Din moment ce avem doar 3 grupuri CH2 de analizat, obținem un lanț lateral hidrofob nepolar., Această buclă părinte creează o umflătură și nu permite ca un lanț care conține prolină să fie liniar, ceea ce înseamnă că îl veți găsi adesea în bucle și la sfârșitul unei helix alfa.
Polar Hidrofobe Aminoacizi
*Acest lucru este un lipicios secțiune, și în funcție de locul de cercetare puteți găsi următoarele clasificate ca polare sau nepolare, hidrofil sau hidrofob. Acordați atenție prezenței grupurilor polare care sunt mici în comparație cu partea generală sau foarte slab polar și, prin urmare, hidrofob.,Cisteina are un S – H ușor polar, dar polaritatea sa este atât de ușoară încât cisteina nu este capabilă să interacționeze corect cu apa, ceea ce o face hidrofobă.cisteina este un aminoacid foarte important atunci când vine vorba de structura terțiară și cuaternară. Cele mai multe interacțiuni cu lanț lateral includ interacțiuni polare/încărcate sau dispersie nepolară Van Der Waals și Londra. Cu toate acestea, lanțul lateral al cisteinei este capabil să formeze o punte disulfidică, care este o legătură covalentă între 2 atomi de sulf prin oxidarea lanțului lateral și îndepărtarea a 2 atomi de hidrogen., Această legătură covalentă este mult mai puternică și mai permanentă în comparație cu interacțiunile terțiare și cuaternare standard.
aceasta este, de asemenea, cauza erorii experimentale în determinarea mărimii/lungimii proteinei pentru proteinele cu mai multe subunități.unii studenți văd acest lucru ca Oh scurgeri dintr-o anvelopă (tyr).aruncați o privire atentă la tirozină. Ce vezi? Se pare că fenilalanina aromatică cu o grupare OH la poziția para (ortho/meta/para 2nd video).,pe de o parte, avem o grupare OH foarte polară și capabilă de legături de hidrogen, dar pe de altă parte, OH este mic în comparație cu dimensiunea grupării benzil (CH2-fenil). Această enigmă este o sursă comună de confuzie, dar dacă înțelegeți acest lucru, veți recunoaște că tirozina, în timp ce polar, este încă un aminoacid hidrofob.
Polar hidrofil aminoacizi
hidrofil după cum sugerează și numele vine de la hidro-apă și filic – iubitoare.
polaritatea provine dintr-o diferență de 0,5-1,9 în electronegativitate între atomii legați., În timp ce nu trebuie să cunoașteți aceste valori pentru MCAT, ar trebui să recunoașteți că legăturile polare vor exista atunci când N și O sunt legate de atomi non-carbon.
diferența de electronegativitate este suficientă pentru a crea o ușoară separare a sarcinii sau a polarității. Și din moment ce atrage ca, aceste grupuri parțial încărcate vor fi atrase de grupuri încărcate opus sau parțial încărcate, cum ar fi apa. Aceste grupuri vor răsuci lanțul polipeptidic pentru a interacționa între ele și cu apa.
grupurile hidrofobe se vor răsuci departe de aceste lanțuri laterale.,Serineseri
gândiți-vă la serină ca alanină cu un grup OH atașat. Spre deosebire de tirozină, OH este majoritatea în această moleculă și polaritatea sa este suficientă pentru a influența întregul grup. Acest lucru face ca Seria să fie polară și foarte hidrofilă.
Treoninethrt
există mai multe moduri de a privi acest grup. Vă puteți gândi la ea ca serină cu o grupare metil suplimentar, sau ca valină, dar cu un OH înlocuind una dintre grupările metil. Îmi amintesc că THREEonine are 3 grupuri diferite: CH, CH3 și OH.
ca și Serina, această grupă variabilă este polară și hidrofilă.,AsparagineAsnN
încercați acest lucru: Slur discursul așa cum spui „asparagină” foarte repede. Se pare că spui ca … N, care este modul în care îmi amintesc abrevierea de 3 litere pentru acest aminoacid. NH2 de la sfârșitul acestei molecule te face să gândești „bază”, dar uită-te la vecinul ei. NH2 lângă un carbonil formează o amidă, care nu-i place să acționeze ca un acid sau o bază în condiții fiziologice standard. Cu toate acestea, cu sarcini parțiale și capacitatea de legare a H atât la oxigenul carbonil, cât și la grupările NH2, obținem un aminoacid hidrofil polar.,
GlutamineGlnQ
mă gândesc la ambii aminoacizi „glut” ca gluttoni care au „consumat” o grupă CH2 suplimentară. Glutamina are aceeași structură ca asparagina, dar cu un CH2 suplimentar glutton în lanțul său. La fel ca asparagina, este polar și hidrofil.
lanțurile laterale acide și bazice de aminoacizi
aciditatea și bazicitatea în aminoacizi este încă o altă sursă de confuzie în rândul studenților. Dacă începe ca un acid, devine o bază? Cum pot găsi taxa? Și așa mai departe.iată trucul: un ACID carboxilic din lanțul lateral vă va oferi un aminoacid acid., Când o grupare carboxil este deprotonată, obțineți o sare de bază conjugată. Deci, dacă vedeți versiunea de sare a unui lanț lateral de acid carboxilic, în timp ce este tehnic o „bază conjugată”, ne vom referi pur și simplu la ea ca versiunea de sare a aminoacidului acid. La fel și pentru bază. Ferește-te pentru atomi de azot „non-distras” în lanțul lateral.
aminoacizi acizi
aminoacizii acizi ar trebui să arate foarte familiari în comparație cu asparagina și glutamina. Și asta pentru că totul despre ele este același, cu excepția grupului funcțional terminal., Amidele (discutate mai sus) sunt polare, dar dacă NH2 este schimbat pentru o grupare OH, obțineți o grupare carboxil acidă.
Acid Aspartic / AspartateAspD
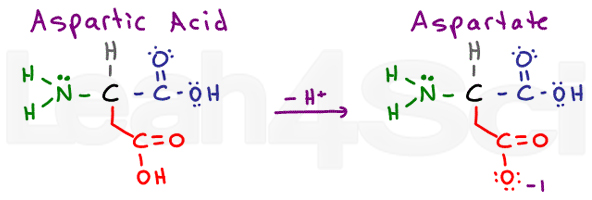
acid Aspartic se referă la protonate acide formă de aminoacizi. Când este deprotonat, veți vedea adesea sarea de bază conjugată denumită aspartat. Aceasta este nomenclatura standard pentru acizii carboxilici.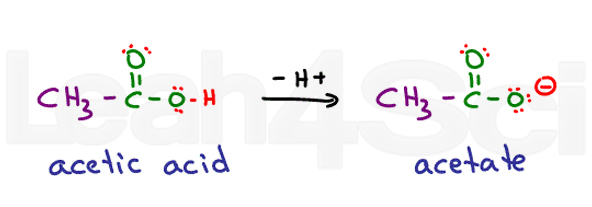
gândiți-vă la acidul etanoic. Numele său comun este acidul acetic. Când deprotonați obțineți acetat., Acizii sunt foarte stabili în apă, deoarece sunt încărcați parțial în forma lor protonată și încărcați complet în forma lor deprotonată. Acest lucru le face foarte hidrofile.
Acid Glutamic / GlutamateGluE
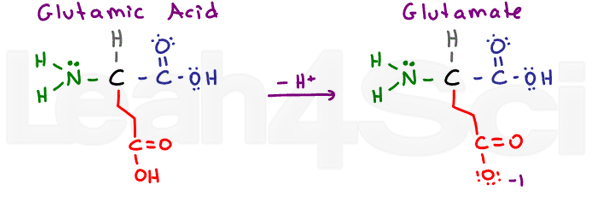
din nou avem o ‘lacom’ de aminoacizi, cu un plus CH2 grup. Acidul Glutamic se referă la forma acidă protonată, iar glutamatul se referă la forma de bază/sare conjugată deprotonată.
ca și acidul aspartic, acidul glutamic este foarte stabil în apă și astfel hidrofil.,aminoacizii bazici conțin un atom de azot cu o pereche de electroni singuri capabili să atace un atom de hidrogen. Când un aminoacid bazic este supus unui pH scăzut (acid), acesta va apuca unul dintre protonii liberi în soluție pentru a forma o sare acidă conjugată. Acestea sunt ușor de recunoscut de azotul pozitiv în lanțul lateral. Spre deosebire de aminoacizii acizi, nu există „nume utilizate în mod obișnuit” pentru a memora aceste săruri conjugate.LysineLysK
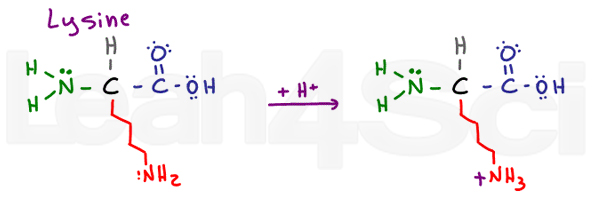
Lizina este o simplă bază de aminoacizi., În ciuda unui lanț lung și potențial hidrofob, are un NH2 de bază la sfârșit. În forma sa deprotonată de bază, lizina este neutră și hidrofilă; cu toate acestea, dacă se găsește în pH fiziologic, lizina va ridica un H+ din soluție pentru a forma o sare NH3+. Sărurile sunt încărcate și, prin urmare, cu siguranta hidrofileArginineArgR
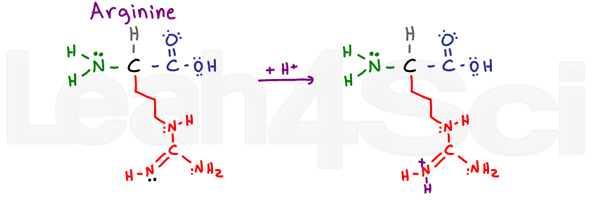
Arginina este confuz și mă face să spun ARGh sau R pentru scurt. De ce? Porțiunea de bază a acestui grup variabil constă dintr-un NH, C=N-H și NH2.,
cei 2 atomi de azot cu o singură legătură își pot folosi perechile singure pentru a rezona cu atomul de azot legat de carbon și dublu. Acest lucru face ca electronii lor să nu fie disponibili pentru a acționa ca bază. Cu toate acestea, azotul dublu legat își folosește legătura pi pentru a rezona, lăsând perechea liberă (prezentată în negru) să acționeze ca azot de bază în acest grup.
Aaah!HistidineHisH

histidina este o altă bază complicată din același motiv ca arginina. Care azot este cel de bază? Uită-te la desen aici, în special la perechile singuratice de pe atomii de azot 2., Inelul de histidină este un compus aromatic heterociclic. Atomul de azot superior nu are o legătură pi. Aceasta înseamnă că trebuie să-și folosească perechile singure pentru a participa la rezonanță.
atomul de azot inferior are deja o legătură pi rezonantă. Acest lucru lasă electronii săi singuri (arătați în negru) liberi să apuce un proton, făcând din acesta atomul de bază.în concluzie, aminoacizii sunt o componentă critică a structurilor biologice și pentru a înțelege Biologia și biochimia pe MCAT., Așa că, în timp ce încerci să memorezi totul despre acești 20 de aminoacizi, este important să înțelegi și de ce ai aminoacizi polari și nepolari, ce face grupul variabil hidrofob sau hidrofil, și desigur, logica din spatele aminoacizilor acizi și bazici protonați/deprotonați.