 aminosyrer er byggesteinene av levende ting. Lange kjeder av aminosyrer som utgjør proteiner, som i sin tur gjør opp mange strukturelle og funksjonelle cellekomponenter.
aminosyrer er byggesteinene av levende ting. Lange kjeder av aminosyrer som utgjør proteiner, som i sin tur gjør opp mange strukturelle og funksjonelle cellekomponenter.
jeg liker å tenke på cellen som en selvstendig by hvor kjernen er hovedstaden, mitokondriene er kraftverket og så videre. Men da har du dine medarbeidere, transport system og struktur av cellen byen, som alle er laget av proteiner – som i sin tur er laget av aminosyrer.,
kompleksiteten av et protein struktur er bestemt av dets sekvens av aminosyrer og den kjemiske natur av deres variabel gruppe sidekjeder. MCAT krever forståelsen av polare og upolare side kjeder og kronglete og conformations forårsaket av hydrofobe og hydrofile vekselsvirkningene
Og ja, du bør være ved å lære utenat hver aminosyre for MCAT. Dette inkluderer siden kjeden, fullt navn, 3-brev navn og enkelt bokstav forkortelse. Men ikke bare stikke ord og strukturer på flashcards i håp om å tvinge det inn i din hukommelse., Du må aktivt takle hver aminosyre individuelt.
For en rask referanse liste laste ned gratis Aminosyre Jukse Ark Studie Guide
- Skriv ut fullt navn
- Tegne aminosyre struktur og variabel gruppe
- Skriv ut de 3-brev og enkelt bokstav forkortelser
- Verbalisere noe unikt med denne spesifikke siden kjeden – høyt! De mer morsomme og sprø tilkoblingen, jo lettere vil du huske det.,
- Gjenta navngiving/tegning prosessen en gang med en gang
- Gjenta ukentlig inntil du føler deg FAST med denne informasjonen
Den Grunnleggende Strukturen i en Aminosyre
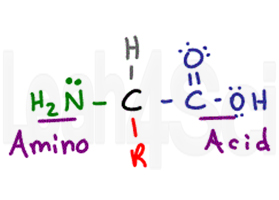 aminosyre får sitt navn fra sin to primære funksjonelle grupper. Aminosyren har en sentral chiral karbon kalles alfa carbon (sort). Knyttet til den sentrale karbon du har et hydrogenatom (grå), en aminosyre eller NH2-gruppe (grønn), og en karboksylsyre COOH-gruppe (lilla). Til slutt har vi den R-gruppen (red), som er en variabel side kjede.,
aminosyre får sitt navn fra sin to primære funksjonelle grupper. Aminosyren har en sentral chiral karbon kalles alfa carbon (sort). Knyttet til den sentrale karbon du har et hydrogenatom (grå), en aminosyre eller NH2-gruppe (grønn), og en karboksylsyre COOH-gruppe (lilla). Til slutt har vi den R-gruppen (red), som er en variabel side kjede.,
Det finnes 20 forskjellige aminosyrer preget av sin unike sidekjeder. De spenner fra en enkel hydrogenatom (glycine) til et komplekst 2-ring resonnere aromatiske system (tryptofan).
Mens det fullt nøytral versjon ovenfor er hvordan de fleste studenter som studerer aminosyrer, og den form vi vil bruke i denne artikkelen, husk at dette er teknisk feil.
Aminosyre i Zwitterion Form
Siden carboxyl gruppen er sure og amino gruppen grunnleggende, de to vil eksistere som et zwitterion i deres conjugated belastet former i fysiologisk pH., Mer på zwitterion og aminosyre kostnader i min neste artikkelen (link kommer senere).
En endelige konseptet før vi bryter ned den individuelle aminosyrer, og det er den 3-dimensjonale protein-strukturen. I et biologisk system, struktur bestemmer funksjonen, slik forståelse amino acid egenskaper er nøkkelen til å forstå strukturen og til slutt protein funksjon.
Primære Strukturen i en 3-D Protein
Den første og mer viktig bestemmelse faktor av protein-strukturen er sekvens av aminosyrer., Hvis polypeptid-kjeden er festet i en annen rekkefølge, kan du få en helt annen overordnet struktur.
Sekundær Struktur av en 3-D Protein
sekundær struktur kommer fra ryggraden hydrogenbinding interaksjoner. Peptid bond slår alle tidligere carboxyl og amino gruppen i en amide funksjonell gruppe. Sekundær struktur av alfa-helix-og beta-pleated ark kommer fra hydrogen binding mellom delvis negative oksygen på karbonyl og delvis positive hydrogen på nitrogen.,
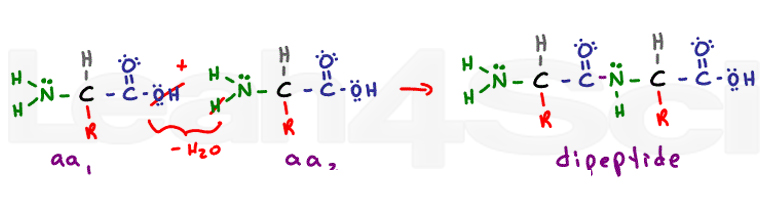
Tertiær Struktur av en 3-D Protein
tertiær struktur er der den ekte 3-dimensjonale folding er innført, og dette er første gang du vil legge merke til side-chain-interaksjoner. DETTE er hvor kunnskap og forståelse av aminosyren sidekjeder er kritiske.
La meg gjenta meg selv, tertiær struktur er første gang vil du se variabel R-gruppen siden kjeden vekselsvirkningene på polypeptid-kjeden. Mange studenter forveksle dette med sekundær struktur, som er bare ryggraden interaksjoner.,
Kvartær Strukturen i en 3-D Multi-Polypeptid Protein
Kvartær struktur refererer til variabelen gruppe interaksjoner mellom ulike polypeptides for å danne en enkelt større protein.
Kvartær strukturer er ikke funnet i alle protein. Hvis protein inneholder kun en enkelt aminosyre strand, vinner den med det høyeste nivå av folding er dens tertiær struktur. Imidlertid, hvis protein er bygd opp av flere polypeptid underenhetene, så kvartære strukturen er det som holder de forskjellige polypeptides sammen.,
Nå som du forstår betydningen av side-chain-egenskaper, la oss dykke inn i aminosyrer. Husk at siden foreldrene amino og carboxyl grupper er «opptatt» med primær/sekundær struktur, de er IKKE analysert når man studerer side-chain-egenskaper og karakteristika.
Dette betyr at du ignorere eventuelle polaritet på både carboxyl og amino grupper og BARE se på sidekjeder.
Ikke-Polar Hydrofobe Aminosyrer
Hydrofobe, som navnet tilsier, er hydro – vann, fobisk – fryktet., Hydrofobe aminosyrer har liten eller ingen prioritet i deres sidekjeder. Mangel på polaritet betyr at de har ingen måte å samhandle med svært polar vann molekyler, noe som gjør dem vann å frykte.
Det er bare fem atomer som vil vises i din aminosyre variabel grupper: H, C, N, O, og S.
Bare vurdere polaritet når du har N, O, S som ‘majoritets’ – faktor. Jeg vil peke ut disse når de oppstår. Imidlertid, hvis alt du ser er Cs og Hs bør du automatisk gjenkjenne en vann-i frykt aminosyre.,
GlycineGlyG
Glysin er en unik aminosyre i at det egentlig ikke har en R-gruppe. Når du tenker » variabel gruppe,’ du bør tenke på karbon knyttet til andre atomer. Men glysin bare har en hydrogen på sin side kjede posisjon. Siden glysin har 2 hydrogenatomer, ett på hver forelder og siden kjeden, det er bare symmetrisk og dermed achiral aminosyre. Siden hydrogen er ikke-polar, glysin er en hydrofobe aminosyrer. Hydrogen side-chain gjør glysin den minste aminosyre.,
AlanineAlaA
Alanin er en enkel aminosyre som har bare en methyl-eller CH3-gruppe som sin side kjede. Siden du ikke se annet enn karbon og hydrogen, Alanin er en non-polar hydrofobe aminosyrer. Det er viktig å erkjenne at dette er en veldig liten aminosyre og er i stand til å være ‘kilt’ på små løkker eller kjeder.
ValineValV
Valin er en annen enkel aminosyre med bare en isopropyl variabel gruppe. Akkurat som alanin, vi ser ingenting, men karbon og hydrogen, noe som gjør valin en non-polar hydrofobe aminosyrer.,
LeucineLeuL
Du kan gjenkjenne leucine som har samme variabel gruppe som valin, men med en ekstra CH2-gruppe. Eller du kan bare erkjenne sin isobutyl side kjede.
Se denne videoen hvis du ikke er kjent med forgrenede sidekjeder som isopropyl eller sec-butyl. Siden leucine har bare Cs og Hs, det er vann i frykt for ikke-polare aminosyrer.
IsoleucineIleI
Isoleucin, som navnet tilsier, er en isomeren av leucine. Forskjellen er plasseringen av CH3 for en sec-butyl snarere enn en isobutyl side kjede. Akkurat som sin isomeren, isoleucin er upolare og hydrofobe.,
MethionineMetM
Metionin er den første potensielt vanskelige aminosyre. Det er siden kjeden består hovedsakelig av Cs og Hs men med en innebygd svovel atom. Selv om du kanskje tror det er hydrofile, betale forsiktig oppmerksomhet til plasseringen av svovel-atom. Innebygd i kjeden og festet til bare karbon-atomer, svovel er delvis «skjult» fra det ytre miljøet.
Mens du ikke trenger å vite electronegativity verdier for MCAT det hjelper til å forstå at S = 2.58 og C = 2.55. Siden forskjellen i electronegativity er mindre enn 0,5, det er INGEN prioritet på dette sidechain.,
Du må også erkjenne metionin som start-codon AUG i RNA oversettelse til proteiner.
PhenylalaninePheF
for Å hjelpe deg å huske at Fenylalanin er F huske at » ph » blir uttalt som ‘F’. Ikke bland dette opp med P for proline.
ta hensyn til strukturen av fenylalanin. Det har et enkelt karbon gruppe med et vedlagt benzen ringen. Fenyl er navnet på et benzen substituent, og dette molekylet har en benzen (fenyl) som er knyttet til strukturen av alanin. Siden fenylalanin har ingenting, men Cs og Hs i sin aromatiske side kjede, det er upolare og hydrofobe.,
TryptophanTrpW
Dette er en vanskelig en. Legg merke til den N-H i denne side-kjeden. N-H bør være polar og i stand til hydrogen binding. Det er imidlertid to grunner til at denne aminosyren er fortsatt non-polar og hydrofobe.
- N-H-gruppen er en liten del av svært store side-kjeden.
- Se nøye på nitrogen, og enda viktigere, på sin ensomme par. Nitrogen er elektroner er integrert i den conjugated aromaticity for tryptofan side kjede., Med andre ord, tenk på sine elektroner som «altfor distrahert» av resonans til å betale mye oppmerksomhet til eksterne vann-miljø.
MCAT krever at du erkjenner at dette er en stor og klumpete aminosyre. Men siden det er en multiple choice eksamen kan du bare huske at tryptofan er BARE aminosyre med TO smeltet ringer.
faktisk det er så stort det kan TUREN (trp) over seg selv og rope ut Waaaaaa (W)
(vær Oppmerksom på mnemonics: Det morsommere, enda rarere, eller skitnere de mnemonic, jo mer sannsynlig at du vil huske det. Holde dette i bakhodet for med-skolen.,)
ProlineProP
Proline er en unik aminosyre, siden det er DEN ENESTE som har ryggrad til sin side kjede. Den proline siden kjeden er en 3-karbon kjede som løkker rundt og festes tilbake til den overordnede amino gruppen. Dette betyr at i motsetning til de andre aminosyrer, proline IKKE har et hydrogenatom på sin nitrogen når de er en del av et polypeptid-kjeden.
du kan Imidlertid ikke glem at nitrogen er IKKE EGENTLIG en del av variabel gruppe, noe som betyr at det ikke kan bidra med noe polaritet. Siden vi bare har 3 CH2-grupper for å analysere får vi en upolar hydrofobe side kjede., Denne forelder-loop skaper en kul og ikke tillate en proline-som inneholder kjede å være lineær, noe som betyr at du vil ofte finne det i looper, og på slutten av en alfa helix.
Polar Hydrofobe Aminosyrer
*Dette er en klebrige delen, og avhengig av hvor du forskning kan du finne følgende kategorisert som polar eller upolare, hydrofile eller hydrofobe. Ta hensyn til tilstedeværelse av polare grupper som er små i forhold til den samlede sidechain, eller svært svakt polar, og derfor er hydrofobe.,
CysteineCysC
Cystein har en litt polar S-H, men sin polaritet er så mild at cystein er i stand til å samhandle med vann slik at det hydrofobe.
Cystein er en svært viktig aminosyre når det kommer til tertiær og kvartær struktur. De fleste side-chain-vekselsvirkningene inkluderer polar/belastet vekselsvirkningene, eller ikke-polar Van Der Waals og London spredning. Imidlertid, cystein side-kjeden er i stand til å danne en disulfide bridge, som er en covalent båndene mellom 2 svovel atomer gjennom side kjede oksidasjon og fjerning av 2 hydrogenatomer., Dette covalent bond er mye sterkere og mer permanent sammenlignet med standard tertiær og kvartær interaksjoner.
Dette er også årsaken til eksperimentelle feil i fastsettelsen protein størrelse/lengde for proteiner med flere underenhetene.
TyrosineTyrY
Noen studenter ser dette som OH lekker fra et dekk (tyr).
Ta en nærmere titt på tyrosin. Hva ser du? Det ser ut som den aromatiske fenylalanin med en OH-gruppe i avsnitt posisjon (ortho/meta/para 2. video).,
På den ene siden har vi en veldig polar-og hydrogen-bond i stand OH-gruppe, men på den annen side, OH den er liten i forhold til størrelsen på benzyl-gruppen (CH2-phenyl). Denne conundrum er en vanlig kilde til forvirring, men hvis du forstår dette, vil du innse at tyrosin, mens polare, er fortsatt en hydrofobe aminosyrer.
Polar Hydrofile Aminosyrer
Hydrofile som navnet tilsier kommer fra hydro-vann og philic – kjærlig.
Polaritet kommer fra en 0.5-1.9 forskjell i electronegativity mellom atomer bundet., Mens du ikke trenger å vite disse verdiene for MCAT, bør du innse at polare bindinger vil eksistere når N og O er bundet til ikke-karbon-atomer.
electronegativity forskjellen er nok til å lage en liten separasjon av ladning eller polaritet. Og siden like tiltrekker like, disse delvis ladet grupper vil bli tiltrukket av motsatt ladet eller delvis ladet grupper, slik som vann. Disse gruppene vil vri polypeptid-kjeden for å samhandle med hverandre og med vann.
Hydrofobe grupper vil vri seg bort fra disse sidekjeder.,
SerineSerS
Tenk på serin som alanin med en OH-gruppen er festet. I motsetning til tyrosin, OH, er de fleste i dette molekylet og dets polaritet er nok til å påvirke hele konsernet. Dette gjør serien polar og svært hydrofil.
ThreonineThrT
Det er flere måter å se på denne gruppen. Du kan tenke på det som serin med en ekstra metyl-gruppen, eller som valin, men med en OH bytte ut en av metyl-grupper. Jeg husker THREEonine som å ha 3 forskjellige grupper: CH, CH3, og OH.
Som serin, denne variabelen gruppen er polar og hydrofile.,
AsparagineAsnN
Prøv dette: Diskreditere deres tale som du sier ‘asparagine’ virkelig rask. Det høres ut som du sier SÅ…N, som er slik jeg husker det 3-bokstaver som forkortelse for denne aminosyren. Den NH2 på slutten av dette molekylet gjør at du tror ‘base’, men se på det neste. NH2 i nærheten av en karbonyl danner en amide, som ikke liker å fungere som en syre eller base under standard fysiologiske forhold. Imidlertid, med delvis gebyrer og H-binding evne på både karbonyl oksygen OG NH2 grupper, får vi en polar hydrofile aminosyre.,
GlutamineGlnQ
jeg tror både ‘mange’ aminosyrer som gluttons å ha «konsumert» en ekstra CH2-gruppe. Glutamin har samme struktur som asparagine, men med en ekstra grådig CH2 i sin kjede. Akkurat som asparagine, det er polare og hydrofile.
Sure og basiske aminosyrer sidekjeder
Surhet og basicity i aminosyrer er enda en kilde til forvirring blant studentene. Hvis det som starter som en syre, vil det bli en base? Hvordan finner jeg kostnad? Og så videre.
Her er trikset: en karboksylsyre i siden kjeden vil gi deg en syrlig aminosyre., Når en carboxyl gruppen er deprotonated, får du en kobling base SALT. Så hvis du ser salt versjon av en karboksylsyre side kjede, mens det er TEKNISK sett en «kobling base,» vi skal bare referere til det som salt versjon av den sure aminosyre. Samme for basen. Se opp for «ikke-distrahert’ nitrogen atomer i siden kjeden.
Sure Aminosyrer
Den sure aminosyrer bør se veldig kjent i forhold til asparagine og glutamin. Og det er fordi alt om dem er de samme bortsett fra terminal funksjonell gruppe., Amides (omtalt ovenfor) er polar, men hvis NH2 er byttet ut med en OH-gruppe, kan du få en syrlig carboxyl gruppe.
asparaginsyre / AspartateAspD
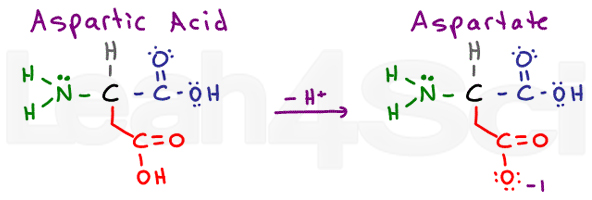
asparaginsyre refererer til protonated sure form av aminosyre. Når deprotonated, vil du ofte se konjugat base salt referert til som aspartat. Dette er standard nomenklatur for karboksylsyre syrer.
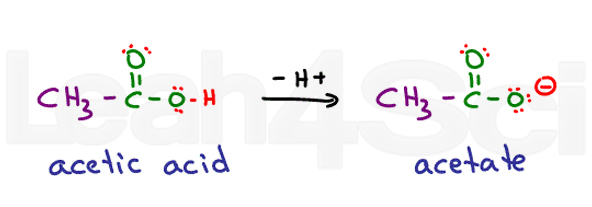
Tenk på ethanoic syre. Sitt vanlige navn er eddiksyre. Når deprotonated du få acetat., Syrer er meget stabil i vannet, siden de er delvis oppladet i deres protonated form og fullt oppladet i deres deprotonated form. Dette gjør dem svært hydrofil.
Glutaminsyre / GlutamateGluE
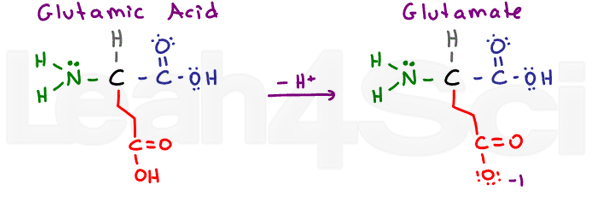
igjen har vi en ‘jerv’ aminosyre med en ekstra CH2-gruppe. Glutaminsyre refererer til protonated sure form, og glutamat refererer til deprotonated konjugat base/salt form.
Som asparaginsyre, glutaminsyre er meget stabil i vannet, og dermed hydrofile.,
Grunnleggende Aminosyrer
Grunnleggende aminosyrer inneholder et nitrogen atom med et enslig elektron par i stand til å angripe et hydrogenatom. Når et grunnleggende aminosyre er utsatt for en lav (sur) pH, det vil ta tak i en av de frie protoner i løsningen for å danne en kobling syre salt. Disse er lett kjennelig på den positive nitrogen i siden kjeden. I motsetning til den sure aminosyrer, er det ingen «vanlig brukte navn’ til å huske for disse konjugat salter.
LysineLysK
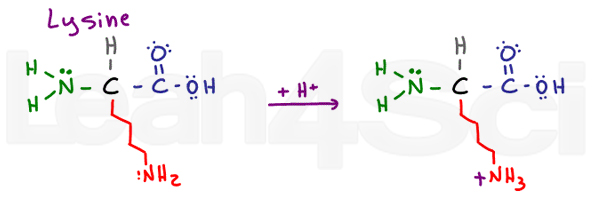
Lysin er en enkel grunnleggende aminosyre., Til tross for en lang og potensielt hydrofobe kjede, det har en grunnleggende NH2 på slutten. I sin grunnleggende deprotonated form, lysin er nøytral og hydrofile; imidlertid, hvis den finnes i fysiologisk pH, lysin vil plukke opp en H+ fra løsning for å danne en NH3+ salt. Salter er ladet og derfor definitivt hydrofile
ArginineArgR
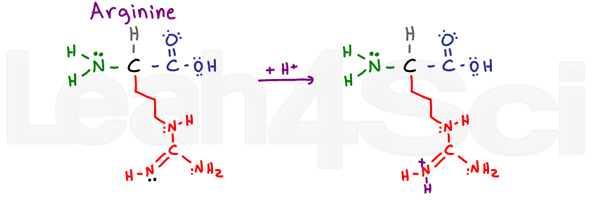
Arginin er forvirrende og gjør meg si ARGh eller R for kort. Hvorfor? Den grunnleggende delen av denne variabelen konsernet består av et NH, C=N-H NH2.,
Det 2 single-bundet nitrogen atomer kan bruke sine enslig par til å resonere med karbon-og dobbeltrom bundet nitrogen atom. Dette gjør deres elektroner UTILGJENGELIG for opptrer som en base. Men, det doble-bundet nitrogen bruker sin pi bond til å resonere, forlater sin gratis enslig par (vist i sort) til å fungere som den grunnleggende nitrogen på denne gruppen.
Argh!
HistidineHisH

Histidin er en annen vanskelig utgangspunkt for den samme grunnen som arginin. SOM nitrogen er grunnleggende? Se på tegningen her, spesielt på lone par på 2 nitrogen atomer., Den histidin ringen er en heterosykliske aromatiske stoff. Øvre nitrogen atom ikke har en pi bond. Dette betyr at det må bruke sin enslig par til å delta i resonans.
lavere nitrogen atom allerede har en klangfull pi bond. Dette etterlater sin ensomme elektroner (vist i sort) fri til å ta en proton, gjør dette det grunnleggende atom.
I konklusjonen
aminosyrer er en kritisk komponent for biologiske strukturer og din forståelse av biologi og biokjemi på MCAT., Og så, som du prøver å huske alt om disse 20 aminosyrer, er det viktig at du også forstå hvorfor du har polare og upolare aminosyrer, hva gjør variabel gruppe hydrofobe eller hydrofile, og selvfølgelig, den logikken bak protonated/deprotonated sure og basiske aminosyrer.