 Les acides aminés sont les éléments constitutifs des êtres vivants. Les longues chaînes d’acides aminés constituent les protéines, qui constituent à leur tour de nombreux composants cellulaires structurels et fonctionnels.
Les acides aminés sont les éléments constitutifs des êtres vivants. Les longues chaînes d’acides aminés constituent les protéines, qui constituent à leur tour de nombreux composants cellulaires structurels et fonctionnels.
J’aime penser à la cellule comme une ville autonome où le noyau est la capitale, les mitochondries sont la centrale électrique et ainsi de suite. Mais alors vous avez vos travailleurs, votre système de transport et la structure même de la ville cellulaire, qui sont tous faits de protéines – qui à leur tour sont faites d’acides aminés.,
La complexité d’une structure protéique est déterminée par sa séquence d’acides aminés et la nature chimique de leurs chaînes latérales de groupe variable. Le MCAT nécessite de comprendre la nature des chaînes latérales polaires et non polaires et la torsion et les conformations causées par les interactions hydrophobes et hydrophiles
Et oui, vous devriez mémoriser chaque acide aminé pour le MCAT. Cela inclut la chaîne latérale, le nom complet, le nom à 3 lettres et l’abréviation à une seule lettre. Mais ne collez pas simplement les mots et les structures sur des cartes mémoire dans l’espoir de les forcer dans votre mémoire., Vous devez vous attaquer activement à chaque acide aminé individuellement.
Pour une liste de référence rapide, téléchargez mon guide d’étude gratuit sur les acides aminés
- Écrivez le nom complet
- Dessinez la structure des acides aminés et le groupe variable
- Écrivez les abréviations à 3 lettres et à une lettre
- Verbalisez quelque chose d’unique à propos de cette chaîne latérale spécifique-à haute voix! Plus la connexion est drôle et folle, plus vous vous en souviendrez facilement.,
- Répétez immédiatement le processus de dénomination/dessin
- Répétez chaque semaine jusqu’à ce que vous vous sentiez SOLIDE avec cette information
La structure de base d’un acide aminé
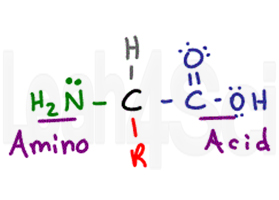 L’acide aminé tire son nom de ses deux groupes fonctionnels primaires. L’acide aminé a un carbone chiral central appelé carbone alpha (noir). Attaché au carbone central, vous avez un atome d’hydrogène (gris), un groupe amino ou NH2 (vert) et un groupe COOH acide carboxylique (violet). Enfin, nous avons le groupe R (rouge), qui est une chaîne latérale variable.,
L’acide aminé tire son nom de ses deux groupes fonctionnels primaires. L’acide aminé a un carbone chiral central appelé carbone alpha (noir). Attaché au carbone central, vous avez un atome d’hydrogène (gris), un groupe amino ou NH2 (vert) et un groupe COOH acide carboxylique (violet). Enfin, nous avons le groupe R (rouge), qui est une chaîne latérale variable.,
Il existe 20 acides aminés différents qui se distinguent par leurs chaînes latérales uniques. Ils vont d’un simple atome d’hydrogène (glycine) à un système aromatique résonnant complexe à 2 cycles (tryptophane).
Bien que la version entièrement neutre ci-dessus soit la façon dont la plupart des étudiants étudient les acides aminés, et la forme que nous utiliserons dans cet article, gardez à l’esprit que cela est techniquement incorrect.
Acide aminé sous forme de Zwitterion
Puisque le groupe carboxyle est acide et le groupe amino basique, les deux existeront sous forme de zwitterion sous leurs formes chargées conjuguées à pH physiologique., Plus sur zwitterion et les charges d’acides aminés dans mon prochain article (lien à suivre).
Un dernier concept avant de décomposer les acides aminés individuels, et c’est la structure protéique en 3 dimensions. Dans un système biologique, la structure détermine la fonction, de sorte que la compréhension des caractéristiques des acides aminés est essentielle pour comprendre la structure et, en fin de compte, la fonction des protéines.
Structure primaire d’une protéine 3D
Le premier et le plus important facteur de détermination de la structure des protéines est la séquence des acides aminés., Si la chaîne polypeptidique est attachée dans un ordre différent, vous obtenez une structure globale très différente.
Structure secondaire d’une protéine 3-D
La structure secondaire provient des interactions de liaison hydrogène de l’épine dorsale. La liaison peptidique transforme chaque ancien groupe carboxyle et aminé en un groupe fonctionnel amide. La structure secondaire de l’hélice alpha et des feuilles plissées bêta provient de la liaison hydrogène entre l’oxygène partiellement négatif sur le carbonyle et l’hydrogène partiellement positif sur l’azote.,
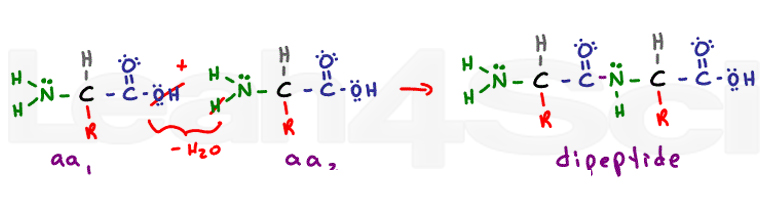
Structure tertiaire d’une protéine 3-D
La structure tertiaire est l’endroit où le pliage tridimensionnel réel est introduit, et c’est la première fois que vous remarquerez des interactions en chaîne latérale. C’est là que la connaissance et la compréhension des chaînes latérales d’acides aminés sont essentielles.
Permettez-moi de me répéter, la structure tertiaire est la première fois que vous verrez des interactions variables de la chaîne latérale du groupe R sur la chaîne polypeptidique. Beaucoup d’étudiants confondent cela avec la structure secondaire, qui n’est que des interactions dorsales.,
Structure quaternaire d’une protéine Multi-polypeptidique 3D
La structure quaternaire fait référence aux interactions de groupe variables entre différents polypeptides pour former une seule protéine plus grande.
Les structures quaternaires ne se trouvent pas dans toutes les protéines. Si la protéine ne contient qu’un seul brin d’acide aminé, le plus haut niveau de pliage est sa structure tertiaire. Cependant, si la protéine est composée de plusieurs sous-unités polypeptidiques, alors la structure quaternaire est ce qui maintient les différents polypeptides ensemble.,
Maintenant que vous comprenez l’importance des caractéristiques de la chaîne latérale, plongeons dans les acides aminés. Gardez à l’esprit que puisque les groupes parents amino et carboxyle sont « occupés » avec la structure primaire/secondaire, ils ne sont PAS analysés lors de l’étude des propriétés et des caractéristiques de la chaîne latérale.
Cela signifie que vous ignorez toute polarité potentielle sur les groupes carboxyle et amino et ne regardez que les chaînes latérales.
Acides aminés hydrophobes Non polaires
Hydrophobe, comme son nom l’indique est hydro-eau, phobique – craignant., Les acides aminés hydrophobes ont peu ou pas de polarité dans leurs chaînes latérales. Le manque de polarité signifie qu’ils n’ont aucun moyen d’interagir avec des molécules d’eau hautement polaires, ce qui les rend craintifs.
Il n’y a que cinq atomes qui apparaîtront dans vos groupes variables d’acides aminés: H, C, N, O et S.
Ne considérez la polarité que lorsque vous avez N, O, S comme facteur « majoritaire ». Je vous signale qu’ils se produisent. Cependant, si tout ce que vous voyez sont Cs et Hs, vous devriez reconnaître automatiquement un acide aminé craignant l’eau.,
GlycineGlyG
La glycine est un acide aminé unique en ce sens qu’elle n’a pas vraiment de groupe R. Lorsque vous pensez « groupe variable R », vous devriez penser au carbone attaché à d’autres atomes. Mais la glycine n’a qu’un hydrogène à sa position de chaîne latérale. Puisque la glycine a 2 atomes d’hydrogène, un chacun sur la chaîne parent et latérale, c’est le seul acide aminé symétrique et donc achiral. Comme l’hydrogène est non polaire, la glycine est un acide aminé hydrophobe. La chaîne latérale de l’hydrogène fait de la glycine le plus petit acide aminé.,
AlanineAlaA
L’alanine est un acide aminé simple qui a juste un groupe méthyle ou CH3 comme chaîne latérale. Puisque vous ne voyez que du carbone et de l’hydrogène, l’alanine est un acide aminé hydrophobe non polaire. Il est important de reconnaître que c’est un très petit acide aminé et capable d’être « coincé » dans des boucles ou des chaînes serrées.
ValineValV
La valine est un autre acide aminé simple avec juste un groupe variable isopropyle. Tout comme l’alanine, nous ne voyons que du carbone et de l’hydrogène, faisant de la valine un acide aminé hydrophobe non polaire.,
LeucineLeuL
Vous pouvez reconnaître la leucine comme ayant le même groupe variable que la valine mais avec un groupe CH2 supplémentaire. Ou vous pouvez simplement reconnaître sa chaîne latérale isobutyle.
Voir cette vidéo si vous n’êtes pas familier avec les chaînes latérales ramifiées comme l’isopropyle ou le sec-butyle. Puisque la leucine a juste Cs et Hs, c’est un acide aminé non polaire craignant l’eau.
IsoleucineIleI
L’isoleucine, comme son nom l’indique, est un isomère de la leucine. La différence est le placement du CH3 pour une chaîne latérale sec-butyle plutôt qu’une chaîne latérale isobutyle. Tout comme son isomère, l’isoleucine est apolaire et hydrophobe.,
MethionineMetM
La méthionine est le premier acide aminé potentiellement délicat. Sa chaîne latérale contient principalement Cs et Hs mais avec un atome de soufre intégré. Bien que vous puissiez penser qu’il est hydrophile, faites attention à l’emplacement de l’atome de soufre. Intégré dans la chaîne et attaché à des atomes de carbone, le soufre est partiellement « caché » de l’environnement extérieur.
Bien que vous n’ayez pas besoin de connaître les valeurs d’électronégativité pour le MCAT, il est utile de comprendre que S = 2.58 et C = 2.55. Puisque la différence d’électronégativité est inférieure à 0,5, il n’y a PAS de polarité de ce côtéla chaîne.,
Vous devez également reconnaître la méthionine comme le codon de départ AUG dans la traduction de l’ARN en protéines.
PhenylalaninePheF
Pour vous aider à vous rappeler que la Phénylalanine est F rappelez-vous que » ph « est prononcé comme un « F ». Ne mélangez pas cela avec P pour proline.
Faites attention à la structure de la phénylalanine. Il a un seul groupe de carbone avec un anneau de benzène attaché. Le phényle est le nom d’un substituant benzénique, et cette molécule a un benzène (phényle) attaché à la structure de l’alanine. Puisque la phénylalanine n’a que Cs et Hs dans sa chaîne latérale aromatique, elle est non polaire et hydrophobe.,
TryptophanTrpW
C’est une question délicate. Remarquez le N-H dans cette chaîne latérale. N-H doit être polaire et capable de liaison hydrogène. Cependant, il y a deux raisons pour lesquelles cet acide aminé est toujours non polaire et hydrophobe.
- Le groupe N-H est une infime partie de la très grande chaîne latérale.
- Regardez attentivement l’azote, et plus important encore, à sa seule paire. Les électrons de l’azote font partie intégrante de l’aromaticité conjuguée de la chaîne latérale du tryptophane., En d’autres termes, pensez à ses électrons comme « trop distraits » par la résonance pour accorder beaucoup d’attention à l’environnement extérieur de l’eau.
Le MCAT vous oblige à reconnaître qu’il s’agit d’un acide aminé volumineux et volumineux. Mais comme il s’agit d’un examen à choix multiples, vous pouvez simplement mémoriser que le tryptophane est le SEUL acide aminé à DEUX anneaux fusionnés.
En fait, il est si grand qu’il peut TRÉBUCHER (trp) sur lui-même et crier Waaaaaaa(W)
(Note sur les mnémoniques: Plus le mnémonique est drôle, bizarre ou plus sale, plus vous vous en souviendrez probablement. Gardez cela à l’esprit pour l’école de médecine.,)
ProlineProP
La proline est un acide aminé unique car c’est LE SEUL qui incorpore l’épine dorsale dans sa chaîne latérale. La chaîne latérale proline est une chaîne 3-carbone qui boucle autour et se fixe au groupe amino parent. Cela signifie que, contrairement aux autres acides aminés, la proline n’a PAS un atome d’hydrogène sur son azote lorsqu’une partie d’une chaîne polypeptidique.
Cependant, vous ne pouvez pas oublier que l’azote ne fait PAS VRAIMENT partie du groupe de variables, ce qui signifie qu’il ne peut pas contribuer à la polarité. Puisque nous n’avons que 3 groupes CH2 à analyser, nous obtenons une chaîne latérale hydrophobe non polaire., Cette boucle parente crée un renflement et ne permet pas à une chaîne contenant une proline d’être linéaire, ce qui signifie que vous la trouverez souvent dans des boucles et à la fin d’une hélice alpha.
Acides aminés hydrophobes polaires
*Ceci est une section collante, et selon l’endroit où vous recherchez, vous pouvez trouver les éléments suivants classés comme polaires ou non polaires, hydrophiles ou hydrophobes. Faites attention à la présence de groupes polaires qui sont petits par rapport à la chaîne latérale globale, ou très faiblement polaires et donc hydrophobes.,
CysteineCysC
La cystéine a un S-H légèrement polaire, mais sa polarité est si légère que la cystéine est incapable d’interagir correctement avec l’eau, ce qui la rend hydrophobe.
La cystéine est un acide aminé très important en ce qui concerne la structure tertiaire et quaternaire. La plupart des interactions en chaîne latérale comprennent les interactions polaires/chargées ou la dispersion non polaire de Van Der Waals et de London. Cependant, la chaîne latérale de la cystéine est capable de former un pont disulfure, qui est une liaison covalente entre 2 atomes de soufre par oxydation de la chaîne latérale et élimination de 2 atomes d’hydrogène., Cette liaison covalente est beaucoup plus forte et plus permanente par rapport aux interactions tertiaires et quaternaires standard.
C’est aussi la cause d’une erreur expérimentale dans la détermination de la taille/longueur des protéines pour les protéines avec plusieurs sous-unités.
TyrosineTyrY
Certains étudiants voient cela comme une fuite d’un pneu (tyr).
Examinez de près la tyrosine. Que voyez-vous? Il ressemble à la phénylalanine aromatique avec un groupe OH en position para (ortho/meta/para 2ème vidéo).,
D’une part, nous avons un groupe OH très polaire et capable de liaison hydrogène, mais d’autre part, le OH est minuscule par rapport à la taille du groupe benzyle (CH2-phényle). Cette énigme est une source courante de confusion, mais si vous comprenez cela, vous reconnaîtrez que la tyrosine, bien que polaire, est toujours un acide aminé hydrophobe.
Acides aminés polaires hydrophiles
Hydrophile comme son nom l’indique vient de l’hydro-eau et de l’amour philique.
La polarité provient d’une différence d’électronégativité de 0,5 à 1,9 entre les atomes liés., Bien que vous n’ayez pas à connaître ces valeurs pour le MCAT, vous devez reconnaître que les liaisons polaires existeront lorsque N et O sont liés à des atomes non carbonés.
La différence d’électronégativité est suffisante pour créer une légère séparation de charge ou de polarité. Et puisque like attire like, ces groupes partiellement chargés seront attirés par des groupes chargés de manière opposée ou partiellement chargés tels que l’eau. Ces groupes vont tordre la chaîne polypeptidique afin d’interagir les uns avec les autres et avec l’eau.
Les groupes hydrophobes se détourneront de ces chaînes latérales.,
SerineSerS
Considérez la sérine comme une alanine avec un groupe OH attaché. Contrairement à la tyrosine, l’OH est majoritaire dans cette molécule et sa polarité est suffisante pour influencer l’ensemble du groupe. Cela rend la série polaire et très hydrophile.
ThreonineThrT
Il existe plusieurs façons d’examiner ce groupe. Vous pouvez le considérer comme de la sérine avec un groupe méthyle supplémentaire, ou comme de la valine mais avec un OH remplaçant l’un des groupes méthyle. Je me souviens de THREEonine comme ayant 3 groupes différents: CH, CH3 et OH.
Comme la sérine, ce groupe variable est polaire et hydrophile.,
AsparagineAsnN
Essayez ceci: Slur votre discours comme vous dites « asparagine » très vite. On dirait que vous dites…N, c’est ainsi que je me souviens de l’abréviation de 3 lettres pour cet acide aminé. Le NH2 à la fin de cette molécule vous fait penser « base », mais regardez son voisin. NH2 près d’un carbonyle forme un amide, qui n’aime pas agir comme un acide ou une base dans des conditions physiologiques standard. Cependant, avec des charges partielles et une capacité de liaison H à la fois au niveau de l’oxygène carbonyle ET des groupes NH2, nous obtenons un acide aminé hydrophile polaire.,
GlutamineGlnQ
Je pense que les deux acides aminés « surabondants » sont des gloutons ayant « consommé » un groupe CH2 supplémentaire. La glutamine a la même structure que l’asparagine mais avec un CH2 glouton supplémentaire dans sa chaîne. Tout comme l’asparagine, elle est polaire et hydrophile.
Chaînes latérales acides et acides aminés basiques
L’acidité et la basicité des acides aminés sont une autre source de confusion chez les étudiants. S’il commence comme un acide, devient-il une base? Comment puis-je trouver la charge? Et ainsi de suite.
Voici l’astuce: un ACIDE carboxylique dans la chaîne latérale vous donnera un acide aminé de l’acide., Lorsqu’un groupe carboxyle est déprotoné, vous obtenez un sel de base conjugué. Donc, si vous voyez la version saline d’une chaîne latérale d’acide carboxylique, alors qu’il s’agit TECHNIQUEMENT d’une « base conjuguée », nous l’appellerons simplement la version saline de l’acide aminé acide. Même chose pour la base. Recherchez les atomes d’azote « non distraits » dans la chaîne latérale.
acides Aminés Acides
Les acides aminés acides devrait être très familier par rapport à l’asparagine et la glutamine. Et c’est parce que tout à leur sujet est le même, sauf pour le groupe fonctionnel terminal., Les amides (discutés ci-dessus) sont polaires, mais si le NH2 est échangé contre un groupe OH, vous obtenez un groupe carboxyle acide.
l’Acide Aspartique / AspartateAspD
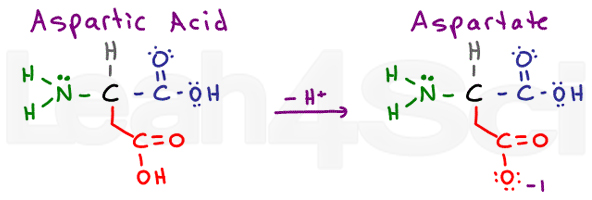
l’acide Aspartique se réfère à la protoné forme acide de l’acide aminé. Lorsqu’il est déprotoné, vous verrez souvent le sel de base conjugué appelé aspartate. C’est la nomenclature standard pour les acides carboxyliques.
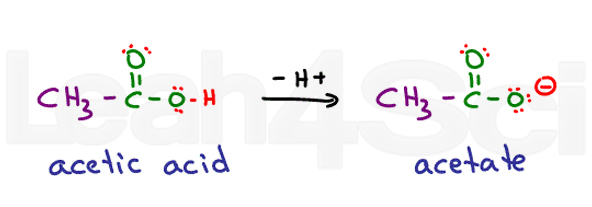
Pense à de l’acide éthanoïque. Son nom commun est l’acide acétique. Lorsque déprotoné vous obtenez de l’acétate., Les acides sont très stables dans l’eau car ils sont partiellement chargés sous leur forme protonée et complètement chargés sous leur forme déprotonée. Cela les rend très hydrophiles.
Acide glutamique/GlutamateGluE
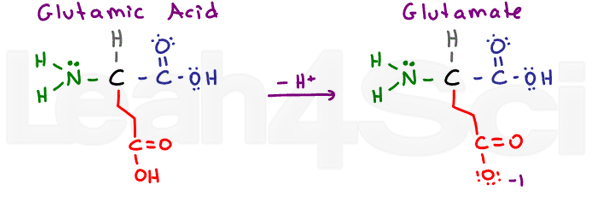
Encore une fois, nous avons un acide aminé ‘glouton’ avec un groupe CH2 supplémentaire. L’acide glutamique se réfère à la forme acide protonée, et le glutamate se réfère à la forme conjuguée base/sel déprotonée.
Comme l’acide aspartique, l’acide glutamique est très stable dans l’eau et donc hydrophile.,
Acides aminés basiques
Les acides aminés basiques contiennent un atome d’azote avec une seule paire d’électrons capable d’attaquer un atome d’hydrogène. Lorsqu’un acide aminé basique est soumis à un pH faible (acide), il saisit l’un des protons libres en solution pour former un sel acide conjugué. Ceux-ci sont facilement reconnaissables par l’azote positif dans la chaîne latérale. Contrairement aux acides aminés acides, il n’y a pas de « noms couramment utilisés » à mémoriser pour ces sels conjugués.
LysineLysK
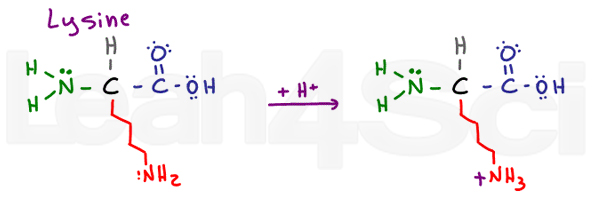
La lysine est un acide aminé basique simple., Malgré une chaîne longue et potentiellement hydrophobe, il a un NH2 de base à la fin. Sous sa forme déprotonée basique, la lysine est neutre et hydrophile; cependant, si elle se trouve dans le pH physiologique, la lysine captera un H+ de la solution pour former un sel NH3+. Les sels sont chargés et donc définitivement hydrophiles
ArginineArgR
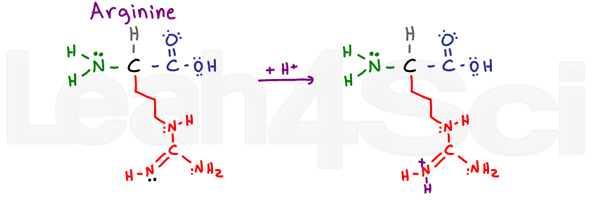
L’arginine est déroutante et me fait dire ARGh ou R pour faire court. Pourquoi? La partie de base de ce groupe de variables se compose d’un NH, C=N-H et NH2.,
Les 2 atomes d’azote à liaison unique peuvent utiliser leurs paires solitaires pour résonner avec l’atome de carbone et l’atome d’azote à liaison double. Cela rend leurs électrons INDISPONIBLES pour agir comme base. Cependant, l’azote à double liaison utilise sa liaison pi pour résonner, laissant sa paire solitaire libre (représentée en noir) agir comme azote de base sur ce groupe.
Argh!
HistidineHisH

L’histidine est une autre base délicate pour la même raison que l’arginine. LEQUEL l’azote est la plus basique? Regardez le dessin ici, en particulier les paires solitaires sur les 2 atomes d’azote., Le cycle histidine est un composé aromatique hétérocyclique. L’atome d’azote supérieur n’a pas de liaison pi. Cela signifie qu’il doit utiliser ses paires solitaires pour participer à la résonance.
L’atome d’azote inférieur a déjà une liaison pi résonnante. Cela laisse ses électrons solitaires (représentés en noir) libres de saisir un proton, ce qui en fait l’atome de base.
En conclusion
Les acides aminés sont un composant essentiel aux structures biologiques et à votre compréhension de la biologie et de la biochimie sur le MCAT., Et donc, lorsque vous essayez de tout mémoriser sur ces 20 acides aminés, il est important que vous compreniez également pourquoi vous avez des acides aminés polaires et non polaires, ce qui rend le groupe variable hydrophobe ou hydrophile, et bien sûr, la logique derrière les acides aminés acides et basiques protonés/déprotonés.