 aminoácidos são os blocos de construção dos seres vivos. Cadeias longas de aminoácidos compõem proteínas, que por sua vez compõem muitos componentes estruturais e funcionais das células.gosto de pensar na célula como uma cidade autónoma onde o núcleo é a capital, a mitocôndria é a central eléctrica e assim por diante. Mas então você tem seus trabalhadores, o sistema de transporte e a própria estrutura da cidade celular, que são todas feitas de proteínas – que por sua vez são feitas de aminoácidos.,
aminoácidos são os blocos de construção dos seres vivos. Cadeias longas de aminoácidos compõem proteínas, que por sua vez compõem muitos componentes estruturais e funcionais das células.gosto de pensar na célula como uma cidade autónoma onde o núcleo é a capital, a mitocôndria é a central eléctrica e assim por diante. Mas então você tem seus trabalhadores, o sistema de transporte e a própria estrutura da cidade celular, que são todas feitas de proteínas – que por sua vez são feitas de aminoácidos.,
a complexidade de uma estrutura proteica é determinada pela sua sequência de aminoácidos e pela natureza química das suas cadeias laterais de grupo variável. O MCAT requer compreensão da natureza das cadeias laterais polares e não-polares e a torção e conformações causadas por interações hidrofóbicas e hidrofílicas
E sim, você deve estar memorizando cada aminoácido para o MCAT. Isto inclui a cadeia lateral, nome completo, nome de três letras e abreviatura de uma única letra. Mas não basta colocar as palavras e estruturas em cartões de memória esperando forçá-lo em sua memória., Você precisa atacar ativamente cada aminoácido individualmente.
Para uma referência rápida de download da lista minha de Aminoácidos livres Cheat Sheet Guia de Estudo
- Escreva o nome completo
- Desenhar o aminoácido estrutura e a variável grupo
- Escrever o 3-letra e letra simples abreviaturas
- Verbalizar algo único sobre este específico cadeia lateral – out loud! Quanto mais engraçada e louca a conexão, mais fácil você se lembrará dela.,
- Repita a nomeação/processo de desenho de uma vez para a DIREITA-AFASTADO
- Repetir semanalmente até que você se sinta SÓLIDA com esta informação
A Estrutura Básica de um Aminoácido
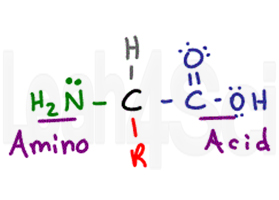 O aminoácido recebe o nome de seus dois principais grupos funcionais. O aminoácido tem um carbono quiral central chamado carbono alfa (negro). Ligado ao carbono central você tem um átomo de hidrogênio (cinza), um amino ou grupo NH2 (verde), e um grupo COOH de ácido carboxílico (roxo). Finalmente temos o grupo R (vermelho), que é uma cadeia lateral variável.,existem 20 aminoácidos diferentes distinguidos pelas suas cadeias laterais únicas. Eles variam de um simples átomo de hidrogênio (glicina) a um complexo sistema aromático ressonante de 2 Anéis (triptofano).
O aminoácido recebe o nome de seus dois principais grupos funcionais. O aminoácido tem um carbono quiral central chamado carbono alfa (negro). Ligado ao carbono central você tem um átomo de hidrogênio (cinza), um amino ou grupo NH2 (verde), e um grupo COOH de ácido carboxílico (roxo). Finalmente temos o grupo R (vermelho), que é uma cadeia lateral variável.,existem 20 aminoácidos diferentes distinguidos pelas suas cadeias laterais únicas. Eles variam de um simples átomo de hidrogênio (glicina) a um complexo sistema aromático ressonante de 2 Anéis (triptofano).
enquanto a versão totalmente neutra acima é como a maioria dos alunos estudam aminoácidos, e a forma que vamos usar neste artigo, tenha em mente que isso é tecnicamente incorreto.
aminoácido na forma de Zwitterion
Uma vez que o grupo carboxilo é ácido e o grupo amino básico, os dois existirão como um zwitterion em suas formas conjugadas carregadas em pH fisiológico., Mais sobre zwitterion e cargas de aminoácidos em meu próximo artigo (link para seguir).
Um conceito final antes de decompormos os aminoácidos individuais, e que é a estrutura proteica tridimensional. Em uma estrutura de sistema biológico determina a função, então compreender as características dos aminoácidos é a chave para entender a estrutura e, em última análise, a função proteica.o primeiro e mais importante fator de determinação da estrutura proteica é a sequência de aminoácidos., Se a cadeia polipeptídica estiver ligada numa ordem diferente, obtém-se uma estrutura global muito diferente.
estrutura secundária de uma proteína 3-D
A estrutura secundária vem de interações de ligação de hidrogênio da coluna vertebral. A ligação peptídica transforma todos os antigos grupos carboxilo e amino num grupo funcional de amida. A estrutura secundária da hélice alfa e das folhas com pregas beta vem da ligação do hidrogênio entre o oxigênio parcialmente negativo no carbonilo e o hidrogênio parcialmente positivo no nitrogênio.,
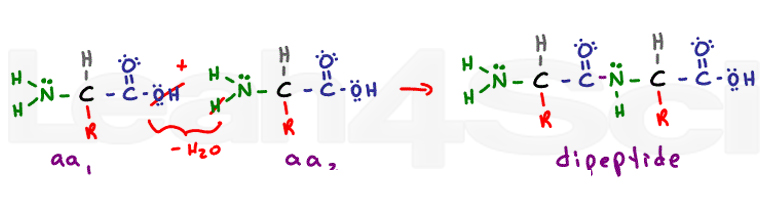
estrutura terciária de uma proteína 3-D
A estrutura terciária é onde a dobra tridimensional real é introduzida, e esta é a primeira vez que você vai notar interações de cadeia lateral. É aqui que o conhecimento e a compreensão das cadeias laterais de aminoácidos são críticos.
Me deixe repetir, a estrutura terciária é a primeira vez que você verá interações variáveis da cadeia lateral do grupo R na cadeia polipeptídica. Muitos alunos confundem isso com a estrutura secundária, que é apenas interações de espinha dorsal.,
Quaternário estrutura de uma proteína 3-D Multi-polipéptido estrutura quaternária refere-se às interações de grupo variável entre diferentes polipéptidos para formar uma única proteína maior.as estruturas quaternárias não são encontradas em todas as proteínas. Se a proteína contém apenas uma cadeia de aminoácidos, então o nível mais elevado de dobragem é a sua estrutura terciária. No entanto, se a proteína é composta por múltiplas subunidades polipeptídicas, então a estrutura quaternária é o que mantém os diferentes polipeptídeos juntos.,agora que você entende o significado das características da cadeia lateral, vamos mergulhar em aminoácidos. Tenha em mente que, uma vez que os grupos amino e carboxilo progenitores estão “ocupados” com estrutura primária/secundária, eles não são analisados ao estudar propriedades e características da cadeia lateral.isso significa que você ignora qualquer polaridade potencial nos grupos carboxilo e amino e só olha para as cadeias laterais.hidrofóbico, como o nome indica é hidro-água, temendo fobia., Os aminoácidos hidrofóbicos têm pouca ou nenhuma polaridade nas suas cadeias laterais. A falta de polaridade significa que eles não têm como interagir com moléculas de água altamente polares, tornando-os tementes à água.
existem apenas cinco átomos que irão aparecer em seus grupos variáveis de aminoácidos: H, C, N, O, E S. Apenas considere a polaridade quando você tem N, O, S como o Fator de ‘maioria’. Vou apontá-los à medida que ocorrem. No entanto, se tudo o que você vê são Cs e Hs você deve reconhecer automaticamente um aminoácido temendo a água.,
Glicineglyg
glicina é um aminoácido único na medida em que não tem realmente um grupo R. Quando você pensa em ‘grupo R variável’, você deve pensar em carbono ligado a outros átomos. Mas a glicina só tem hidrogénio na sua posição de cadeia lateral. Uma vez que a glicina tem 2 átomos de hidrogénio, um na cadeia progenitora e lateral, é o único aminoácido simétrico e, portanto, achiral. Como o hidrogênio não é polar, a glicina é um aminoácido hidrofóbico. A cadeia lateral do hidrogénio faz da glicina o menor aminoácido.,
AlanineAlaA
alanina é um aminoácido simples que tem apenas um grupo metil ou CH3 como sua cadeia lateral. Como não se vê nada além de carbono e hidrogénio, a alanina é um aminoácido hidrofóbico não polar. É importante reconhecer que este é um aminoácido muito pequeno e capaz de ser “preso” em laços apertados ou correntes.
ValineValV
valina é outro aminoácido simples com apenas um grupo variável isopropilo. Tal como a alanina, só vemos carbono e hidrogénio, fazendo da valina um aminoácido hidrofóbico não polar.,
LeucineLeuL
pode reconhecer a leucina como tendo o mesmo grupo variável que a valina, mas com um grupo extra CH2. Ou pode simplesmente reconhecer a sua corrente lateral de isobutilo.Veja este vídeo se você não está familiarizado com cadeias laterais ramificadas como isopropil ou sec-butil. Uma vez que a leucina tem apenas Cs E Hs, é um aminoácido não polar temido a água.
IsoleucineIleI
Isoleucina, como o nome indica, é um isómero da leucina. A diferença é a colocação do CH3 para um sec-butil em vez de uma cadeia lateral isobutil. Assim como seu isômero, isoleucina é não-Solar e hidrofóbica.,
Metioninemetm
metionina é o primeiro aminoácido potencialmente complicado. A sua cadeia lateral contém sobretudo Cs E Hs, mas com um átomo de enxofre incorporado. Enquanto você pode pensar que é hidrofílico, preste atenção à localização do átomo de enxofre. Embutido na cadeia e ligado apenas aos átomos de carbono, o enxofre é parcialmente “escondido” do ambiente exterior.
embora você não tenha que conhecer os valores de eletronegatividade para o MCAT, ele ajuda a entender Que S = 2.58 E C = 2.55. Uma vez que a diferença na eletronegatividade é inferior a 0,5, não há polaridade neste sidechain.,
Você também deve reconhecer a metionina como o início do codon AUG na tradução de RNA para proteínas.
Fenilalaninefef
para o ajudar a lembrar que a fenilalanina é F lembre-se que o ” ph “é pronunciado como um “F”. Não mistures isto com P por proline.preste atenção à estrutura da fenilalanina. Tem um único grupo de carbono com um anel benzeno anexado. Fenil é o nome de um substituinte benzeno, e esta molécula tem um benzeno (fenil) ligado à estrutura da alanina. Como a fenilalanina não tem nada além de Cs e Hs em sua cadeia lateral aromática, é não-Solar e hidrofóbica.,
Triptofantrpw
Esta é difícil. Repara no N-H desta corrente lateral. N-H deve ser polar e capaz de ligar hidrogénio. No entanto, há duas razões para este aminoácido ainda não ser polar e hidrofóbico.
- o grupo N-H é uma pequena porção da cadeia lateral Muito Grande.
- olhe cuidadosamente para o nitrogênio, e mais importante, para seus pares solitários. Os elétrons de nitrogênio são parte integrante da aromaticidade conjugada para a cadeia lateral triptofana., Em outras palavras, pense em seus elétrons como “muito distraídos” pela ressonância para prestar muita atenção ao ambiente externo da água.
o MCAT requer que você reconheça que este é um aminoácido grande e volumoso. Mas como é um exame de escolha múltipla, podes simplesmente memorizar que o triptofano é o único aminoácido com dois anéis fundidos.
Na verdade, é tão grande que pode tropeçar (trp) sobre si mesmo e gritar Waaaaaaaa (W)
(nota sobre mnemônica: o mais engraçado, mais estranho, ou mais sujo o mnemônico, o mais provável você vai se lembrar disso. Lembra-te disto para a Faculdade de medicina.,)
ProlineProP
prolina é um aminoácido único, uma vez que é o único que incorpora a espinha dorsal em sua cadeia lateral. A cadeia lateral prolina é uma cadeia de 3-carbono que faz loops ao redor e se liga de volta ao grupo amino original. Isto significa que, ao contrário dos outros aminoácidos, prolina não tem um átomo de hidrogênio em seu nitrogênio quando parte de uma cadeia polipeptídica.
no entanto, você não pode esquecer que o nitrogênio não é realmente parte do grupo variável, o que significa que ele não pode contribuir com qualquer polaridade. Uma vez que temos apenas 3 grupos CH2 para analisar, temos uma cadeia lateral não-Solar hidrofóbica., Este laço-mãe cria uma protuberância e não permite que uma cadeia contendo prolina seja linear, o que significa que muitas vezes você vai encontrá-lo em loops e no final de uma hélice alfa.
aminoácidos hidrofóbicos polares
*esta é uma secção pegajosa, e dependendo de onde você pesquisar, você pode encontrar o seguinte categorizado como polar ou não-polar, hidrofílico ou hidrofóbico. Preste atenção à presença de grupos polares que são pequenos em comparação com o sidechain geral, ou muito fracamente polares e, portanto, hidrofóbicos.,
Cisteinecisc
cisteína tem um S-H ligeiramente polar, mas a sua polaridade é tão ligeira que a cisteína é incapaz de interagir adequadamente com a água, tornando-a hidrofóbica.a cisteína é um aminoácido muito importante quando se trata de estrutura terciária e quaternária. A maioria das interações de cadeia lateral incluem interações polares / carregadas ou dispersões não-polares de Van Der Waals e de Londres. However, cysteine’s side chain is capable of forming a dissulfide bridge, which is a covalent bonds between 2 sulfur atoms through side chain oxidation and removal of 2 hydrogen atoms., Esta ligação covalente é muito mais forte e permanente quando comparada com as interações terciárias e quaternárias padrão.This is also the cause for experimental error in determining protein size / length for proteins with multiple subunits.
Tirosinetyry
alguns alunos vêem isto como Oh vazando de um pneu (tyr).Veja BEM a tirosina. O que vês? Parece a fenilalanina aromática com um grupo OH na posição para (Orto/meta/para 2nd video).,
por um lado, temos um grupo OH muito polar e de ligação hidrogênio capaz, mas por outro lado, o OH é minúsculo quando comparado com o tamanho do grupo benzílico (CH2-fenil). Este enigma é uma fonte comum de confusão, mas se você entender isso, você vai reconhecer que a tirosina, enquanto polar, ainda é um aminoácido hidrofóbico.os aminoácidos hidrofílicos polares, tal como o nome indica, são hidrofílicos e filicamados.polaridade vem de uma diferença de 0,5-1,9 na eletronegatividade entre átomos ligados., Embora você não tenha que saber estes valores para o MCAT, você deve reconhecer que as ligações polares existirão quando N e O estão ligados a átomos não-Carbono.a diferença de eletronegatividade é suficiente para criar uma ligeira separação de carga ou polaridade. E como tal atrai semelhante, estes grupos parcialmente carregados serão atraídos por grupos opostos carregados ou parcialmente carregados, como a água. Estes grupos irão torcer a cadeia polipeptídica de modo a interagir uns com os outros e com a água.grupos hidrofóbicos se afastarão destas cadeias laterais.,
SerineSerS
pense na serina como alanina com um grupo OH ligado. Ao contrário da tirosina, A OH é a maioria nesta molécula e sua polaridade é suficiente para influenciar todo o grupo. Isto torna a série polar e muito hidrofílica.
Treoninethrt
Existem várias maneiras de olhar para este grupo. Você pode pensar nele como serina com um grupo metil extra, ou como valina, mas com um oh substituindo um dos grupos metil. Lembro-me da Treeonina ter três grupos diferentes: CH, CH3 e OH.como serina, este grupo variável é polar e hidrofílico.,Asparagineasnnn tenta isto: reduza o discurso enquanto diz “asparagina” muito depressa. Parece que estás a dizer como … N, que é como me lembro da abreviatura de 3 letras para este aminoácido. O NH2 no final desta molécula faz você pensar “base”, mas olhe para o vizinho. NH2 perto de um carbonilo forma um amida, que não gosta de agir como um ácido ou base sob condições fisiológicas padrão. No entanto, com cargas parciais e capacidade de ligação H tanto no oxigênio carbonila quanto nos grupos NH2, temos um aminoácido hidrofílico polar.,eu penso em ambos os aminoácidos “glut” como gluttons que “consumiram” um grupo extra CH2. A glutamina tem a mesma estrutura que a asparagina, mas com um CH2 Glutton extra na sua cadeia. Tal como a asparagina, é polar e hidrofílica.
cadeias laterais ácidas e básicas de aminoácidos
acidez e basicidade nos aminoácidos é mais uma fonte de confusão entre os alunos. Se começa como um ácido, torna-se uma base? Como encontro a carga? E assim por diante.aqui está o truque: um ácido carboxílico na cadeia lateral dar-lhe-á um aminoácido ácido., Quando um grupo carboxilo é desprotonado, obtém-se um sal base conjugado. Então, se você ver a versão salina de uma cadeia lateral de ácido carboxílico, enquanto é tecnicamente uma base conjugada, simplesmente nos referiremos a ela como a versão salina do aminoácido ácido. O mesmo para a base. Cuidado com os átomos de azoto “não distraídos” na cadeia lateral.aminoácidos ácidos Os aminoácidos ácidos devem parecer muito familiares em comparação com asparagina e glutamina. E isso é porque tudo sobre eles é o mesmo, exceto para o grupo funcional terminal., As amidas (discutidas acima) são polares, mas se o NH2 é trocado por um grupo OH, você obtém um grupo carboxilo ácido.
ácido aspártico / Aspartatoaspd
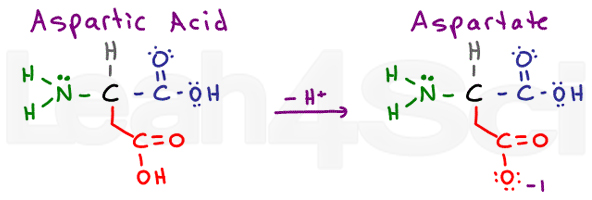
ácido aspártico refere-se à forma protonada do aminoácido. Quando desprotonado, verá o sal base conjugado chamado aspartato. Esta é a nomenclatura padrão para ácidos carboxílicos.
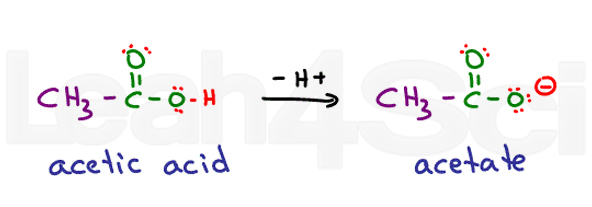
pensa no ácido etanóico. Seu nome comum é ácido acético. Quando desprotonado você tem acetato., Os ácidos são muito estáveis na água, uma vez que são parcialmente carregados na sua forma protonada e totalmente carregados na sua forma desprotonada. Isto torna-os altamente hidrofílicos.
ácido glutâmico / GlutamateGluE
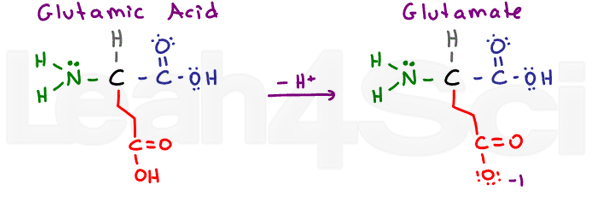
mais uma vez temos um aminoácido ‘glutton’ com um grupo extra CH2. Ácido glutâmico refere-se à forma ácida protonada, e glutamato refere-se à forma base/Sal conjugada desprotonada.como o ácido aspártico, o ácido glutâmico é muito estável na água e, portanto, hidrofílico.,
aminoácidos básicos
aminoácidos básicos contêm um átomo de azoto com um par de electrões solitário capaz de atacar um átomo de hidrogénio. Quando um aminoácido básico é submetido a um baixo pH (ácido), ele irá agarrar um dos prótons livres em solução para formar um sal ácido conjugado. Estes são facilmente reconhecidos pelo nitrogênio positivo na cadeia lateral. Ao contrário dos aminoácidos ácidos, não existem “nomes comumente usados” para memorizar esses sais conjugados.
Lisinelisk
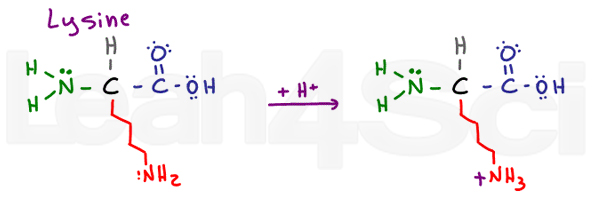
lisina é um simples aminoácido básico., Apesar de uma cadeia longa e potencialmente hidrofóbica, tem um NH2 básico no final. Na sua forma deprotonada básica, a lisina é neutra e hidrofílica; no entanto, se encontrada em pH fisiológico, a lisina vai pegar um H+ da solução para formar um sal NH3+. Sais são carregados e portanto definitivamente hidrofílicos
Argininineargr
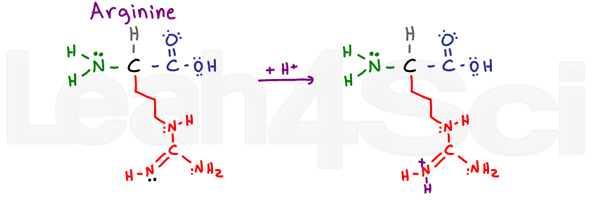
arginina é confusa e me faz dizer ARGh ou R para abreviar. Por quê? A parte básica deste grupo de variáveis consiste em NH, C=N-H e NH2.,os 2 átomos de nitrogênio de ligação única podem usar seus pares solitários para ressoar com o átomo de carbono e nitrogênio de ligação dupla. Isso torna seus elétrons indisponíveis para atuar como uma base. No entanto, o nitrogênio duplamente ligado usa sua ligação pi para ressoar, deixando seu par solitário livre (mostrado em preto) para agir como o nitrogênio básico neste grupo.Argh!
HistidineHisH

histidina é outra base complicada pela mesma razão que arginina. Qual é o nitrogênio básico? Olhe para o desenho aqui, particularmente para os pares solitários nos 2 átomos de nitrogênio., O anel de histidina é um composto aromático heterocíclico. O átomo de azoto superior não tem uma ligação pi. Isto significa que deve utilizar os seus pares solitários para participar na ressonância.o átomo de nitrogênio inferior já tem uma ligação pi ressonante. Isto deixa seus elétrons solitários (mostrados em preto) livres para pegar um próton, tornando este o átomo básico.
Em conclusão
aminoácidos são um componente crítico para as estruturas biológicas e para a sua compreensão da biologia e bioquímica sobre o MCAT., E assim, enquanto você tenta memorizar tudo sobre esses 20 aminoácidos, é importante que você também entenda por que você tem aminoácidos polares e não-polares, o que torna o grupo variável hidrofóbico ou hidrofílico, e, claro, a lógica por trás dos aminoácidos ácido protonado/desprotonado e básico.