aminokyseliny jsou stavebními kameny živých věcí. Dlouhé řetězce aminokyselin tvoří bílkoviny, které zase tvoří mnoho strukturních a funkčních buněčných složek.
rád považuji buňku za samostatné město, kde je jádro hlavním městem, mitochondrie je elektrárna a tak dále. Ale pak máte své pracovníky, dopravní systém a samotnou strukturu buněčného města, které jsou vyrobeny z bílkovin – které jsou zase vyrobeny z aminokyselin.,
složitost proteinové struktury je určena její sekvencí aminokyselin a chemickou povahou jejich postranních řetězců s proměnnou skupinou. MCAT vyžaduje pochopení povahy polárních a nepolárních bočních řetězců a kroucení a konformací způsobených hydrofobními a hydrofilními interakcemi
a ano, měli byste si zapamatovat každou aminokyselinu pro MCAT. To zahrnuje postranní řetězec, celé jméno, název 3 písmen a zkratku jednoho písmena. Ale ne jen držet slova a struktury na kartičky doufat, že ji vynutit do paměti., Musíte aktivně řešit každou aminokyselinu individuálně.
Pro rychlé referenční list ke stažení můj zdarma Aminokyseliny tahák Studijní Příručka
- vypsat celé jméno
- Nakreslit aminokyseliny struktury a proměnné skupiny
- vypsat 3-písmeno a jedno písmeno zkratky
- Verbalizovat něco, co je jedinečné o tento specifický postranní řetězec – nahlas! Čím zábavnější a bláznivější je spojení, tím snadněji si to zapamatujete.,
- Opakování pojmenování/kreslení proces, jakmile HNED
- Opakovat každý týden, dokud se nebudete cítit PLNÁ s touto informací
Základní Struktura Aminokyselin
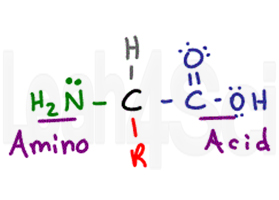 aminokyselina dostane jeho jméno od jeho dvě základní funkční skupiny. Aminokyselina má centrální chirální uhlík nazývaný alfa uhlík (černý). K centrálnímu uhlíku máte atom vodíku (šedý), aminoskupinu nebo skupinu NH2 (zelená) a karboxylovou skupinu COOH (fialová). Nakonec máme skupinu R (červená), což je variabilní postranní řetězec.,
aminokyselina dostane jeho jméno od jeho dvě základní funkční skupiny. Aminokyselina má centrální chirální uhlík nazývaný alfa uhlík (černý). K centrálnímu uhlíku máte atom vodíku (šedý), aminoskupinu nebo skupinu NH2 (zelená) a karboxylovou skupinu COOH (fialová). Nakonec máme skupinu R (červená), což je variabilní postranní řetězec.,
existuje 20 různých aminokyselin, které se vyznačují jedinečnými postranními řetězci. Pohybují se od jednoduchého atomu vodíku (glycin) až po komplexní 2-Kruhový rezonující aromatický systém (tryptofan).
Zatímco plně-neutrální verze výše je, jak většina studentů aminokyselin, a formulář použijeme v tomto článku, mějte na paměti, že to je technicky nesprávné.
Aminokyseliny v Zwitterion Formulář
Od karboxylové skupiny je kyselé a amino skupiny základní, dva bude existovat jako zwitterion v jejich konjugované nabité formy ve fyziologické pH., Více o zwitterion a aminokyselinových nábojích v mém dalším článku (odkaz na následující).
jeden konečný koncept, než rozložíme jednotlivé aminokyseliny, a to je 3-dimenzionální proteinová struktura. V biologické struktuře systému určuje funkci, takže pochopení vlastností aminokyselin je klíčem k pochopení struktury a nakonec funkce bílkovin.
primární struktura 3-D proteinu
prvním a důležitějším determinačním faktorem proteinové struktury je sekvence aminokyselin., Pokud je polypeptidový řetězec připojen v jiném pořadí, získáte velmi odlišnou celkovou strukturu.
sekundární struktura 3D proteinu
sekundární struktura pochází z páteřních vodíkových vazebných interakcí. Peptidová vazba mění každou bývalou karboxylovou a aminoskupinu na funkční skupinu amidů. Sekundární struktura alfa helix a beta skládaný listy pocházejí z vodíkové vazby mezi částečně záporný kyslík karbonylu a částečně kladný vodík na dusíku.,
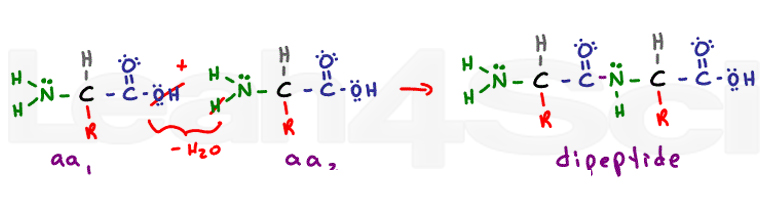
Terciární Struktura 3-D Protein
terciární struktura je místo, kde skutečná 3-dimenzionální skládací, je představen, a je to poprvé, všimnete si, boční řetězce interakcí. To je místo, kde jsou kritické znalosti a porozumění aminokyselinovým postranním řetězcům.
dovolte mi, abych se opakoval, terciární struktura je poprvé, kdy uvidíte variabilní interakce postranního řetězce R-skupiny na polypeptidovém řetězci. Mnoho studentů to zaměňuje se sekundární strukturou, což jsou pouze páteřní interakce.,
Kvartérní Struktura 3-D Multi-Polypeptid Bílkoviny
Kvartérní struktura se vztahuje k proměnné skupiny interakce mezi různými polypeptidy tvoří jeden větší bílkovin.
kvartérní struktury se nenacházejí v každém proteinu. Pokud protein obsahuje pouze jeden aminokyselinový pramen, pak nejvyšší úroveň skládání je jeho terciární struktura. Nicméně, pokud je protein tvořen více polypeptidovými podjednotkami, pak kvartérní struktura je to, co drží různé polypeptidy dohromady.,
Nyní, když pochopíte význam charakteristik postranního řetězce, pojďme se ponořit do aminokyselin. Mějte na paměti, že od rodičů amino a karboxylové skupiny jsou „busy“ s primární/sekundární struktury, NEJSOU analyzovány při studiu side-chain vlastnosti a charakteristiky.
to znamená, že ignorujete jakoukoli potenciální polaritu na karboxylových i aminoskupinách a díváte se pouze na postranní řetězce.
nepolární Hydrofobní Aminokyseliny
Hydrofobní, jak název napovídá, je hydro – voda, fobií – strachu., Hydrofobní aminokyseliny mají ve svých bočních řetězcích malou nebo žádnou polaritu. Nedostatek polarity znamená, že nemají žádný způsob interakce s vysoce polárními molekulami vody, což z nich dělá strach z vody.
ve vašich variabilních skupinách aminokyselin se objeví pouze pět atomů: H, C, N, O a s.
zvažte polaritu pouze tehdy, pokud máte N, O, S jako „většinový“ faktor. Upozorním na to, jak k nim dojde. Pokud však vidíte pouze Cs a Hs, měli byste automaticky rozpoznat aminokyselinu, která se bojí vody.,
GlycineGlyG
Glycin je jedinečná aminokyselina v tom, že ve skutečnosti nemá skupinu R. Když si myslíte, že ‚variabilní R skupina,‘ měli byste myslet na uhlík připojený k jiným atomům. Ale glycin má pouze vodík v poloze postranního řetězce. Vzhledem k tomu, že glycin má 2 atomy vodíku, každý jeden na nadřazeném a bočním řetězci, je to jediná symetrická a tedy achirová aminokyselina. Vzhledem k tomu, že vodík je nepolární, glycin je hydrofobní aminokyselina. Vodíkový postranní řetězec činí glycin nejmenší aminokyselinou.,
AlanineAlaA
alanin je jednoduchá aminokyselina, která má jako postranní řetězec pouze methylovou nebo CH3 skupinu. Protože nevidíte nic jiného než uhlík a vodík, alanin je nepolární hydrofobní aminokyselina. Je důležité si uvědomit, že se jedná o velmi malou aminokyselinu a je schopna být „zaklíněna“ do těsných smyček nebo řetězců.
ValineValV
valin je další jednoduchá aminokyselina s pouze isopropylovou proměnnou skupinou. Stejně jako alanin nevidíme nic jiného než uhlík a vodík, což z valinu činí nepolární hydrofobní aminokyselinu.,
LeucineLeuL
leucin poznáte tak, že má stejnou proměnnou skupinu jako valin, ale s extra skupinou CH2. Nebo můžete jednoduše rozpoznat jeho postranní řetězec isobutyl.
Podívejte se na toto video, Pokud nejste obeznámeni s rozvětvenými bočními řetězci, jako je isopropyl nebo sec-butyl. Protože leucin má jen Cs a Hs, je to voda, která se bojí nepolární aminokyseliny.
IsoleucineIleI
isoleucin, jak název napovídá, je izomer leucinu. Rozdíl je umístění CH3 pro SEC-butyl spíše než isobutyl boční řetězec. Stejně jako jeho izomer je isoleucin nepolární a hydrofobní.,
MethionineMetM
methionin je první potenciálně složitá aminokyselina. Je to boční řetězec obsahuje většinou Cs a Hs, ale s vloženým atomem síry. I když si možná myslíte, že je hydrofilní, věnujte pozornost umístění atomu síry. Síra, vložená do řetězce a připojená pouze k atomům uhlíku, je částečně „skrytá“ z vnějšího prostředí.
i když nemusíte znát hodnoty elektronegativity pro MCAT, pomáhá pochopit, že S = 2.58 A C = 2.55. Vzhledem k tomu, že rozdíl v elektronegativitě je menší než 0,5, na této straně není polarita.,
musíte také rozpoznat methionin jako počáteční kodon AUG v RNA překladu na proteiny.
Fenylalanineff
, který vám pomůže zapamatovat si, že fenylalanin je F nezapomeňte, že “ ph „je vyslovováno jako „F“. Nemíchejte to S P proline.
věnujte pozornost struktuře fenylalaninu. Má jednu uhlíkovou skupinu s připojeným benzenovým kroužkem. Fenyl je název pro substituent benzenu a tato molekula má benzen (fenyl) připojený ke struktuře alaninu. Vzhledem k tomu, že fenylalanin nemá ve svém aromatickém postranním řetězci nic jiného než Cs a Hs, je nepolární a hydrofobní.,
Tryptofantrpw
toto je složité. Všimněte si N-H v tomto bočním řetězci. N-H by měl být polární a schopný vodíkové vazby. Existují však dva důvody, proč je tato aminokyselina stále nepolární a hydrofobní.
- skupina N-H je malá část velmi velkého bočního řetězce.
- Podívejte se pozorně na dusík a co je důležitější, na jeho osamělé páry. Elektrony dusíku jsou nedílnou součástí konjugované aromaticity pro tryptofanový postranní řetězec., Jinými slovy, myslete na jeho elektrony jako na „příliš rozptýlené“ rezonancí, abyste věnovali velkou pozornost vnějšímu vodnímu prostředí.
MCAT vyžaduje, abyste si uvědomili, že se jedná o velkou a objemnou aminokyselinu. Ale protože je to zkouška s více možnostmi výběru, můžete si jednoduše zapamatovat, že tryptofan je jediná aminokyselina se dvěma tavenými kroužky.
Ve skutečnosti je to tak velká, že může VÝLET (trp) přes sebe a křičet Waaaaaa (W)
(Poznámka na mnemotechnické pomůcky: vtipnější, divnější, nebo špinavější mnemotechnická pomůcka, tím větší je pravděpodobnost, budete si to pamatovat. Mějte to na paměti pro med-school.,)
ProlineProP
Proline je jedinečná aminokyselina, protože je jediná, která začleňuje páteř do svého bočního řetězce. Boční řetězec proline je 3-uhlíkový řetězec, který se obepíná a váže se zpět k mateřské aminoskupině. To znamená, že na rozdíl od ostatních aminokyselin nemá prolin na svém dusíku atom vodíku, když je součástí polypeptidového řetězce.
nemůžete však zapomenout, že dusík není ve skutečnosti součástí proměnné skupiny, což znamená, že nemůže přispívat k žádné polaritě. Protože máme jen 3 skupiny CH2 k analýze, dostaneme nepolární hydrofobní postranní řetězec., Tato mateřská smyčka vytváří vyboulení a neumožňuje lineární řetězec obsahující prolin, což znamená, že jej často najdete ve smyčkách a na konci alfa šroubovice.
Polární Hydrofobní Aminokyseliny
*Toto je nepříjemné části, a v závislosti na tom, kde jste výzkum může najít následující rozděleny do kategorií jako polární nebo nepolární, hydrofilní nebo hydrofobní. Věnujte pozornost přítomnosti polárních skupin, které jsou malé ve srovnání s celkovou stranou, nebo velmi slabě polární, a proto hydrofobní.,
CysteineCysC
Cystein má mírně polární S-H, ale jeho polarita je tak mírné, že cystein je schopen správně komunikovat s vodou, což je hydrofobní.
cystein je velmi důležitá aminokyselina, pokud jde o terciární a kvartérní strukturu. Většina interakcí s postranním řetězcem zahrnuje polární / nabité interakce nebo nepolární Van Der Waals a londýnskou disperzi. Boční řetězec cysteinu je však schopen vytvořit disulfidový most, což je kovalentní vazba mezi 2 atomy síry oxidací bočního řetězce a odstraněním 2 atomů vodíku., Tato kovalentní vazba je mnohem silnější a trvalejší oproti standardnímu terciární a kvartérní interakce.
To je také příčinou experimentální chyby při určování velikosti/délky bílkovin pro proteiny s více podjednotkami.
TyrosineTyrY
někteří studenti to vidí jako Oh unikající z pneumatiky (tyr).
podívejte se blíže na tyrosin. Co vidíš? Vypadá to jako aromatický fenylalanin se skupinou OH v poloze para (ortho/meta/para 2nd video).,
Na jedné straně máme velmi polární a hydrogen-bond schopný OH skupinu, ale na druhou stranu, OH je malé ve srovnání s velikostí benzyl skupina (CH2-fenyl). Tento hlavolam je běžným zdrojem zmatku, ale pokud tomu rozumíte, poznáte, že tyrosin, zatímco polární, je stále hydrofobní aminokyselinou.
polární hydrofilní aminokyseliny
hydrofilní, jak název napovídá, pocházejí z hydro-vody a filiální lásky.
polarita pochází z rozdílu 0,5-1,9 v elektronegativitě mezi vázanými atomy., I když nemusíte znát tyto hodnoty pro MCAT, měli byste si uvědomit, že polární vazby budou existovat, když N A O budou vázány na atomy bez uhlíku.
rozdíl elektronegativity stačí k vytvoření mírného oddělení náboje nebo polarity. A protože stejně jako přitahuje, tyto částečně nabité skupiny budou přitahovány k opačně nabitým nebo částečně nabitým skupinám, jako je voda. Tyto skupiny budou otáčet polypeptidovým řetězcem, aby interagovaly mezi sebou a vodou.
hydrofobní skupiny se od těchto bočních řetězců odvrátí.,
Serinesery
myslete na serin jako na alanin s připojenou skupinou OH. Na rozdíl od tyrosinu je OH většinou v této molekule a jeho polarita stačí k ovlivnění celé skupiny. Díky tomu je řada polární a velmi hydrofilní.
Threoninethrthrt
existuje několik způsobů, jak se podívat na tuto skupinu. Můžete si to myslet jako serin s extra methylovou skupinou, nebo jako valin, ale s OH nahrazující jednu z methylových skupin. Vzpomínám si, že THREEonine má 3 různé skupiny: CH, CH3, a OH.
stejně jako serin je tato proměnná skupina polární a hydrofilní.,
Asparaginasnn
zkuste to: Slur svou řeč, jak říkáte „asparagin“ opravdu rychle. Zní to, jako byste říkal … N, což je, jak si pamatuji zkratku 3-letter pro tuto aminokyselinu. NH2 na konci této molekuly vás nutí myslet na „základnu“, ale podívejte se na souseda. NH2 poblíž karbonylu tvoří amid, který nemá rád působit jako kyselina nebo báze za standardních fyziologických podmínek. Nicméně, s částečnými náboji a schopností h-lepení jak u karbonylového kyslíku, tak u skupin NH2, získáme polární hydrofilní aminokyselinu.,
GlutamineGlnQ
myslím na obě „glut“ aminokyseliny jako gluttony, které „spotřebovaly“ další skupinu CH2. Glutamin má stejnou strukturu jako asparagin, ale s extra žravým CH2 v řetězci. Stejně jako asparagin je polární a hydrofilní.
kyselé a bazické aminokyseliny postranní řetězce
kyselost a bazicita aminokyselin je dalším zdrojem zmatku mezi studenty. Pokud to začíná jako kyselina, stane se základem? Jak najdu obvinění? A tak dále.
zde je trik: karboxylová kyselina v postranním řetězci vám dá kyselou aminokyselinu., Když je karboxylová skupina deprotonována, dostanete konjugovanou základní sůl. Takže pokud vidíte, sůl verzi karboxylový postranní řetězec, i když je TECHNICKY ‚konjugovaná báze,‘ budeme jednoduše odkazují na to jako sůl verzi kyselé aminokyseliny. Totéž pro základnu. Podívejte se na ‚non-rozptylovat‘ atomy dusíku v postranním řetězci.
kyselé aminokyseliny
kyselé aminokyseliny by měly vypadat velmi dobře ve srovnání s asparaginem a glutaminem. A to proto, že všechno o nich je stejné, s výjimkou terminálové funkční skupiny., Amidy (diskutované výše) jsou polární, ale pokud je NH2 vyměněn za skupinu OH, dostanete kyselou karboxylovou skupinu.
Kyselina Asparagová / AspartateAspD
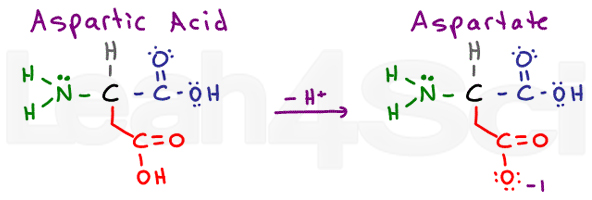
kyselina Asparagová odkazuje na protonované kyselé formě aminokyselin. Při deprotonaci často uvidíte konjugovanou základní sůl označovanou jako aspartát. Toto je standardní nomenklatura pro karboxylové kyseliny.
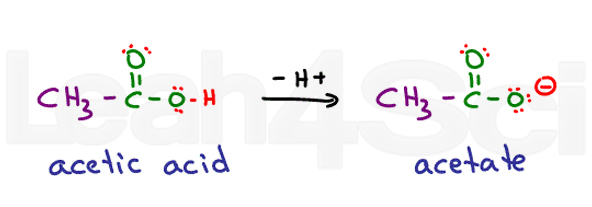
myslete na kyselinu ethanovou. Jeho běžným názvem je kyselina octová. Při deprotonaci dostanete acetát., Kyseliny jsou ve vodě velmi stabilní, protože jsou částečně nabité ve své protonované formě a plně nabité ve své deprotonované formě. Díky tomu jsou vysoce hydrofilní.
kyselina glutamová / GlutamateGluE
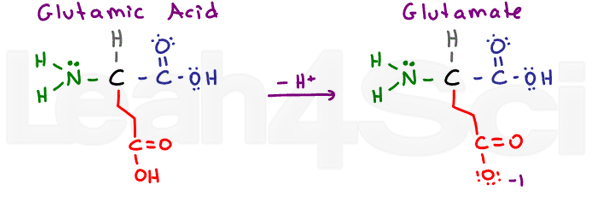
opět máme aminokyselinu „glutton“ s extra skupinou CH2. Kyselina glutamová se týká protonované kyselé formy a glutamát se týká deprotonované konjugované báze/formy soli.
stejně jako kyselina asparagová je kyselina glutamová ve vodě velmi stabilní a tím hydrofilní.,
základní aminokyseliny
základní aminokyseliny obsahují atom dusíku s osamělým elektronovým párem schopným napadnout atom vodíku. Když je základní aminokyselina vystavena nízkému (kyselému) pH, uchopí jeden z volných protonů v roztoku a vytvoří sůl kyseliny konjugované. Ty jsou snadno rozpoznatelné pozitivním dusíkem v bočním řetězci. Na rozdíl od kyselých aminokyselin, neexistují žádné „běžně používané názvy“ pro zapamatování těchto konjugovaných solí.
LysineLysK
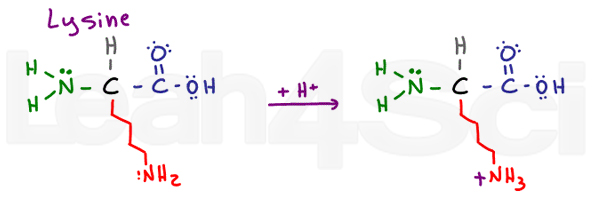
Lysin je jednoduchá základní aminokyselina., Navzdory dlouhému a potenciálně hydrofobnímu řetězci má na konci základní NH2. Ve své základní deprotonované formě je lysin neutrální a hydrofilní; pokud se však vyskytne ve fyziologickém pH, lysin vyzvedne H+ z roztoku a vytvoří sůl NH3+. Soli jsou nabité, a proto rozhodně hydrofilní,
ArginineArgR
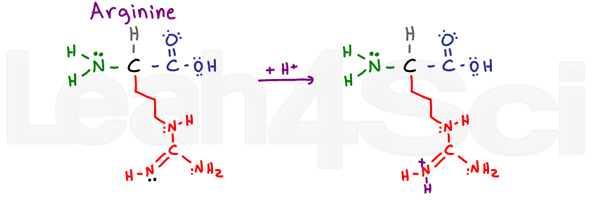
Arginin je matoucí a dělá mi říci, ARGh nebo R pro krátké. Proč? Základní část této proměnné skupiny se skládá z NH, C=N-H a NH2.,
2 single-vázané atomy dusíku mohou používat své osamělé páry rezonovat s uhlíku a dvakrát vázán atom dusíku. Díky tomu jsou jejich elektrony nedostupné pro působení jako základny. Nicméně, double-vázaný dusík používá jeho pí vazba rezonovat, takže jeho volné elektronové páry (na obrázku v černém), aby jednala jako základní dusíku na tuto skupinu.
Argh!
HistidineHisH

Histidin je další složité základnu pro stejný důvod jako arginin. Který dusík je základní? Podívejte se na kresbu zde, zejména na osamělé páry na atomech dusíku 2., Histidin kruh je heterocyklická aromatická sloučenina. Horní atom dusíku nemá vazbu pi. To znamená, že musí používat své osamělé páry k účasti na rezonanci.
spodní atom dusíku má již rezonující vazbu pi. To ponechává jeho osamělé elektrony (znázorněné v černé barvě) volné k uchopení protonu, což z něj činí základní atom.
závěrem
Aminokyseliny jsou základní složkou biologických struktur a na vaše pochopení biologie a biochemie na MCAT., A tak, jak se pokusíte zapamatovat si vše, co o těchto 20 aminokyselin, je důležité, aby také pochopit, proč mají polární a nepolární aminokyseliny, co dělá skupina proměnných hydrofobní nebo hydrofilní, a samozřejmě, logika protonované/deprotonated kyselé a bazické aminokyseliny.