 Aminosäuren sind die Bausteine von Lebewesen. Lange Aminosäureketten bilden Proteine, aus denen wiederum viele strukturelle und funktionelle Zellkomponenten bestehen.
Aminosäuren sind die Bausteine von Lebewesen. Lange Aminosäureketten bilden Proteine, aus denen wiederum viele strukturelle und funktionelle Zellkomponenten bestehen.
Ich denke gerne an die Zelle als eine in sich geschlossene Stadt, in der der Kern die Hauptstadt ist, die Mitochondrien das Kraftwerk sind und so weiter. Aber dann haben Sie Ihre Arbeiter, Ihr Transportsystem und die Struktur der Zellstadt, die alle aus Proteinen bestehen – die wiederum aus Aminosäuren bestehen.,
Die Komplexität einer Proteinstruktur wird durch ihre Aminosäuresequenz und die chemische Natur ihrer variablen Gruppenseitenketten bestimmt. Das MCAT erfordert das Verständnis der Natur polarer und unpolarer Seitenketten und der Verdrehung und Konformationen, die durch hydrophobe und hydrophile Wechselwirkungen
verursacht werden, und ja, Sie sollten sich jede Aminosäure für das MCAT merken. Dazu gehören die Seitenkette, der vollständige Name, der Name mit 3 Buchstaben und die Abkürzung mit einem Buchstaben. Aber kleben Sie die Wörter und Strukturen nicht einfach auf Karteikarten, in der Hoffnung, sie in Ihr Gedächtnis zu zwingen., Sie müssen jede Aminosäure einzeln aktiv angehen.
Für eine schnelle Referenzliste Laden Sie meinen kostenlosen Aminosäure-Spickzettel herunter Studienführer
- Schreiben Sie den vollständigen Namen
- Zeichnen Sie die Aminosäurestruktur und die variable Gruppe
- Schreiben Sie die Abkürzungen mit 3 Buchstaben und einzelnen Buchstaben
- Verbalisieren Sie etwas Einzigartiges über diese spezifische Seitenkette-laut! Je lustiger und verrückter die Verbindung ist, desto leichter werden Sie sich daran erinnern.,
- Den Benennungs – / Zeichenvorgang sofort einmal wiederholen
- wöchentlich wiederholen, bis Sie sich mit diesen Informationen FEST fühlen
Die Grundstruktur einer Aminosäure
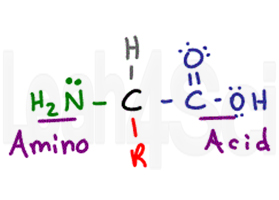 Die Aminosäure erhält ihren Namen von ihren beiden primären Funktionsgruppen. Die Aminosäure hat einen zentralen chiralen Kohlenstoff, den Alpha-Kohlenstoff (schwarz). An den zentralen Kohlenstoff gebunden haben Sie ein Wasserstoffatom (grau), eine Amino-oder NH2-Gruppe (grün) und eine Carbonsäure-COOH-Gruppe (lila). Schließlich haben wir die R-Gruppe (rot), die eine variable Seitenkette.,
Die Aminosäure erhält ihren Namen von ihren beiden primären Funktionsgruppen. Die Aminosäure hat einen zentralen chiralen Kohlenstoff, den Alpha-Kohlenstoff (schwarz). An den zentralen Kohlenstoff gebunden haben Sie ein Wasserstoffatom (grau), eine Amino-oder NH2-Gruppe (grün) und eine Carbonsäure-COOH-Gruppe (lila). Schließlich haben wir die R-Gruppe (rot), die eine variable Seitenkette.,
Es gibt 20 verschiedene Aminosäuren, die sich durch ihre einzigartigen Seitenketten auszeichnen. Sie reichen von einem einfachen Wasserstoffatom (Glycin) bis zu einem komplexen 2-Ring-resonanzaromatischen System (Tryptophan).
Während die völlig neutrale Version oben ist, wie die meisten Studenten Aminosäuren studieren, und die Form, die wir in diesem Artikel verwenden werden, bedenken Sie, dass dies technisch falsch ist.
Aminosäure in Zwitterionform
Da die Carboxylgruppe sauer und die Aminogruppe basisch ist, existieren die beiden als Zwitterion in ihren konjugierten geladenen Formen im physiologischen pH-Wert., Mehr zu Zwitterion und Aminosäureladungen in meinem nächsten Artikel (Link zu folgen).
Ein endgültiges Konzept, bevor wir die einzelnen Aminosäuren abbauen, und das ist die 3-dimensionale Proteinstruktur. In einem biologischen System bestimmt die Struktur die Funktion, daher ist das Verständnis der Aminosäureeigenschaften der Schlüssel zum Verständnis der Struktur und letztendlich der Proteinfunktion.
Primärstruktur eines 3-D-Proteins
Der erste und wichtigere Bestimmungsfaktor der Proteinstruktur ist die Aminosäuresequenz., Wenn die Polypeptidkette in einer anderen Reihenfolge befestigt ist, erhalten Sie eine sehr unterschiedliche Gesamtstruktur.
Sekundärstruktur eines 3-D-Proteins
Die Sekundärstruktur stammt aus Rückgrat-Wasserstoffbindungs-Wechselwirkungen. Die Peptidbindung verwandelt jede ehemalige Carboxyl – und Aminogruppe in eine Amidfunktionsgruppe. Die Sekundärstruktur von Alpha-Helix-und Beta-Faltenblättern ergibt sich aus der Wasserstoffbindung zwischen dem teilweise negativen Sauerstoff auf dem Carbonyl und dem teilweise positiven Wasserstoff auf dem Stickstoff.,
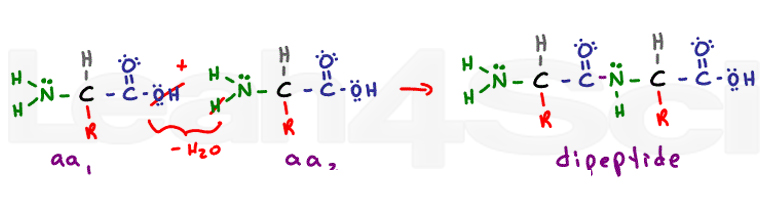
Tertiärstruktur eines 3-D-Proteins
In der Tertiärstruktur wird die reale 3-dimensionale Faltung eingeführt, und dies ist das erste Mal, dass Sie Seitenketteninteraktionen bemerken. HIER sind Wissen und Verständnis von Aminosäure-Seitenketten entscheidend.
Lassen Sie mich wiederholen, Tertiärstruktur ist das erste Mal, dass Sie variable R-Gruppen-Seitenketteninteraktionen in der Polypeptidkette sehen. Viele Schüler verwechseln dies mit sekundärer Struktur, die nur Rückgrat-Interaktionen ist.,
Quaternäre Struktur eines 3-D-Multipolypeptidproteins
Quaternäre Struktur bezieht sich auf die variablen Gruppeninteraktionen zwischen verschiedenen Polypeptiden, um ein einzelnes größeres Protein zu bilden.
Quartäre Strukturen finden sich nicht in jedem Protein. Wenn das Protein nur einen einzelnen Aminosäurestrang enthält, ist die höchste Faltung seine tertiäre Struktur. Wenn das Protein jedoch aus mehreren Polypeptiduntereinheiten besteht, hält die quartäre Struktur die verschiedenen Polypeptide zusammen.,
Nachdem Sie nun die Bedeutung der Seitenketteneigenschaften verstanden haben, lassen Sie uns in Aminosäuren eintauchen. Denken Sie daran, dass die übergeordneten Amino-und Carboxylgruppen, da sie mit der Primär – /Sekundärstruktur „beschäftigt“ sind, BEI der Untersuchung der Seitenketteneigenschaften und-eigenschaften NICHT analysiert werden.
Dies bedeutet, dass Sie jede mögliche Polarität sowohl bei der Carboxyl-als auch bei der Aminogruppe ignorieren und NUR die Seitenketten betrachten.
Unpolare hydrophobe Aminosäuren
Hydrophob, wie der Name schon sagt, ist hydro-Wasser, phobisch-fearing., Hydrophobe Aminosäuren haben wenig oder keine Polarität in ihren Seitenketten. Der Mangel an Polarität bedeutet, dass sie keine Möglichkeit haben, mit hochpolaren Wassermolekülen zu interagieren, wodurch sie Wasser fürchten.
Es gibt nur fünf Atome, die in Ihren Aminosäure-Variablengruppen erscheinen: H, C, N, O und S.
Berücksichtigen Sie die Polarität nur, wenn Sie N, O, S als „Mehrheitsfaktor“ haben. Ich werde darauf hinweisen, wie sie auftreten. Wenn Sie jedoch nur Cs und Hs sehen, sollten Sie automatisch eine wasserfressende Aminosäure erkennen.,
GlycineGlyG
Glycin ist eine einzigartige Aminosäure, da es nicht wirklich eine R-Gruppe hat. Wenn Sie „variable R-Gruppe“ denken, sollten Sie an Kohlenstoff denken, der an andere Atome gebunden ist. Aber Glycin hat nur einen Wasserstoff an seiner Seitenkettenposition. Da Glycin 2 Wasserstoffatome hat, jeweils eines an der Eltern-und Seitenkette, ist es die einzige symmetrische und damit achirale Aminosäure. Da Wasserstoff unpolar ist, ist Glycin eine hydrophobe Aminosäure. Die Wasserstoffseitenkette macht Glycin zur kleinsten Aminosäure.,
AlanineAlaA
Alanin ist eine einfache Aminosäure, die nur eine Methyl-oder CH3-Gruppe als Seitenkette hat. Da Sie nur Kohlenstoff und Wasserstoff sehen, ist Alanin eine unpolare hydrophobe Aminosäure. Es ist wichtig zu erkennen, dass dies eine sehr kleine Aminosäure ist und in engen Schleifen oder Ketten „eingeklemmt“ werden kann.
ValineValV
Valin ist eine weitere einfache Aminosäure mit nur einer isopropylvariablen Gruppe. Genau wie Alanin sehen wir nur Kohlenstoff und Wasserstoff, was Valin zu einer unpolaren hydrophoben Aminosäure macht.,
LeucineLeuL
Sie können Leucin als dieselbe variable Gruppe wie Valin erkennen, jedoch mit einer zusätzlichen CH2-Gruppe. Oder Sie erkennen einfach seine Isobutylseitenkette.
Sehen Sie sich dieses Video an, wenn Sie mit verzweigten Seitenketten wie Isopropyl oder Sec-Butyl nicht vertraut sind. Da Leucin nur Cs und Hs hat, ist es eine wasserfressende unpolare Aminosäure.
IsoleucineIleI
Isoleucin ist, wie der Name schon sagt, ein Isomer von Leucin. Der Unterschied ist die Platzierung des CH3 für eine sec-Butyl statt einer Isobutylseitenkette. Genau wie sein Isomer ist Isoleucin unpolar und hydrophob.,
MethionineMetM
Methionin ist die erste potenziell gefährliche Aminosäure. Es ist Seitenkette enthält meist Cs und Hs, aber mit einem eingebetteten Schwefelatom. Während Sie vielleicht denken, dass es hydrophil ist, achten Sie sorgfältig auf die Position des Schwefelatoms. Eingebettet in die Kette und nur an Kohlenstoffatomen befestigt, ist Schwefel teilweise vor der äußeren Umgebung „verborgen“.
Obwohl Sie keine Elektronegativitätswerte für den MCAT kennen müssen, hilft es zu verstehen, dass S = 2.58 und C = 2.55. Da der Unterschied in der Elektronegativität kleiner als 0,5 ist, gibt es KEINE Polarität auf dieser Sidechain.,
Sie müssen auch Methionin als Start-Codon AUG in RNA-Übersetzung zu Proteinen erkennen.
PhenylalaninePheF
Um Ihnen zu helfen, sich daran zu erinnern, dass Phenylalanin F ist Denken Sie daran, dass “ ph “ als “ F “ ausgesprochen wird. Verwechseln Sie das nicht mit P für Proline.
achten Sie auf die Struktur von Phenylalanin. Es hat eine einzelne Kohlenstoffgruppe mit einem angebrachten Benzolring. Phenyl ist der Name für einen Benzolsubstituenten, und dieses Molekül hat ein Benzol (Phenyl), das an die Struktur von Alanin gebunden ist. Da Phenylalanin in seiner aromatischen Seitenkette nur Cs und Hs enthält, ist es unpolar und hydrophob.,
TryptophanTrpW
Dies ist eine knifflige Sache. Beachten Sie die N-H in dieser Seitenkette. N-H sollte polar und in der Lage sein, Wasserstoff zu binden. Es gibt jedoch zwei Gründe, warum diese Aminosäure immer noch unpolar und hydrophob ist.
- Die N-H-Gruppe ist ein winziger Teil der sehr großen Seitenkette.
- Schauen Sie sich Stickstoff und vor allem seine einsamen Paare genau an. Stickstoffelektronen sind integraler Bestandteil der konjugierten Aromatizität für die Tryptophan-Seitenkette., Mit anderen Worten, denken Sie an seine Elektronen als „zu abgelenkt“ durch Resonanz, um der äußeren Wasserumgebung viel Aufmerksamkeit zu schenken.
Bei der MCAT müssen Sie erkennen, dass es sich um eine große und sperrige Aminosäure handelt. Da es sich jedoch um eine Multiple-Choice-Prüfung handelt, können Sie sich einfach merken, dass Tryptophan die EINZIGE Aminosäure mit ZWEI verschmolzenen Ringen ist.Tatsächlich ist es so groß, dass es über sich selbst stolpern und Waaaaaa (W) schreien kann
(Hinweis zur Mnemonik: Je lustiger, seltsamer oder schmutziger die Mnemonik ist, desto wahrscheinlicher werden Sie sich daran erinnern. Denken Sie daran für die Med-School.,)
ProlineProP
Prolin ist eine einzigartige Aminosäure, da es DIE EINZIGE ist, die das Rückgrat in seine Seitenkette integriert. Die Proline-Seitenkette ist eine 3-Kohlenstoff-Kette, die sich um die übergeordnete Aminogruppe schlängelt und sie an diese zurückbindet. Dies bedeutet, dass Prolin im Gegensatz zu den anderen Aminosäuren KEIN Wasserstoffatom auf seinem Stickstoff hat, wenn es Teil einer Polypeptidkette ist.
Sie können jedoch nicht vergessen, dass Stickstoff NICHT WIRKLICH Teil der Variablengruppe ist, was bedeutet, dass er keine Polarität beitragen kann. Da wir nur 3 CH2-Gruppen zur Analyse haben, erhalten wir eine unpolare hydrophobe Seitenkette., Diese Elternschleife erzeugt eine Ausbuchtung und erlaubt nicht, dass eine Proline-haltige Kette linear ist, was bedeutet, dass Sie sie oft in Schleifen und am Ende einer Alpha-Helix finden.
Polare hydrophobe Aminosäuren
*Dies ist ein klebriger Abschnitt, und je nachdem, wo Sie recherchieren, finden Sie die folgenden Kategorien polar oder unpolar, hydrophil oder hydrophob. Achten Sie auf das Vorhandensein von polaren Gruppen, die im Vergleich zur Gesamtseitenhülle klein oder sehr schwach polar und daher hydrophob sind.,
CysteineCysC
Cystein hat ein leicht polares S-H, aber seine Polarität ist so mild, dass Cystein nicht richtig mit Wasser interagieren kann, was es hydrophob macht.
Cystein ist eine sehr wichtige Aminosäure, wenn es um tertiäre und quartäre Struktur geht. Die meisten Seitenketteninteraktionen umfassen polare / geladene Interaktionen oder unpolare Van Der Waals-und London-Dispersion. Die Seitenkette von Cystein ist jedoch in der Lage, eine Disulfidbrücke zu bilden, bei der es sich um kovalente Bindungen zwischen 2 Schwefelatomen durch Seitenkettenoxidation und Entfernung von 2 Wasserstoffatomen handelt., Diese kovalente Bindung ist viel stärker und dauerhafter im Vergleich zu den Standard-tertiären und quartären Wechselwirkungen.
Dies ist auch die Ursache für experimentelle Fehler bei der Bestimmung der Proteingröße / – länge für Proteine mit mehreren Untereinheiten.
TyrosineTyrY
Einige Schüler sehen dies als OH aus einem Reifen (tyr) undicht.
Schauen Sie sich Tyrosin genau an. Was siehst du? Es sieht aus wie das aromatische Phenylalanin mit einer OH-Gruppe an der Para-Position (ortho/meta/para 2.Video).,
Einerseits haben wir eine sehr polare und wasserstoffbindungsfähige OH-Gruppe, andererseits ist das OH im Vergleich zur Größe der Benzylgruppe (CH2-phenyl) winzig. Dieses Rätsel ist eine häufige Quelle der Verwirrung, aber wenn Sie dies verstehen, werden Sie erkennen, dass Tyrosin, während es polar ist, immer noch eine hydrophobe Aminosäure ist.
Polare hydrophile Aminosäuren
Hydrophil, wie der Name schon sagt, kommt von Hydrowasser und philisch – liebend.
Polarität kommt von einem 0,5-1,9 Unterschied in der Elektronegativität zwischen gebundenen Atomen., Obwohl Sie diese Werte für die MCAT nicht kennen müssen, sollten Sie erkennen, dass polare Bindungen bestehen, wenn N und O an Nicht-Kohlenstoffatome gebunden sind.
Die Elektronegativitätsdifferenz reicht aus, um eine leichte Trennung von Ladung oder Polarität zu erzeugen. Und da like like anzieht, werden diese teilweise geladenen Gruppen von entgegengesetzt geladenen oder teilweise geladenen Gruppen wie Wasser angezogen. Diese Gruppen verdrehen die Polypeptidkette, um miteinander und mit Wasser zu interagieren.
Hydrophobe Gruppen werden sich von diesen Seitenketten wegdrehen.,
Serineser
Stellen Sie sich Serin als Alanin mit einer OH-Gruppe vor. Im Gegensatz zu Tyrosin ist das OH die Mehrheit in diesem Molekül und seine Polarität reicht aus, um die gesamte Gruppe zu beeinflussen. Dies macht Serie polar und sehr hydrophil.
ThreonineThrT
Es gibt mehrere Möglichkeiten, diese Gruppe zu betrachten. Sie können es sich als Serin mit einer zusätzlichen Methylgruppe oder als Valin vorstellen, aber mit einem OH, das eine der Methylgruppen ersetzt. Ich erinnere mich an drei verschiedene Gruppen: CH, CH3 und OH.
Wie Serin ist diese variable Gruppe polar und hydrophil.,
asparagineasnnn
Versuchen Sie dies: Schlürfen Sie Ihre Rede, wie Sie sagen, ‚asparagine‘ wirklich schnell. Es hört sich so an, als würden Sie ALS…N sagen, so erinnere ich mich an die 3-Buchstaben-Abkürzung für diese Aminosäure. Das NH2 am Ende dieses Moleküls lässt Sie an „Base“ denken, aber schauen Sie sich seinen Nachbarn an. NH2 in der Nähe eines Carbonyls bildet ein Amid, das unter physiologischen Standardbedingungen nicht gerne als Säure oder Base wirkt. Mit Teilladungen und H-Bindungsfähigkeit sowohl an Carbonylsauerstoff ALS AUCH an NH2-Gruppen erhalten wir jedoch eine polare hydrophile Aminosäure.,
GlutamineGlnQ
Ich denke an beide „Glut“ – Aminosäuren als Gefäße, die eine zusätzliche CH2-Gruppe „konsumiert“ haben. Glutamin hat die gleiche Struktur wie Asparagin, aber mit einem extra gefräßigen CH2 in seiner Kette. Genau wie Asparagin ist es polar und hydrophil.
Saure und basische Aminosäure Seitenketten
Säure und Basizität in Aminosäuren ist eine weitere Quelle der Verwirrung unter den Studenten. Wenn es als Säure beginnt, wird es dann eine Base? Wie finde ich die Ladung? Und so weiter.
Hier ist der Trick: Eine Carbonsäure in der Seitenkette gibt Ihnen eine saure Aminosäure., Wenn eine Carboxylgruppe deprotoniert wird, erhalten Sie ein konjugiertes Basissalz. Wenn Sie also die Salzversion einer Carbonsäureseitenkette sehen, während sie TECHNISCH gesehen eine „konjugierte Base“ ist, werden wir sie einfach als Salzversion der sauren Aminosäure bezeichnen. Gleiches gilt für die Basis. Achten Sie auf „nicht abgelenkte“ Stickstoffatome in der Seitenkette.
Saure Aminosäuren
Die sauren Aminosäuren sollten im Vergleich zu Asparagin und Glutamin sehr vertraut aussehen. Und das liegt daran, dass alles an ihnen bis auf die Terminalfunktionsgruppe gleich ist., Amide (oben diskutiert) sind polar, aber wenn das NH2 gegen eine OH-Gruppe ausgetauscht wird, erhalten Sie eine saure Carboxylgruppe.
Asparaginsäure / Aspartataspd
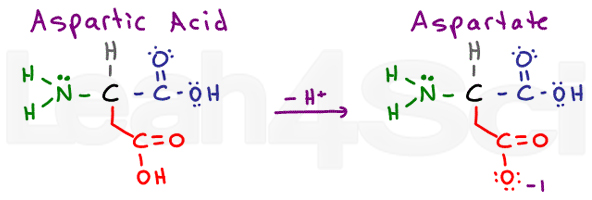
Asparaginsäure bezieht sich auf die protonierte saure Form der Aminosäure. Wenn Sie deprotoniert sind, sehen Sie oft das konjugierte Basissalz, das als Aspartat bezeichnet wird. Dies ist die Standardnomenklatur für Carbonsäuren.
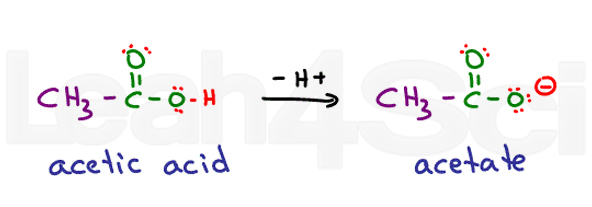
Denken ethanoic acid. Sein gebräuchlicher Name ist Essigsäure. Wenn Sie deprotoniert werden, erhalten Sie Acetat., Säuren sind in Wasser sehr stabil, da sie teilweise in ihrer protonierten Form geladen und in ihrer deprotonierten Form vollständig geladen sind. Dies macht sie sehr hydrophil.
Glutaminsäure / GlutamateGluE
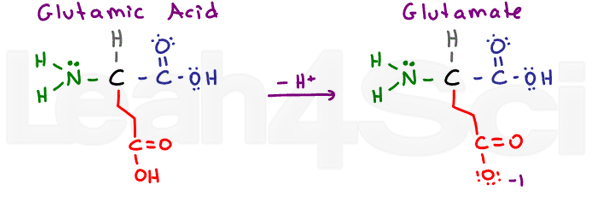
Wieder einmal haben wir eine ‚glutton‘ Aminosäure mit einer zusätzlichen CH2-Gruppe. Glutaminsäure bezieht sich auf die protonierte saure Form und Glutamat bezieht sich auf die deprotonierte Konjugatbase/Salzform.
Wie Asparaginsäure ist Glutaminsäure in Wasser sehr stabil und somit hydrophil.,
Basische Aminosäuren
Basische Aminosäuren enthalten ein Stickstoffatom mit einem einsamen Elektronenpaar, das ein Wasserstoffatom angreifen kann. Wenn eine basische Aminosäure einem niedrigen (sauren) pH-Wert ausgesetzt ist, greift sie eines der freien Protonen in Lösung, um ein konjugiertes Säuresalz zu bilden. Diese sind leicht an den positiven Stickstoff in der Seitenkette zu erkennen. Im Gegensatz zu den sauren Aminosäuren gibt es keine „häufig verwendeten Namen“, die man sich für diese Konjugatsalze merken kann.
Lysinel >
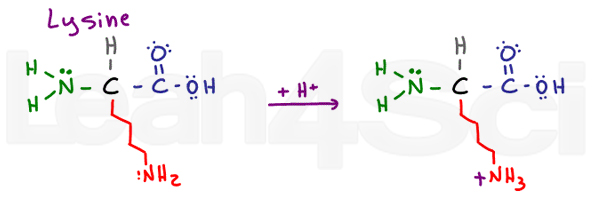
Lysin ist eine einfache basische Aminosäure., Trotz einer langen und potenziell hydrophoben Kette hat es am Ende ein grundlegendes NH2. In seiner grundlegenden deprotonierten Form ist Lysin neutral und hydrophil; Wenn es jedoch im physiologischen pH-Wert gefunden wird, nimmt Lysin ein H+ aus der Lösung auf, um ein NH3+ – Salz zu bilden. Salze sind geladen und daher definitiv hydrophil
ArginineArgR
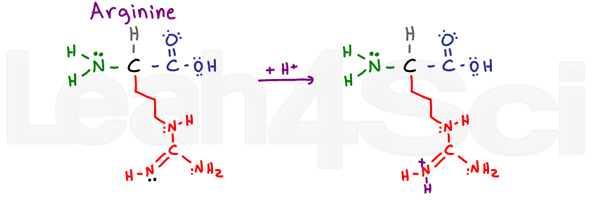
Arginin ist verwirrend und lässt mich kurz ARGh oder R sagen. Warum? Der Grundteil dieser Variablengruppe besteht aus einem NH, C=N-H und NH2.,
Die 2 einzeln gebundenen Stickstoffatome können ihre einsamen Paare verwenden, um mit dem Kohlenstoff und dem doppelt gebundenen Stickstoffatom in Resonanz zu treten. Dies macht ihre Elektronen NICHT VERFÜGBAR, um als Basis zu fungieren. Der doppelt gebundene Stickstoff verwendet jedoch seine pi-Bindung, um zu schwingen, und lässt sein freies einzelnes Paar (schwarz dargestellt) als basischen Stickstoff in dieser Gruppe wirken.
Argh!
HistidineHisH

Histidin ist eine weitere knifflige Basis aus dem gleichen Grund wie Arginin. WELCHER Stickstoff ist der grundlegende? Schauen Sie sich die Zeichnung hier an, insbesondere die einsamen Paare der 2 Stickstoffatome., Der Histidinring ist eine heterocyclische aromatische Verbindung. Das obere Stickstoffatom hat keine pi-Bindung. Dies bedeutet, dass es seine einsamen Paare verwenden muss, um an Resonanz teilzunehmen.
Das untere Stickstoffatom hat bereits eine resonante pi-Bindung. Dies lässt seine einsamen Elektronen (in schwarz gezeigt) frei, um ein Proton zu greifen, was dies zum Grundatom macht.
Zusammenfassend
Aminosäuren sind ein kritischer Bestandteil für biologische Strukturen und für Ihr Verständnis von Biologie und Biochemie am MCAT., Wenn Sie also versuchen, sich alles über diese 20 Aminosäuren zu merken, ist es wichtig, dass Sie auch verstehen, warum Sie polare und unpolare Aminosäuren haben, was die variable Gruppe hydrophob oder hydrophil macht, und natürlich die Logik hinter protonierten/deprotonierten sauren und basischen Aminosäuren.