de Volta para Escrever Estruturas de Lewis para as Moléculas
a fim de atender as exigências de valência normal, às vezes, é necessário ter mais de um vínculo, isto é, mais do que uma compartilhado par de elétrons entre dois átomos. Um caso em ponto é formaldeído, CH2O.a fim de fornecer carbono com quatro ligações nesta molécula, devemos considerar o carbono como formando duas ligações ao oxigênio, bem como um para cada um dos dois hidrogénios., Ao mesmo tempo, o átomo de oxigênio também é fornecido com os dois títulos de sua valência normal requer:
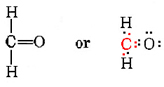
Note que todos os quatro elétrons compartilhados em carbono-oxigênio bond estão incluídos tanto no octeto de carbono e o octeto de oxigênio. Uma ligação envolvendo dois pares de elétrons é chamada de ligação dupla.ocasionalmente, as valências habituais dos átomos de uma molécula não nos dizem qual deve ser a estrutura do esqueleto., Por exemplo, no monóxido de carbono, CO, é difícil ver como um átomo de carbono (Valência habitual de 4) pode ser combinado com um único átomo de oxigênio (Valência habitual de 2). Em um caso como este, onde as valências parecem ser incompatíveis, a contagem de elétrons de Valência geralmente leva a uma estrutura que satisfaz a Regra do octeto. O carbono tem 4 elétrons de Valência e o oxigênio tem 6, para um total de 10. Queremos organizar estes 10 elétrons em dois octetos, mas dois grupos separados de 8 elétrons precisariam de 16 elétrons., Somente compartilhando 16-10, ou 6, elétrons (de modo que esses 6 elétrons são parte de cada octeto, e, com efeito, contam duas vezes) podemos satisfazer a Regra do octeto. Isso leva a uma estrutura
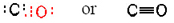
Aqui três pares de elétrons são compartilhados entre dois átomos, e temos uma ligação tripla. Ligações duplas e triplas não são apenas dispositivos para ajudar a encaixar diagramas de Lewis na teoria dos octetos. Eles têm uma existência objetiva, e sua presença em uma molécula muitas vezes tem um efeito profundo em como ela reage com outras moléculas., As ligações triplas são invariavelmente mais curtas que as ligações duplas, que por sua vez são mais curtas que as ligações únicas. In 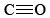 , for instance, the carbon-oxygen distance is 114 pm, in
, for instance, the carbon-oxygen distance is 114 pm, in 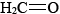 it is 121 pm, while in both ethyl alcohol and dimethyl ether and methanol it is 142 pm. Abaixo estão imagens de 3-D Jmol de monóxido de carbono, formaldeído e metanol, para comparar a diferença de comprimento de ligação com.,
it is 121 pm, while in both ethyl alcohol and dimethyl ether and methanol it is 142 pm. Abaixo estão imagens de 3-D Jmol de monóxido de carbono, formaldeído e metanol, para comparar a diferença de comprimento de ligação com.,
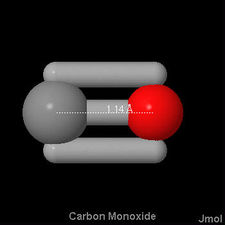
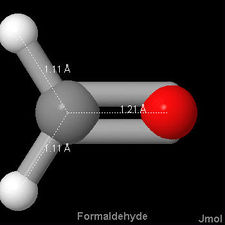
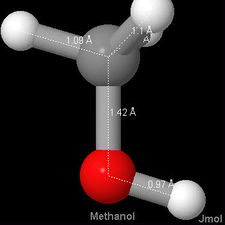
Isto concorda com a onda mecânica imagem da ligação química como sendo causado pela concentração de elétrons de densidade entre os núcleos. Quanto mais pares de elétrons são compartilhados, maior esta densidade e mais próximos os átomos são unidos. De acordo com isto, também esperaríamos que múltiplos títulos fossem mais fortes do que os únicos., De fato, a energia de ligação de C—O é encontrada experimentalmente a 360 kJ mol–1, enquanto que a de 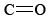 é 736 kJ mol–1, e a de
é 736 kJ mol–1, e a de 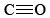 é uma gigantesca 1072 kJ mol–1. O id
é uma gigantesca 1072 kJ mol–1. O id
tripla ligação no monóxido de carbono é a ligação covalente mais forte conhecida.
a formação de ligações duplas e triplas não é tão difundida entre os átomos da tabela periódica como se pode esperar. Pelo menos um dos átomos envolvidos em uma ligação múltipla é quase sempre C, N, ou O, e na maioria dos casos ambos os átomos são membros deste trio., Outros elementos completam os seus octetos formando ligações únicas adicionais em vez de múltiplas ligações.
2H4.solução
Uma vez que os átomos de hidrogénio são univalentes, todos eles devem certamente estar ligados a átomos de carbono, presumivelmente dois a cada carbono. Cada átomo de carbono, portanto, tem a situação
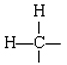
em que duas ligações ainda devem ser contabilizadas., Assumindo que os dois átomos de carbono são unidos por uma ligação dupla, todos os valence requisitos são satisfeitos, e nós podemos desenhar a estrutura de Lewis contendo satisfatória octetos:
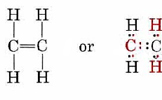
Desenhar fórmulas estruturais para (a) o CO2 e SiO2.
solução:
A) O carbono requer quatro ligações, e cada oxigênio requer duas ligações, e assim duas ligações
ligações duplas irão satisfazer as valências normais., A estrutura é
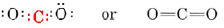
Olhando para o Jmol imagem para esta molécula, o 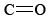 ligações duplas têm uma distância menor do que aqueles vistos em formol, mas o são mais do que a ligação tripla em monóxido de carbono:
ligações duplas têm uma distância menor do que aqueles vistos em formol, mas o são mais do que a ligação tripla em monóxido de carbono:
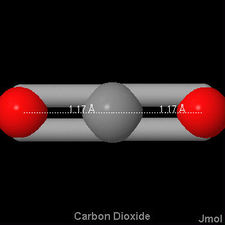
b) Silício também tem uma valência normal de 4, mas não é um elemento que facilmente formas de ligações duplas., Cada silício pode formar ligações únicas para quatro átomos de oxigênio no entanto,
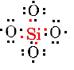
Agora o silício está satisfeito, mas cada oxigênio carece de um elétron e só formou uma ligação. Se cada um dos oxygens link para outro silício, eles vão ficar satisfeitos, mas, em seguida, adicionados átomos de silício vai ter não utilizados valências:
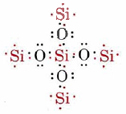
O processo de adição de oxigênio ou de átomos de silício pode continuar indefinidamente, produzindo uma gigante rede de ligadas de átomos ligados., Nesta molécula gigante, cada silício é ligado a quatro oxigenos e cada oxigênio a dois silicons, e assim há tantos átomos de oxigênio como o silício. A fórmula molecular pode ser escrita (SiO2) N onde n é um número muito grande. Uma porção desta molécula gigante é mostrada abaixo.
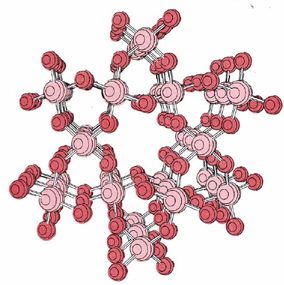
a diferença nas habilidades dos átomos de carbono e silício para formar ligações duplas tem consequências importantes no ambiente natural. Como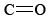 ligações duplas formam—se facilmente, o dióxido de carbono consiste de moléculas individuais-não há “espaços vazios” nos átomos de carbono ou oxigênio onde elétrons adicionais podem ser compartilhados., Portanto, há pouco para manter uma molécula de dióxido de carbono perto de outra, e a temperaturas comuns as moléculas movem-se independentemente. Numa escala macroscópica isto significa que o dióxido de carbono tem as propriedades de um gás. Em dióxido de silício, por outro lado, fortes ligações covalentes ligam todos os átomos de silício e oxigênio juntos em uma rede tridimensional. A temperaturas ordinárias, os átomos não podem vibrar longe de suas posições atribuídas, e o dióxido de silício tem as propriedades macroscópicas de um sólido.,como gás, o dióxido de carbono é muito mais livre do que o dióxido de silício para circular através do ambiente. Ele pode ser removido da atmosfera pelas plantas no processo fotossintético e eventualmente retornado ao ar por meio da respiração. Esta é uma das razões pelas quais a vida terrestre se baseia em compostos de carbono. Se um suprimento de carbono a partir do dióxido de carbono atmosférico não estivesse disponível, os organismos vivos seriam muito diferentes em forma e estrutura dos que conhecemos na terra.,autores de ficção científica gostam de sugerir, por causa da relação periódica de carbono e silício, que a vida em algum planeta distante pode ser baseada em silício. É bastante difícil imaginar, porém, o mecanismo pelo qual tais formas de vida obteriam silício das rochas e do solo da superfície de seu planeta. Certamente enfrentariam grandes dificuldades se a combinação de silício com oxigênio para formar dióxido de silício fosse usada como fonte de energia., Imagine respirar um sólido em vez do dióxido de carbono gasoso que se forma quando o carbono se combina com o oxigénio durante a respiração em organismos terrestres! As propriedades macroscópicas que são determinadas pela estrutura microscópica e pela ligação são cruciais em atividades fundamentais como a vida e a respiração.de volta à escrita das estruturas de Lewis para moléculas
ligações duplas formam—se facilmente, o dióxido de carbono consiste de moléculas individuais-não há “espaços vazios” nos átomos de carbono ou oxigênio onde elétrons adicionais podem ser compartilhados., Portanto, há pouco para manter uma molécula de dióxido de carbono perto de outra, e a temperaturas comuns as moléculas movem-se independentemente. Numa escala macroscópica isto significa que o dióxido de carbono tem as propriedades de um gás. Em dióxido de silício, por outro lado, fortes ligações covalentes ligam todos os átomos de silício e oxigênio juntos em uma rede tridimensional. A temperaturas ordinárias, os átomos não podem vibrar longe de suas posições atribuídas, e o dióxido de silício tem as propriedades macroscópicas de um sólido.,como gás, o dióxido de carbono é muito mais livre do que o dióxido de silício para circular através do ambiente. Ele pode ser removido da atmosfera pelas plantas no processo fotossintético e eventualmente retornado ao ar por meio da respiração. Esta é uma das razões pelas quais a vida terrestre se baseia em compostos de carbono. Se um suprimento de carbono a partir do dióxido de carbono atmosférico não estivesse disponível, os organismos vivos seriam muito diferentes em forma e estrutura dos que conhecemos na terra.,autores de ficção científica gostam de sugerir, por causa da relação periódica de carbono e silício, que a vida em algum planeta distante pode ser baseada em silício. É bastante difícil imaginar, porém, o mecanismo pelo qual tais formas de vida obteriam silício das rochas e do solo da superfície de seu planeta. Certamente enfrentariam grandes dificuldades se a combinação de silício com oxigênio para formar dióxido de silício fosse usada como fonte de energia., Imagine respirar um sólido em vez do dióxido de carbono gasoso que se forma quando o carbono se combina com o oxigénio durante a respiração em organismos terrestres! As propriedades macroscópicas que são determinadas pela estrutura microscópica e pela ligação são cruciais em atividades fundamentais como a vida e a respiração.de volta à escrita das estruturas de Lewis para moléculas