Zurück zum Schreiben von Lewis-Strukturen für Moleküle
Um die Anforderungen der normalen Wertigkeit zu erfüllen, ist es manchmal notwendig, mehr als eine Bindung zu haben, dh mehr als ein gemeinsames Elektronenpaar zwischen zwei Atomen. Ein Beispiel dafür ist Formaldehyd, CH2O.Um Kohlenstoff mit vier Bindungen in diesem Molekül zu versorgen, müssen wir Kohlenstoff als zwei Bindungen zum Sauerstoff sowie eine zu jedem der beiden Hydrogene betrachten., Gleichzeitig wird das Sauerstoffatom auch mit den beiden Bindungen versorgt, deren normale Wertigkeit erfordert:
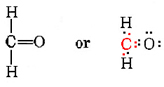
Beachten Sie, dass alle vier der geteilten Elektronen in der Kohlenstoff-Sauerstoff-Bindung sowohl im Oktett von Kohlenstoff als auch im Oktett von Sauerstoff enthalten sind. Eine Bindung mit zwei Elektronenpaaren wird als Doppelbindung bezeichnet.
Gelegentlich sagen uns die üblichen Wertigkeiten der Atome in einem Molekül nicht, wie die Skelettstruktur aussehen soll., Zum Beispiel ist es in Kohlenmonoxid, CO, schwer zu sehen, wie ein Kohlenstoffatom (übliche Wertigkeit von 4) mit einem einzelnen Sauerstoffatom (übliche Wertigkeit von 2) abgeglichen werden kann. In einem solchen Fall, in dem die Valenzen inkompatibel erscheinen, führt das Zählen von Valenzelektronen normalerweise zu einer Struktur, die der Oktettregel entspricht. Kohlenstoff hat 4 Valenzelektronen und Sauerstoff hat 6, für insgesamt 10. Wir möchten diese 10 Elektronen in zwei Oktetten anordnen, aber zwei separate Gruppen von 8 Elektronen würden 16 Elektronen erfordern., Nur wenn wir 16-10 oder 6 Elektronen teilen (so dass diese 6 Elektronen Teil jedes Oktetts sind und tatsächlich zweimal zählen), können wir die Oktettregel erfüllen. Dies führt zur Struktur
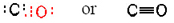
Hier werden drei Elektronenpaare zwischen zwei Atomen geteilt, und wir haben eine Dreifachbindung. Doppel – und Dreifachbindungen sind nicht nur Vorrichtungen, um Lewis-Diagramme in die Oktetttheorie einzupassen. Sie haben eine objektive Existenz, und ihre Anwesenheit in einem Molekül hat oft einen tiefgreifenden Einfluss darauf, wie es mit anderen Molekülen reagiert., Triple Bonds sind immer kürzer als Double Bonds, die wiederum kürzer als Single Bonds sind. In 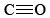 beträgt der Kohlenstoff-Sauerstoff-Abstand beispielsweise 114 pm, in
beträgt der Kohlenstoff-Sauerstoff-Abstand beispielsweise 114 pm, in 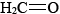 121 pm, während er sowohl in Ethylalkohol als auch in Dimethylether und Methanol 142 pm beträgt. Nachfolgend finden Sie 3-D-Aerosolbilder von Kohlenmonoxid, Formaldehyd und Methanol, um den Unterschied in der Bindungslänge mit zu vergleichen.,
121 pm, während er sowohl in Ethylalkohol als auch in Dimethylether und Methanol 142 pm beträgt. Nachfolgend finden Sie 3-D-Aerosolbilder von Kohlenmonoxid, Formaldehyd und Methanol, um den Unterschied in der Bindungslänge mit zu vergleichen.,
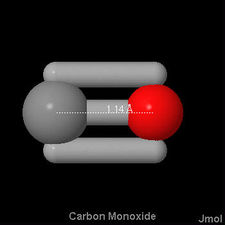
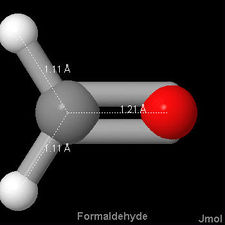
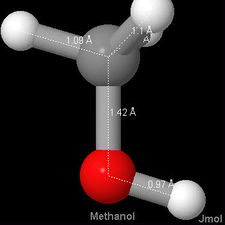
Dies stimmt mit dem wellenmechanischen Bild der chemischen Bindung überein, das durch die Konzentration der Elektronendichte zwischen den Kernen verursacht wird. Je mehr Paare von Elektronen geteilt werden, desto größer ist diese Dichte und desto enger werden die Atome zusammengezogen. In diesem Sinne würden wir auch erwarten, dass mehrere Anleihen stärker sind als einzelne Anleihen., Tatsächlich ist die Bindungsenergie von C—O experimentell 360 kJ mol–1, während die von 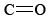 736 kJ mol–1 ist und die von
736 kJ mol–1 ist und die von 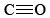 ein gigantisches 1072 kJ mol–1 ist. Die
ein gigantisches 1072 kJ mol–1 ist. Die 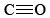 Dreifachbindung in Kohlenmonoxid erweist sich als die stärkste bekannte kovalente Bindung.
Dreifachbindung in Kohlenmonoxid erweist sich als die stärkste bekannte kovalente Bindung.
Die Bildung von Doppel – und Dreifachbindungen ist unter den Atomen des Periodensystems nicht so weit verbreitet, wie man es erwarten könnte. Mindestens eines der Atome, die an einer Mehrfachbindung beteiligt sind, ist fast immer C, N oder O, und in den meisten Fällen sind beide Atome Mitglieder dieses Trios., Andere Elemente vervollständigen ihre Oktette, indem sie anstelle mehrerer Bindungen zusätzliche Einzelbindungen bilden.
2H4.
Lösung Da Wasserstoffatome univalent sind, müssen sie sicherlich alle an Kohlenstoffatome gebunden sein, vermutlich zwei an jeden Kohlenstoff. Jedes Kohlenstoffatom hat somit die Situation
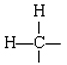
, in der noch zwei Bindungen berücksichtigt werden müssen., Unter der Annahme, dass die beiden Kohlenstoffatome durch eine Doppelbindung verbunden sind, sind alle Valenzanforderungen erfüllt, und wir können eine Lewis-Struktur zeichnen, die zufriedenstellende Oktette enthält:
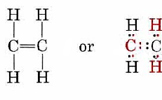
Zeichnen Sie Strukturformeln für (a) CO2 und SiO2.
Lösung:
a) Kohlenstoff benötigt vier Bindungen, und jeder Sauerstoff benötigt zwei Bindungen, und so erfüllen zwei 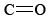 Doppelbindungen die normalen Wertigkeiten., Die Struktur ist
Doppelbindungen die normalen Wertigkeiten., Die Struktur ist
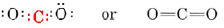
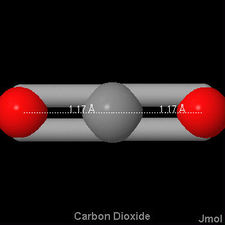
Wenn man sich das Jmol-Bild für dieses Molekül ansieht, haben die 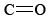 Doppelbindungen einen kürzeren Abstand als die in Formaldehyd, aber die sind länger als die Dreifachbindung in Kohlenmonoxid:
Doppelbindungen einen kürzeren Abstand als die in Formaldehyd, aber die sind länger als die Dreifachbindung in Kohlenmonoxid:
b) Silizium hat auch einen normalen valenz von 4, aber es ist kein Element, das leicht Doppelbindungen bildet., Jedes Silizium kann einzelne Bindungen zu vier Sauerstoffatomen bilden jedoch
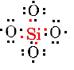
Jetzt ist das Silizium erfüllt, aber jedem Sauerstoff fehlt ein Elektron und hat nur eine Bindung gebildet. Wenn sich jedes der Oxygene mit einem anderen Silizium verbindet, sind sie zufrieden, aber die hinzugefügten Siliziumatome haben ungenutzte Wertigkeiten:
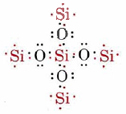
Das Hinzufügen von Sauerstoff-oder Siliziumatomen kann unbegrenzt fortgesetzt werden und ein riesiges Gitter kovalent gebundener Atome erzeugen., In diesem riesigen Molekül ist jedes Silizium an vier Oxygene und jeder Sauerstoff an zwei Silikone gebunden, und so gibt es so viele Sauerstoffatome wie Silizium. Die molekulare Formel könnte geschrieben werden (SiO2)n wobei n eine sehr große Zahl ist. Ein Teil dieses riesigen Moleküls ist unten gezeigt.
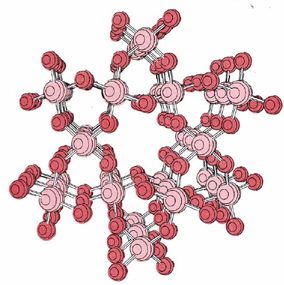
Der Unterschied in der Fähigkeit von Kohlenstoff – und Siliziumatomen, Doppelbindungen zu bilden, hat wichtige Konsequenzen in der natürlichen Umgebung. Da 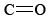 Doppelbindungen leicht bilden, besteht Kohlendioxid aus einzelnen Molekülen—es gibt keine“ Leerräume “ auf den Kohlenstoff-oder Sauerstoffatomen, in denen zusätzliche Elektronen geteilt werden können., Daher gibt es wenig, um ein Kohlendioxidmolekül nahe an ein anderes zu halten,und bei gewöhnlichen Temperaturen bewegen sich die Moleküle unabhängig voneinander. Auf makroskopischer Ebene bedeutet dies, dass Kohlendioxid die Eigenschaften eines Gases hat. In Siliziumdioxid hingegen verbinden starke kovalente Bindungen alle Silizium – und Sauerstoffatome in einem dreidimensionalen Netzwerk miteinander. Bei gewöhnlichen Temperaturen können die Atome nicht weit von ihren zugeteilten Positionen vibrieren, und Siliciumdioxid hat die makroskopischen Eigenschaften eines Feststoffs.,
Doppelbindungen leicht bilden, besteht Kohlendioxid aus einzelnen Molekülen—es gibt keine“ Leerräume “ auf den Kohlenstoff-oder Sauerstoffatomen, in denen zusätzliche Elektronen geteilt werden können., Daher gibt es wenig, um ein Kohlendioxidmolekül nahe an ein anderes zu halten,und bei gewöhnlichen Temperaturen bewegen sich die Moleküle unabhängig voneinander. Auf makroskopischer Ebene bedeutet dies, dass Kohlendioxid die Eigenschaften eines Gases hat. In Siliziumdioxid hingegen verbinden starke kovalente Bindungen alle Silizium – und Sauerstoffatome in einem dreidimensionalen Netzwerk miteinander. Bei gewöhnlichen Temperaturen können die Atome nicht weit von ihren zugeteilten Positionen vibrieren, und Siliciumdioxid hat die makroskopischen Eigenschaften eines Feststoffs.,
Als Gas ist Kohlendioxid viel freier als Siliziumdioxid, um durch die Umwelt zu zirkulieren. Es kann durch Pflanzen im photosynthetischen Prozess aus der Atmosphäre entfernt und schließlich mittels Atmung in die Luft zurückgeführt werden. Dies ist einer der Gründe, warum das Landleben auf Kohlenstoffverbindungen basiert. Wenn eine Zufuhr von Kohlenstoff aus atmosphärischem Kohlendioxid nicht verfügbar wäre, wären lebende Organismen in Form und Struktur ganz anders als die, die wir auf der Erde kennen.,
Science-Fiction-Autoren schlagen aufgrund der periodischen Beziehung von Kohlenstoff und Silizium gerne vor, dass das Leben auf einem fernen Planeten auf Silizium basieren könnte. Es ist jedoch ziemlich schwer vorstellbar, mit welchem Mechanismus solche Lebensformen Silizium aus den Gesteinen und dem Boden der Oberfläche ihres Planeten gewinnen würden. Sicherlich würden sie große Schwierigkeiten haben, wenn die Kombination von Silizium mit Sauerstoff zur Bildung von Siliciumdioxid als Energiequelle genutzt würde., Stellen Sie sich vor, Sie atmen einen Feststoff anstelle des gasförmigen Kohlendioxids aus, das sich bildet, wenn sich Kohlenstoff während der Atmung in terrestrischen Organismen mit Sauerstoff verbindet! Makroskopische Eigenschaften, die durch mikroskopische Struktur und Bindung bestimmt werden, sind selbst bei so grundlegenden Aktivitäten wie Leben und Atmen von entscheidender Bedeutung.
Zurück zum Schreiben von Lewis-Strukturen für Moleküle