Back to Writing Lewis Structures for Molecules
Al fine di soddisfare i requisiti di valenza normale, a volte è necessario avere più di un legame, cioè più di una coppia condivisa di elettroni tra due atomi. Un esempio calzante è la formaldeide, CH2O. Per fornire al carbonio quattro legami in questa molecola, dobbiamo considerare che il carbonio forma due legami con l’ossigeno e uno con ciascuno dei due idrogeni., Allo stesso tempo l’atomo di ossigeno è anche dotato dei due legami che la sua valenza normale richiede:
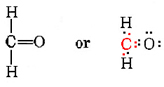
Si noti che tutti e quattro gli elettroni condivisi nel legame carbonio-ossigeno sono inclusi sia nell’ottetto di carbonio che nell’ottetto di ossigeno. Un legame che coinvolge due coppie di elettroni è chiamato doppio legame.
Occasionalmente le solite valenze degli atomi in una molecola non ci dicono quale dovrebbe essere la struttura dello scheletro., Ad esempio, nel monossido di carbonio, CO, è difficile vedere come un atomo di carbonio (valenza usuale di 4) possa essere abbinato a un singolo atomo di ossigeno (valenza usuale di 2). In un caso come questo, in cui le valenze sembrano essere incompatibili, il conteggio degli elettroni di valenza di solito porta a una struttura che soddisfa la regola dell’ottetto. Il carbonio ha 4 elettroni di valenza e l’ossigeno ne ha 6, per un totale di 10. Vogliamo organizzare questi 10 elettroni in due ottetti, ma due gruppi separati di 8 elettroni richiederebbero 16 elettroni., Solo condividendo 16-10, o 6, elettroni (in modo che quei 6 elettroni facciano parte di ciascun ottetto e, in effetti, contino due volte) possiamo soddisfare la regola dell’ottetto. Questo porta alla struttura
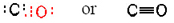
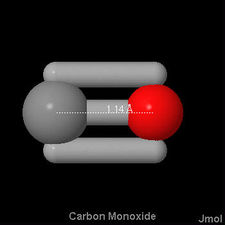
Qui tre coppie di elettroni sono condivise tra due atomi e abbiamo un triplo legame. Doppi e tripli legami non sono semplicemente dispositivi per aiutare ad adattare i diagrammi di Lewis nella teoria dell’ottetto. Hanno un’esistenza oggettiva e la loro presenza in una molecola ha spesso un effetto profondo su come reagisce con altre molecole., Le obbligazioni triple sono invariabilmente più corte delle obbligazioni doppie, che a loro volta sono più corte delle obbligazioni singole. In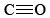 , ad esempio, la distanza carbonio-ossigeno è 114 pm, in
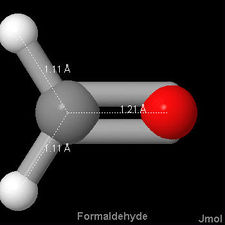
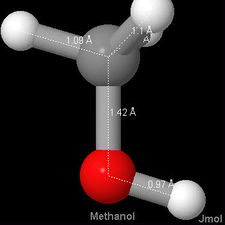
, ad esempio, la distanza carbonio-ossigeno è 114 pm, in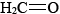 è 121 pm, mentre sia nell’alcool etilico che nell’etere dimetilico e nel metanolo è 142 pm. Di seguito sono riportate le immagini 3-D Jmol di monossido di carbonio, formaldeide e metanolo, per confrontare la differenza di lunghezza del legame con.,
è 121 pm, mentre sia nell’alcool etilico che nell’etere dimetilico e nel metanolo è 142 pm. Di seguito sono riportate le immagini 3-D Jmol di monossido di carbonio, formaldeide e metanolo, per confrontare la differenza di lunghezza del legame con.,
Questo concorda con l’immagine onda-meccanica del legame chimico come causata dalla concentrazione di densità elettronica tra i nuclei. Più coppie di elettroni sono condivise, maggiore è questa densità e più strettamente gli atomi vengono uniti. In linea con questo, ci aspetteremmo anche che più obbligazioni siano più forti delle singole obbligazioni., Infatti, l’energia di legame di C—O è trovata sperimentalmente per essere 360 kJ mol-1, mentre quella di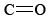 è 736 kJ mol–1, e quella di
è 736 kJ mol–1, e quella di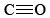 è un gigantesco 1072 kJ mol–1. Il legame triplo
è un gigantesco 1072 kJ mol–1. Il legame triplo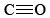 nel monossido di carbonio risulta essere il legame covalente più forte conosciuto.
nel monossido di carbonio risulta essere il legame covalente più forte conosciuto.
La formazione di legami doppi e tripli non è così diffusa tra gli atomi della tavola periodica come ci si potrebbe aspettare. Almeno uno degli atomi coinvolti in un legame multiplo è quasi sempre C, N o O, e nella maggior parte dei casi entrambi gli atomi sono membri di questo trio., Altri elementi completano i loro ottetti formando singoli legami aggiuntivi piuttosto che legami multipli.
2H4.
Soluzione Poiché gli atomi di idrogeno sono univalenti, devono certamente essere tutti legati agli atomi di carbonio, presumibilmente due per ogni carbonio. Ogni atomo di carbonio ha quindi la situazione
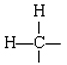
in cui due legami devono ancora essere contabilizzati., Supponendo che i due atomi di carbonio siano uniti da un doppio legame, tutti i requisiti di valenza sono soddisfatti e possiamo disegnare una struttura di Lewis contenente ottetti soddisfacenti:
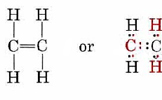
Disegnare formule strutturali per (a) CO2 e SiO2.
Soluzione:
a) Il carbonio richiede quattro legami, e ogni ossigeno richiede due legami, e quindi due 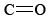 doppi legami soddisferanno le normali valenze., La struttura è
doppi legami soddisferanno le normali valenze., La struttura è
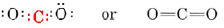
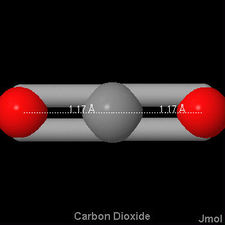
Guardando il che jmol immagine di questa molecola, il 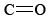 doppi legami hanno una distanza minore rispetto a quelli visti in formaldeide, ma superiore al triplo legame di monossido di carbonio:
doppi legami hanno una distanza minore rispetto a quelli visti in formaldeide, ma superiore al triplo legame di monossido di carbonio:
b) il Silicio ha anche una valenza normale di 4, ma non è un elemento che facilmente forme di doppi legami., Ogni silicio può formare singoli legami a quattro atomi di ossigeno tuttavia,
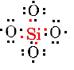
Ora il silicio è soddisfatto, ma ogni ossigeno manca di un elettrone e ha formato solo un legame. Se ciascuno degli ossigeni si collega a un altro silicio, saranno soddisfatti, ma poi gli atomi di silicio aggiunti avranno valenze inutilizzate:
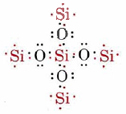
Il processo di aggiunta di atomi di ossigeno o silicio può continuare indefinitamente, producendo un gigantesco reticolo di atomi legati covalentemente., In questa molecola gigante ogni silicio è legato a quattro ossigeni e ogni ossigeno a due siliconi, e quindi ci sono tanti atomi di ossigeno quanto il silicio. La formula molecolare potrebbe essere scritta (SiO2) n dove n è un numero molto grande. Una parte di questa molecola gigante è mostrata sotto.
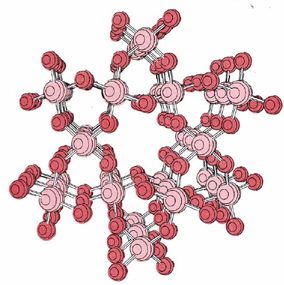
La differenza nelle capacità degli atomi di carbonio e silicio di formare doppi legami ha importanti conseguenze nell’ambiente naturale. Poiché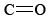 i doppi legami si formano facilmente, l’anidride carbonica è costituita da singole molecole—non ci sono “spazi vuoti” sugli atomi di carbonio o di ossigeno in cui possono essere condivisi elettroni aggiuntivi., Quindi c’è poco da tenere una molecola di anidride carbonica vicino a un altro, e a temperature ordinarie le molecole si muovono in modo indipendente. Su scala macroscopica ciò significa che l’anidride carbonica ha le proprietà di un gas. Nel biossido di silicio, d’altra parte, forti legami covalenti collegano tutti gli atomi di silicio e ossigeno insieme in una rete tridimensionale. A temperature ordinarie gli atomi non possono vibrare lontano dalle loro posizioni assegnate e il biossido di silicio ha le proprietà macroscopiche di un solido.,
i doppi legami si formano facilmente, l’anidride carbonica è costituita da singole molecole—non ci sono “spazi vuoti” sugli atomi di carbonio o di ossigeno in cui possono essere condivisi elettroni aggiuntivi., Quindi c’è poco da tenere una molecola di anidride carbonica vicino a un altro, e a temperature ordinarie le molecole si muovono in modo indipendente. Su scala macroscopica ciò significa che l’anidride carbonica ha le proprietà di un gas. Nel biossido di silicio, d’altra parte, forti legami covalenti collegano tutti gli atomi di silicio e ossigeno insieme in una rete tridimensionale. A temperature ordinarie gli atomi non possono vibrare lontano dalle loro posizioni assegnate e il biossido di silicio ha le proprietà macroscopiche di un solido.,
Come gas, l’anidride carbonica è molto più libera del biossido di silicio per circolare attraverso l’ambiente. Può essere rimosso dall’atmosfera dalle piante nel processo fotosintetico e alla fine restituito all’aria per mezzo della respirazione. Questo è uno dei motivi per cui la vita terrestre si basa su composti di carbonio. Se non fosse disponibile una fornitura di carbonio dall’anidride carbonica atmosferica, gli organismi viventi sarebbero molto diversi per forma e struttura da quelli che conosciamo sulla terra.,
Gli autori di fantascienza amano suggerire, a causa della relazione periodica tra carbonio e silicio, che la vita su qualche pianeta lontano potrebbe essere basata sul silicio. È piuttosto difficile immaginare, però, il meccanismo con cui tali forme di vita otterrebbero silicio dalle rocce e dal suolo della superficie del loro pianeta. Certamente avrebbero dovuto affrontare grandi difficoltà se la combinazione di silicio con ossigeno per formare biossido di silicio dovesse essere utilizzato come fonte di energia., Immagina di espirare un solido invece dell’anidride carbonica gassosa che si forma quando il carbonio si combina con l’ossigeno durante la respirazione negli organismi terrestri! Le proprietà macroscopiche determinate dalla struttura microscopica e dal legame sono cruciali anche in attività fondamentali come la vita e la respirazione.
Torna a scrivere strutture di Lewis per molecole