Einleitung
Eine der wichtigsten Entdeckungen auf dem Gebiet der Fluoreszenzmikroskopie fand sich in einer Qualle in den 1960er Jahren. Osamu Shimomura von der Princeton University studierte in victoria, einer biolumineszierenden Qualle., Es sollte hier darauf hingewiesen werden, dass Lumineszenz nicht dasselbe ist wie Fluoreszenz:
- Lumineszenz: die spontane Emission von Licht von einer Substanz (wenn diese Substanz ein Tier ist, wird sie als Biolumineszenz bezeichnet)
- Fluoreszenz: die Emission von Licht von einer Substanz, die Licht absorbiert hat und angeregt wird
Durch die Untersuchung von A. victoria wurden zwei Hauptproteine entdeckt: Aequorin (ein Photoprotein) und green fluorescent Protein (GFP). Die Qualle produziert Kalzium, das mit Aequorin interagiert und blaue Lumineszenz erzeugt., Dieses blaue Licht wird von GFP absorbiert und als grüne Fluoreszenz wieder emittiert. Diese Proteine wurden aus der Qualle isoliert und gereinigt und werden bis heute in der Forschung stark eingesetzt. Für diese Forschung haben Osamu Shimomura und Kollegen 2008 den Nobelpreis für Chemie gewonnen.
Grün fluoreszierendes Protein
GFP wird durch Licht im blauen/violetten/ultravioletten Teil des Spektrums angeregt und emittiert Licht im grünen Teil (daher der Name). Die Struktur des Proteins ist in Abb.1., GFP ist eine Tonnenform mit dem fluoreszierenden Teil (dem Chromophor), der aus nur drei Aminosäuren besteht. Wenn dieser Chromophor blaues Licht absorbiert, emittiert er grüne Fluoreszenz.
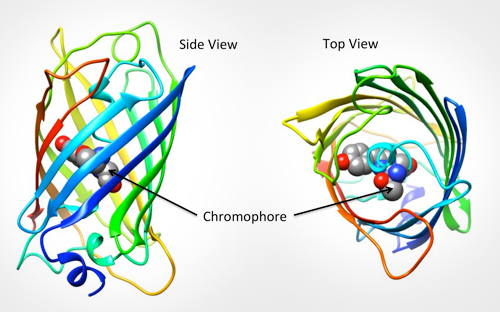
GFP In der Forschung
Die Verwendung von GFP in der Forschung wurde deutlich, sobald das Gen für GFP ebenfalls isoliert wurde und GFP zu Zellen hinzugefügt oder genetisch in lebende Organismen transplantiert werden konnte. Einige Anwendungen und Vorteile von GFP unten diskutiert.
GFP als Toxizitätsmarker: Aufgrund der Tatsache, dass GFP mit zunehmender Toxizität an Fluoreszenzintensität abnimmt, kann es als Marker für Umwelttoxizität verwendet werden., GFP kann Wirtsorganismen ohne negativen Effekt zugesetzt werden, und dann wird die Intensität in verschiedenen Umgebungen in verschiedenen Organismen nachverfolgt.
GFP ist vererbbar, wenn ein Organismus GFP in sein Genom eingeschlagen hat, wird GFP natürlich ohne zusätzliche Prozesse an die Nachkommen weitergegeben, so dass nicht-invasive Wege zur Einführung eines fluoreszierenden Markers und zur Verfolgung über Generationen von Tieren oder Zellen möglich sind. GFP stört keine biologischen Prozesse., Transgene Mäuse können mit GFP markiert werden, was dann bei ihren Nachkommen leicht beobachtet werden kann, indem sie einfach blauem oder UV-Licht ausgesetzt werden, wie in Abb.2.
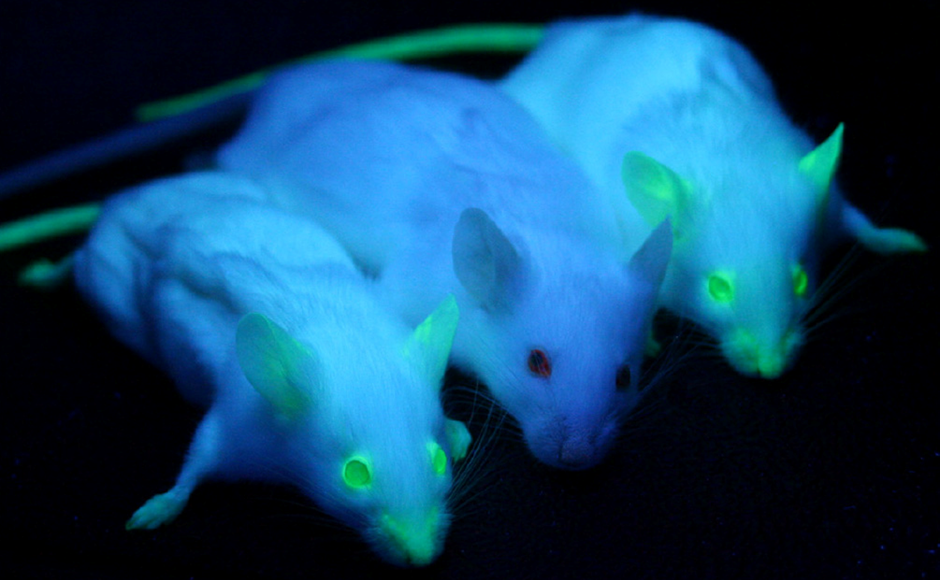
GFP kann mit anderen Proteinen verschmolzen werden, wodurch diese Proteine effektiv fluoreszierend werden. Dies kann mit speziellen Linkern erfolgen, damit GFP die Funktion des interessierenden Proteins nicht beeinflusst und dennoch durch Zellen diffundieren kann. Auf diese Weise kann jedes Protein lokalisiert und mit Standard-Fluoreszenzmikroskopie verfolgt werden, indem ein blaues Licht auf die Zellen scheint, wird das Protein von Interesse mit einem grünen Licht fluoreszieren zurück.,
GFP in Lebendzellexperimenten: Das klassische grün fluoreszierende Molekül ist Fluoresceinisothiocyanat (FITC), das jedoch für Zellen toxisch ist und nicht direkt verwendet werden kann, ohne die Zellen vorher zu fixieren oder unvermeidbare Schäden zu verursachen. GFP ist weit weniger schädlich, da es ein natürlich vorkommendes Protein ist und in Experimenten an lebenden Zellen verwendet werden kann, während es praktisch keinen Schaden verursacht, insbesondere wenn es an Nachkommen weitergegeben wird.
GFP in fortgeschrittenen Mikroskopie-Anwendungen., Mit GFP wurden mehrere fluoreszenzmikroskopische Anwendungen wie Fluoreszenzrückgewinnung nach Photobleaching (FRAP) und Förster Resonance Energy Transfer (FRET) entwickelt, die es Forschern ermöglichen, immer spezifischere und leistungsfähigere Fluoreszenzanwendungen für ihre Bildgebung zu nutzen. Diese Techniken werden in anderen kurzen Artikeln beschrieben, nämlich was ist BUND und was ist FRAP?
GFP ist modifizierbar, da der genetische und Aminosäurecode für GFP gut verstanden ist und mehreren Modifikationen unterzogen wurde., Erstens wurde GFP modifiziert, um ein verbessertes GFP (eGFP) zu erzeugen, das eine erhöhte Fluoreszenzintensität, eine größere Photostabilität, bequemere Anregungsspitzen und einen höheren Wirkungsgrad bei Raumtemperatur aufweist. Änderungen direkt am Chromophor ermöglichen es GFP, mit verschiedenen Farben zu fluoreszieren, wodurch Blau (BFP), Cyan (CFP), Gelb (YFP), Rot (RFP) und andere erzeugt werden, die alle separat verbessert wurden und ihre eigenen Anwendungen haben. Einige herausragende Modifikationen umfassen mCherry (rot), Citrin und Venus (gelb) und Cerulean (Cyan), um nur einige zu nennen., Es existieren jetzt ganze Familien fluoreszierender Proteine, die alle vom ursprünglichen GFP abgeleitet sind, wie in Abb.3.
Zusammenfassung
GFP ist ein grundlegender Bestandteil der Fluoreszenzmikroskopie, da die Benutzerfreundlichkeit und die Anwendungen nur durch die Vorstellungskraft des Forschers begrenzt sind. Ständige Verbesserungen der GFP im Laufe der Zeit haben dazu geführt, dass die Fluoreszenzmikroskopie und-forschung aufgrund der hochflexiblen Natur von GFP und der großen Anzahl von Forschungen, die auf der Verwendung von GFP und seinen vielen Varianten basieren, vorangekommen sind.