introduktion
en av de viktigastediskoverier inom fluorescerande mikroskopi hittades i en manet på 1960-talet. Osamu Shimomura från Princeton University studerade Aequorea victoria, en bioluminescent maneter., Det bör här vara positivt att luminiscens inte är detsamma som fluorescens:
- luminiscens: den spontana emissionen av ljus från ett ämne (när det ämnet är ett djur, kallas det bioluminescens)
- fluorescens: emissionen av ljus från ett ämne som har absorberat ljus och blir upphetsad
genom studien av A. victoria upptäcktes två huvudproteiner: aequorin (ett fotoprotein) och grönt fluorescerande protein (GFP).. – herr talman! Maneten producerar kalcium, som interagerar med aequorin och producerar blå luminescens., Detta blå ljus absorberas av GFP och åter emitteras som grön fluorescens. Dessa proteiner har isolerats och renats från maneten och används kraftigt i forskning till denna dag. För denna forskning vann Osamu Shimomura och kollegor Nobelpriset i kemi 2008.
grönt fluorescerande Protein
GFP är upphetsad av ljus i den blå/violett / ultravioletta delen av spektrumet och avger ljus i den gröna delen (därav namnet). Strukturen av proteinet kan ses i Fig.1., GFP är en tunnform med den fluorescerande delen (kromoforen) som består av bara tre aminosyror. När denna kromofor absorberar blått ljus, avger den grön fluorescens.
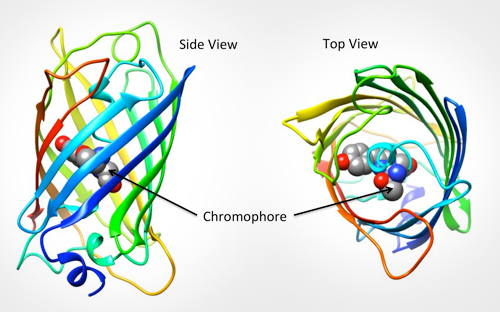
GFP i forskning
användningen av GFP i forskning blev tydlig när genen för GFP också isolerades och GFP kunde tillsättas till celler eller genetiskt ympas i levande organismer. Vissa tillämpningar och fördelar med GFP diskuteras nedan.
GFP som toxicitetsmarkör: på grund av att GFP minskar i fluorescensintensiteten med ökande toxicitet kan den användas som markör för miljötoxicitet., GFP kan läggas till värdorganismer utan negativ effekt, och sedan spåras intensiteten i olika miljöer i olika organismer.
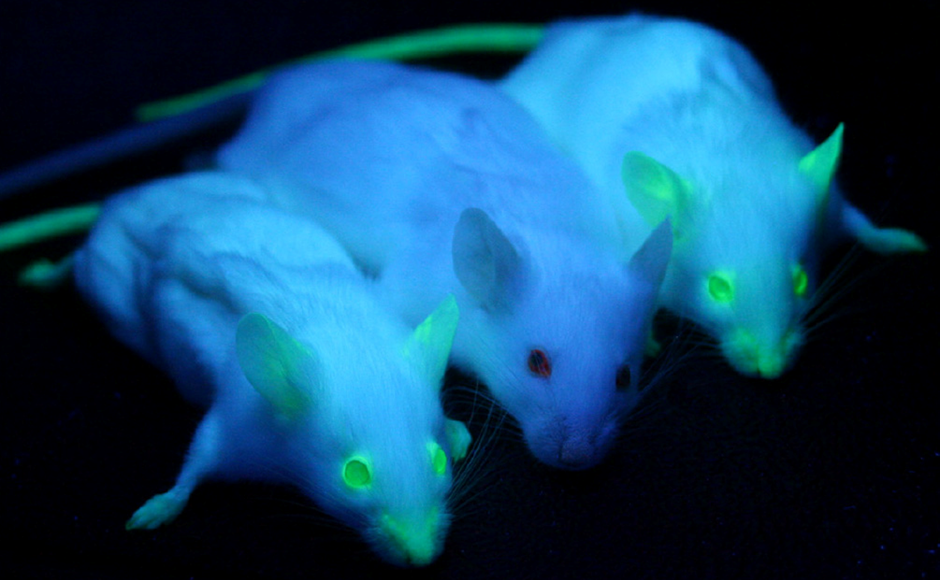
GFP är ärftligt, om en organism har GFP knackat in i sitt Genom, kommer GFP naturligtvis att överföras på avkomman utan några ytterligare processer, vilket möjliggör icke-invasiva sätt att införa en fluorescerande markör och spåra den över generationer av djur eller celler. GFP stör inte några biologiska processer., Transgena möss kan märkas med GFP, som sedan lätt observeras i deras avkomma bara genom att utsätta dem för blått eller UV-ljus, som ses i Fig.2.
GFP kan smälta till andra proteiner, vilket effektivt gör dessa proteiner fluorescerande. Detta kan göras med speciella linkers så att GFP inte påverkar funktionen av proteinet av intresse, och det kan fortfarande diffundera genom celler. Detta gör att något protein kan lokaliseras och spåras med hjälp av standard fluorescerande mikroskopi, genom att skina ett blått ljus på cellerna, kommer proteinet av intresse att fluorescera tillbaka med ett grönt ljus.,
GFP i experiment med levande celler: den klassiska gröna fluorescerande molekylen är fluoresceinisotiocyanat (FITC), men detta är giftigt för celler och kan inte användas direkt utan att först fixera cellerna eller orsaka oundviklig skada. GFP är mycket mindre skadligt eftersom det är ett naturligt förekommande protein och kan användas i experiment på levande celler samtidigt som det orsakar praktiskt taget ingen skada, särskilt om det vidarebefordras till avkomman.
GFP i avancerade mikroskopiapplikationer., Flera fluorescensmikroskopiapplikationer såsom fluorescensåtervinning efter fotoblekning (FRAP) och Förster resonance energy transfer (FRET) utvecklades med GFP, vilket gör det möjligt för forskare att använda allt mer specifika och kraftfulla tillämpningar av fluorescens för deras bildbehandling. Dessa tekniker beskrivs i andra korta artiklar, nämligen vad är FRET och vad är FRAP?
GFP är modifierbar, eftersom den genetiska och aminosyrakoden för GFP är väl förstådd har den varit föremål för flera modifieringar., För det första modifierades GFP för att producera förbättrad GFP (eGFP), som har ökad fluorescensintensitet, större fotostabilitet, bekvämare excitationstoppar och högre effektivitet vid rumstemperatur. Modifieringar direkt till chromophore tillåter GFP att fluoresce med olika färger, skapa blå (BFP), cyan (CFP), gul (YFP), röd (RFP) och andra, som alla har förbättrats separat och har sina egna applikationer. Några enastående ändringar inkluderar mCherry (röd), Citrin och Venus (gul) och Cerulean (cyan) för att nämna några., Hela familjer av fluorescerande proteiner finns nu, alla härledda från den ursprungliga GFP, som ses i Fig.3.
sammanfattning
GFP är en grundläggande del av fluorescensmikroskopi på grund av användarvänligheten och ansökningarna begränsas endast av forskarens fantasi. Konstanta förbättringar på GFP över tiden har orsakat fluorescensmikroskopi och forskning att gå framåt, på grund av GFP: s mycket flexibla natur och den stora forskningen som bygger på att använda GFP och dess många varianter.