12.7 tampoane
obiective de învățare
- Define tampon.
- identificați corect cele două componente ale unui tampon.după cum este indicat în secțiunea 12.4 „acizi și baze puternice și slabe și sărurile lor”, acizii slabi sunt relativ obișnuiți, chiar și în alimentele pe care le consumăm. Dar întâlnim ocazional un acid sau o bază puternică, cum ar fi acidul stomacal, care are un pH puternic acid de 1, 7. Prin definiție, acizii și bazele puternice pot produce o cantitate relativ mare de ioni H+ sau OH și, prin urmare, au activități chimice marcate., În plus, cantități foarte mici de acizi și baze puternice pot schimba foarte repede pH-ul unei soluții. Dacă s—ar adăuga 1 mL de acid stomacal în sânge și nu ar exista niciun mecanism de corectare, pH-ul sângelui ar scădea de la aproximativ 7, 4 la aproximativ 4, 7-un pH care nu favorizează continuarea vieții. Din fericire, organismul are un mecanism pentru minimizarea unor astfel de modificări dramatice ale pH-ului.mecanismul implică un tampono soluție care rezistă schimbărilor dramatice ale pH-ului., o soluție care rezistă schimbărilor dramatice ale pH-ului., Tampoanele fac acest lucru prin faptul că sunt compuse din anumite perechi de soluții: fie un acid slab plus o sare derivată din acel acid slab, fie o bază slabă plus o sare a acelei baze slabe. De exemplu, un tampon poate fi compus din hc2h3o2 dizolvat (un acid slab) și NaC2H3O2 (sarea derivată din acel acid slab). Un alt exemplu de tampon este o soluție care conține NH3 (o bază slabă) și NH4Cl (o sare derivată din acea bază slabă).
să folosim un tampon HC2H3O2/nac2h3o2 pentru a demonstra cum funcționează tampoanele., Dacă o bază puternică—o sursă de OH−(aq) ioni—este adăugat la soluția tampon, acei ioni OH− va reacționa cu HC2H3O2 într-o reacție acido-bazic:
HC2H3O2(aq) + OH−(aq) → H2O(ℓ) + C2H3O2−(aq)
mai Degrabă decât schimbarea pH-ului în mod dramatic de a face soluția de bază, a adăugat OH− ioni reacționa pentru a face H2O, deci pH-ul nu se schimba prea mult.dacă în soluția tampon se adaugă un acid puternic—o sursă de ioni H+, ionii H+ vor reacționa cu anionul din sare. Deoarece HC2H3O2 este un acid slab, nu este ionizat prea mult., Acest lucru înseamnă că, dacă o mulțime de ioni H+ și C2H3O2− ioni sunt prezente în aceeași soluție, ei vor veni împreună pentru a face HC2H3O2:
H+(aq) + C2H3O2−(aq) → HC2H3O2(aq)
mai Degrabă decât schimbarea pH-ul dramatic și de a face soluție acidă, a adăugat ioni H+ reacționa pentru a face moleculele unui acid slab. Figura 12.2″ acțiunile tampoanelor ” ilustrează ambele acțiuni ale unui tampon.figura 12.2 acțiunile tampoanelor
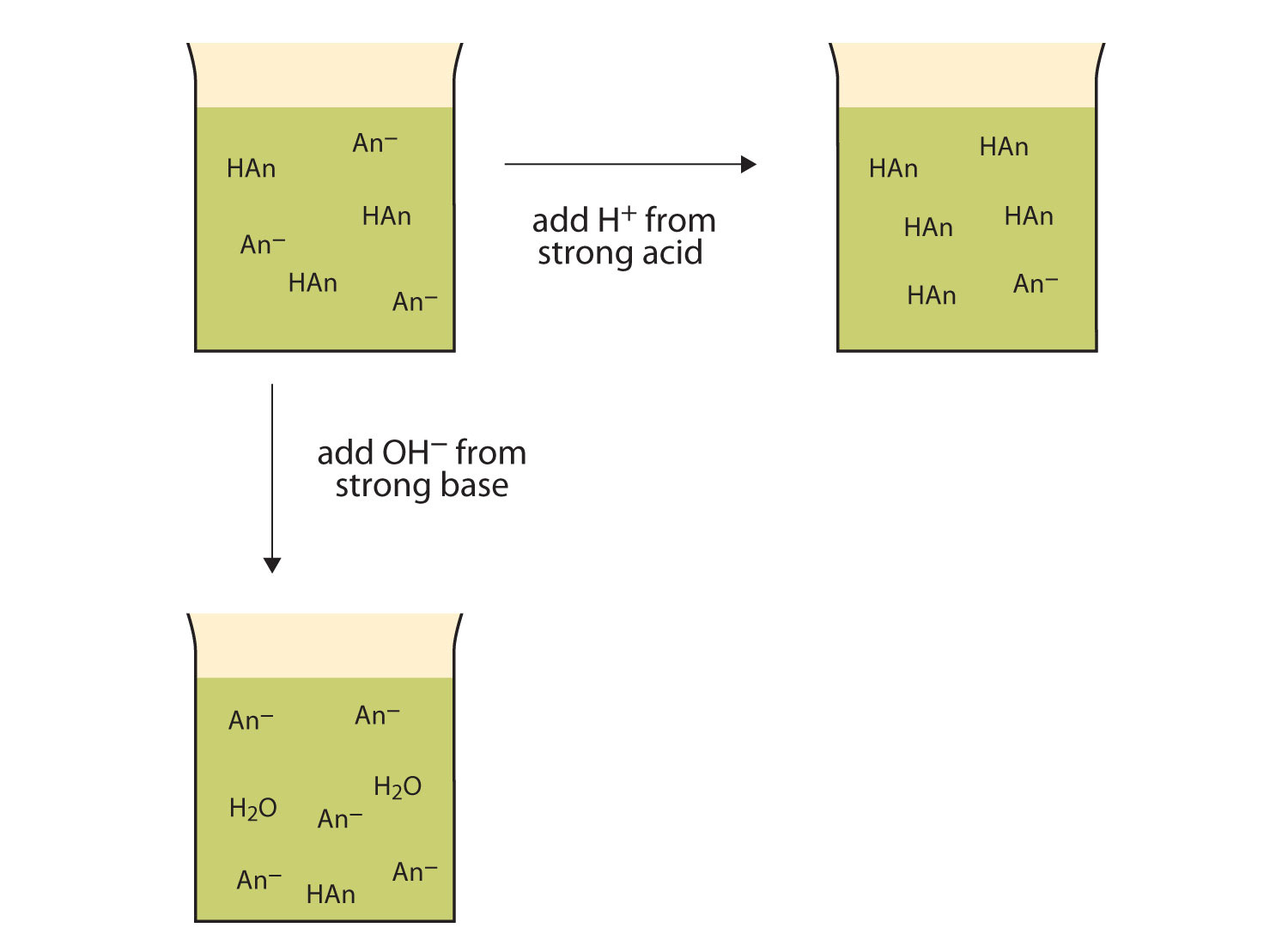
tampoanele pot reacționa atât cu acizi puternici (top), cât și cu baze puternice (laterale) pentru a minimiza modificările mari ale pH-ului.,tampoanele obținute din baze slabe și sărurile bazelor slabe acționează în mod similar. De exemplu, într-un buffer care conține NH3 și NH4Cl NH3 molecule pot reacționa cu excesul de ioni H+ introdus de acizi tari:
NH3(aq) + H+(aq) → NH4+(aq)
în timp ce NH4+(aq) ion poate reacționa cu orice ioni OH− introdus de baze tari:
NH4+(aq) + OH−(aq) → NH3(aq) + H2O(ℓ)
Exemplu 15
Ce combinații de compuși pot face o soluție tampon?,
- HCHO2 și NaCHO2
- HCl și NaCl
- CH3NH2 și CH3NH3Cl
- NH3 și NaOH
Soluție
- HCHO2 este acid formic, un acid slab, în timp ce NaCHO2 de sare este făcut de anioni slab acid (de formiat de ion ). Combinația acestor două soluții ar face o soluție tampon.
- HCl este un acid puternic, nu un acid slab, astfel încât combinația acestor două soluții nu ar face o soluție tampon.
- CH3NH2 este metilamina, care este ca NH3 cu unul dintre atomii săi H substituiți cu o grupare CH3. Deoarece nu este listat în tabelul 12.,2 „acizi și baze puternice”, putem presupune că este o bază slabă. Compusul CH3NH3Cl este o sare făcută din acea bază slabă, astfel încât combinația acestor două soluții ar face o soluție tampon.
- NH3 este o bază slabă, dar NaOH este o bază puternică. Combinația acestor două soluții nu ar face o soluție tampon.
Testați-vă
ce combinații de compuși pot face o soluție tampon?,
- NaHCO3 și NaCl
- H3PO4 și NaH2PO4
- NH3 și (NH4)3PO4
- NaOH și NaCl
Răspunsuri
- nu
- da
- da
- nu
Tampoane funcționează bine doar pentru cantități limitate de adăugat acid tare sau bază. Odată ce soluția este complet reacționată, soluția nu mai este un tampon și pot apărea modificări rapide ale pH-ului. Spunem că un tampon are o anumită capacitatecantitatea de acid puternic sau de bază un tampon poate contracara.., Tampoanele care au mai multe dizolvate dizolvate în ele pentru a începe au capacități mai mari, așa cum s-ar putea aștepta.sângele uman are un sistem de tamponare pentru a minimiza modificările extreme ale pH – ului .un tampon în sânge se bazează pe prezența HCO3− și H2CO3. Cu acest tampon prezent, chiar dacă un anumit acid stomacal și-ar găsi drumul direct în sânge, modificarea pH-ului sângelui ar fi minimă. În interiorul multor celule ale corpului, există un sistem de tamponare bazat pe ioni de fosfat.,deși medicamentele nu sunt tocmai „alimente și băuturi”, le ingerăm, așa că haideți să aruncăm o privire la un acid care este probabil cel mai frecvent medicament: acidul acetilsalicilic, cunoscut și sub denumirea de aspirină. Aspirina este bine cunoscută ca un calmant și antipiretic (reductor de febră).
structura aspirinei este prezentată în figura însoțitoare. Partea acidă este încercuită; atomul H din acea parte poate fi donat, deoarece aspirina acționează ca un acid Brønsted-Lowry. Deoarece nu este prezentat în tabelul 12.,2 „acizi și baze puternice”, acidul acetilsalicilic este un acid slab. Cu toate acestea, este încă un acid și având în vedere că unii oameni consumă zilnic cantități relativ mari de aspirină, natura sa acidă poate provoca probleme în mucoasa stomacului, în ciuda apărării stomacului împotriva propriului acid stomacal.figura 12.3 structura moleculară a aspirinei
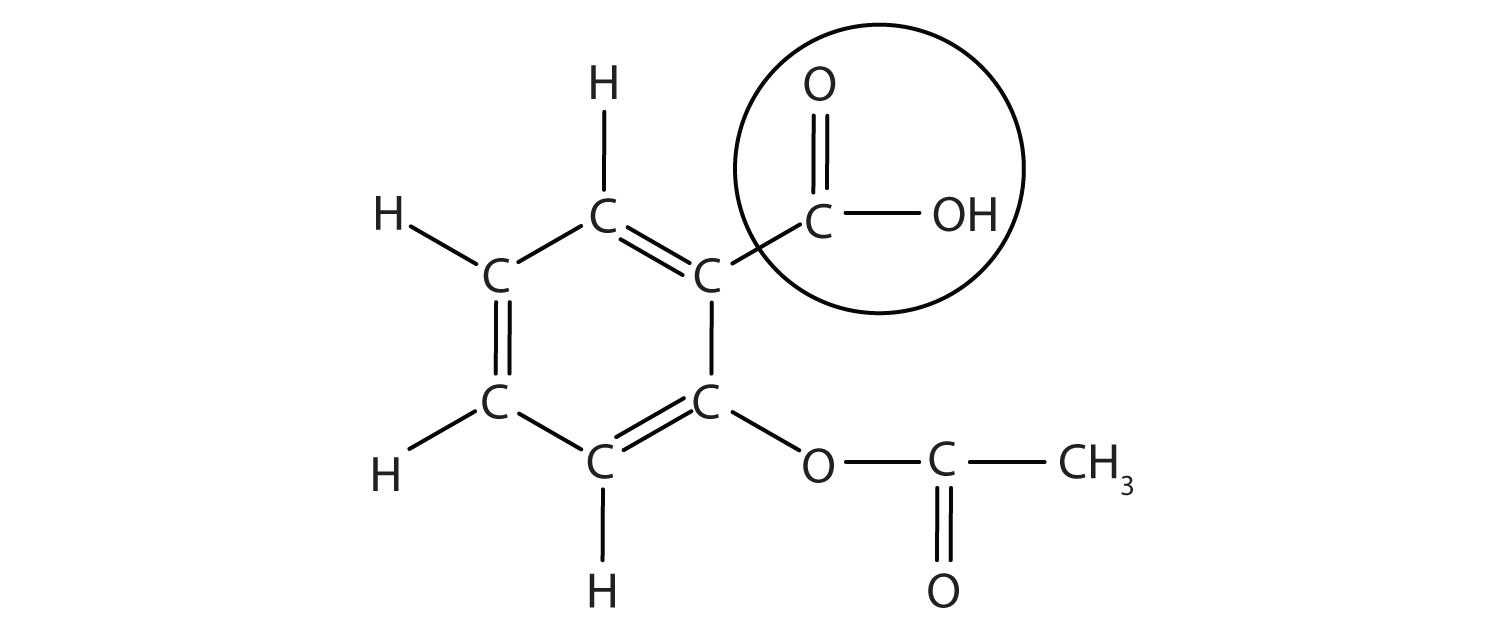
atomii încercuiți sunt partea acidă a moleculei.deoarece proprietățile acide ale aspirinei pot fi problematice, multe mărci de aspirină oferă o formă de „aspirină tamponată” a medicamentului., În aceste cazuri, aspirina conține, de asemenea, un agent de tamponare—de obicei MgO—care reglează aciditatea aspirinei pentru a minimiza efectele secundare acide.la fel de util și comun ca aspirina, a fost comercializat oficial ca medicament începând cu 1899. US Food and Drug Administration (FDA), agenția guvernamentală însărcinată cu supravegherea și aprobarea medicamentelor în Statele Unite, nu a fost formată până în 1906., Unii au susținut că, în cazul în care FDA a fost format înainte de aspirina a fost introdus, aspirina nu poate fi primit aprobarea din cauza potențialului său de efecte secundare—hemoragii gastro-intestinale, zgomote în urechi, sindromul Reye (o problemă de ficat), și unele reacții alergice. Cu toate acestea, recent aspirina a fost touted pentru efectele sale în diminuarea atacuri de cord si accidente vasculare cerebrale, deci este probabil ca aspirina este aici pentru a rămâne.
Takeaway cheie
- un tampon este o soluție care rezistă schimbărilor bruște ale pH-ului.
exerciții
-
Define tampon., Ce două componente chimice conexe sunt necesare pentru a face un tampon?se poate face un tampon prin combinarea unui acid puternic cu o bază puternică? De ce sau de ce nu?
-
ce combinații de compuși pot face un tampon? Să presupunem soluții apoase.
- HCl și NaCl
- HNO2 și NaNO2
- NH4NO3 și HNO3
- NH4NO3 și NH3
-
Ce combinații de compuși poate face un tampon? Să presupunem soluții apoase.,
- H3PO4 și Na3PO4
- NaHCO3 și Na2CO3
- NaNO3 și Ca(NO3)2
- HN3 și NH3
-
Pentru fiecare combinație în Exercițiu 3, care este un buffer, scrie ecuațiile chimice pentru reacțiile de tampon componente atunci când un acid tare și o bază tare este adăugat.pentru fiecare combinație din exercițiul 4 care este un tampon, scrieți ecuațiile chimice pentru reacțiile componentelor tampon atunci când se adaugă un acid puternic și o bază puternică.,sistemul tampon fosfat complet se bazează pe patru substanțe: H3PO4, H2PO4−, HPO42−și PO43 -. Ce soluții tampon diferite pot fi făcute din aceste substanțe?
-
explicați de ce NaBr nu poate fi o componentă nici într-un tampon acid, nici într-un tampon bazic.
-
se obțin două soluții care conțin aceleași concentrații de soluții. O soluție este compusă din H3PO4 și Na3PO4, în timp ce cealaltă este compusă din HCN și NaCN. Ce soluție ar trebui să aibă capacitatea mai mare ca tampon?,
-
se obțin două soluții care conțin aceleași concentrații de soluții. O soluție este compusă din NH3 și NH4NO3, în timp ce cealaltă este compusă din H2SO4 și Na2SO4. Ce soluție ar trebui să aibă capacitatea mai mare ca tampon?
răspunsuri
-
un tampon este combinația dintre un acid sau o bază slabă și o sare a acelui acid sau bază slabă.,
-
-
- nu
- da
- nu
- da
-
-
3b: acid tare: NO2− + H+ → HNO2; bază puternică: HNO2 + OH− → NO2− + H2O; 3d: bază puternică: NH4+ + OH− → NH3 + H2O; puternic acid: NH3 + H+ → NH4+
-
-
Tampoane pot fi făcute din trei combinații: (1) H3PO4 și H2PO4−, (2) H2PO4− și HPO42−, și (3) HPO42− și PO43−. (Tehnic, un tampon poate fi realizat din oricare două componente.,)
-
-
tamponul fosfat ar trebui să aibă o capacitate mai mare.
-