US Pharm. 2010; 35(8):HS2-HS4. Staphylococcus aureus rezistent la meticilină (MRSA) este una dintre principalele cauze ale infecțiilor dobândite atât în domeniul sănătății, cât și în comunitate.1,2 infecțiile datorate MRSA sunt asociate cu un risc ridicat de morbiditate și mortalitate și duc la costuri ridicate de îngrijire a sănătății.3-5 incidența infecțiilor cu MRSA în Statele Unite a crescut constant în ultimii ani de la 22% în 1995 la 60% în 2003.,6 Sănătate asociate cu MRSA (HA-MRSA) este legat de spitale și de îngrijire pe termen lung facilități și este comună la pacienții cu spitalizare prelungită, trecut antimicrobiene utilizare, ulcere de decubit, dializă, locuirea catetere, enterală mese, sau istoria IV abuzul de droguri.7,8 în ultimii ani, cu toate acestea, a existat o creștere a unei noi tulpini de MRSA numită MRSA asociată comunității (CA-MRSA)., Acest lucru pare să fie dobândit în ambulatoriu, iar transmiterea se face prin contact fizic strâns, cum ar fi în centrele de zi, rezervațiile indiene și facilitățile corecționale și printre sportivi, personal militar și bărbați care fac sex cu bărbați.7,9,10
distingerea tulpinilor MRSA
Mai multe rapoarte au evidențiat diferențe între tulpinile HA-MRSA și CA-MRSA, inclusiv prezența diferitelor genotipuri între cele două tulpini. CA-MRSA este susceptibilă la mai multe antibiotice non-beta-lactamice, în timp ce tulpinile HA-MRSA nu sunt., Tulpinile de CA-MRSA sunt mai susceptibile de a codifica anumiți factori virulenți care au fost asociați cu pneumonia severă (în special la copii) și infecțiile cutanate și ale țesuturilor moi la adulți.8,11,12 CDC a stabilit criteriile de diferențiere a CA-MRSA de HA-MRSA. Aceste linii directoare includ izolarea unei culturi MRSA pozitive în termen de 48 de ore de la internarea unui pacient în spital. Pentru a fi considerat CA-MRSA, pacientul nu trebuie să aibă oricare dintre următoarele: spitalizare recentă; admiterea la un azil de bătrâni, hospice sau o unitate de îngrijire calificată; dializă; sau intervenții chirurgicale recente., De asemenea, pacientul nu trebuie să aibă catetere interioare sau alte dispozitive medicale.13
Tratează CA-MRSA
CDC recomandă tratarea și prevenirea unor focare de CA-MRSA includ acoperă infecții care produc puroi, spălat pe mâini frecvent, nu schimbul de obiecte personale, masina de spalat lenjerii de pat murdare și hainele cu apă caldă, iar uscarea cârpe într-un uscător fierbinte, comparativ cu uscare la aer.13 pentru abcesele cutanate, tratamentul include incizia și drenajul abceselor cu sau fără antibiotice sistemice, în funcție de gravitatea infecției.,Tratamentul CA-MRSA include, de obicei, utilizarea de agenți precum clindamicina, tetraciclinele și trimetoprim-sulfametoxazolul (tmp-SMX). Antibioticul rifampicină nu trebuie utilizat niciodată ca monoterapie pentru tratamentul MRSA. Rezistența se dezvoltă rapid cu monoterapia cu rifampicină; cu toate acestea, atunci când este utilizată în combinație cu un alt agent anti-MRSA, poate eradica mai eficient organismele din locurile purtătoare.15 antibioticele menționate mai sus sunt, de obicei, opțiuni de tratament viabile la pacienții tratați în ambulatoriu., În infecții grave care necesită spitalizare, antibiotice IV inclusiv vancomicină, linezolid, quinupristin-dalfopristin, daptomicina, tigeciclina, și telavancin sunt adecvate terapii care pot fi utilizate (TABELUL 1).
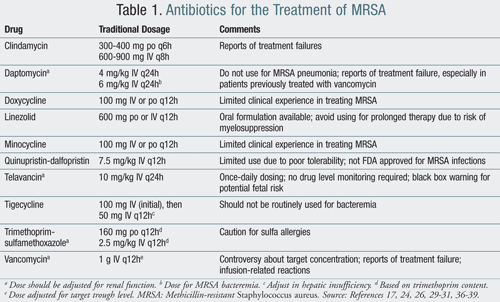
Deși clindamicina (Cleocin.) ar putea fi folosite pentru CA-MRSA, rezistența a fost raportat a fi de până la 19% la pacienții tratați cu ea. Astfel, pacienții tratați cu clindamicină trebuie monitorizați mai atent pentru dezvoltarea rezistenței autoinduse.,16 clindamicina a fost, de asemenea, asociată cu dezvoltarea infecțiilor cu Clostridium difficile, limitând utilizarea acesteia pe o perioadă îndelungată.TMP-SMX (Bactrim) poate fi considerată o alternativă la terapia cu vancomicină în unele cazuri de infecții cu MRSA. Cu toate acestea, ca și în cazul clindamicinei, au existat rapoarte privind eșecurile tratamentului. Această terapie are, de asemenea, o utilizare limitată datorită incidenței ridicate a alergiilor la sulfonamidă, care au fost raportate la până la 10% din populație.,18
minociclina (Minocin) și doxiciclina (Vibramicina) sunt antibiotice de tetraciclină care au fost utilizate pentru tratamentul MRSA. Aceste medicamente au doar date limitate privind utilizarea în MRSA, dar s-a raportat succes clinic.19
tratarea ha-MRSA
antibioticele parenterale sunt considerate standardul de aur pentru tratamentul HA-MRSA. Timp de câteva decenii, antibioticul glicopeptidic vancomicină a fost utilizat pe scară largă. vancomicina (Vancocina) inhibă sinteza peretelui celular; cu toate acestea, are o activitate bactericidă mai lentă in vitro., Odată cu utilizarea excesivă a acestuia, s-au raportat susceptibilități reduse și apariția heterorezistenței vancomicinei în S aureus.20,21 creșterea într-o subpopulatie de S aureus cu concentrația minimă inhibitorie (CMI) a >2 mcg/mL la vancomicină (denumite MIC ticălos) este asociat cu ambele microbiologice și clinice eșec. Comitetul Național pentru standarde clinice de laborator (NCCLS) a propus noi valori critice pentru vancomicină—schimbarea CMI pentru „sensibile” de la ≤4 mcg/mL la ≤2 mcg/mL.,22 rațiunea acestei propuneri se bazează parțial pe observațiile clinice anecdotice ale eșecurilor tratamentului în timpul tratamentului cu doze standard de vancomicină la pacienții cu CMI de 4 mcg/mL. În plus, pot fi necesare concentrații minime mai mari (de exemplu, concentrații minime de 15-20 mcg/mL) pentru infecții grave, cum ar fi pneumonia și osteomielita, datorită penetrării slabe a țesuturilor de către vancomicină. Au existat unele rapoarte anecdotice privind posibila nefrotoxicitate asociată cu aceste concentrații minime mari.,
Jeffres et al au prezentat un rezumat în 2006 Interscience Conferință pe Agenți Antimicrobieni și Chimioterapie (ICAAC) care a analizat riscul de nefrotoxicitate cu mai mare vancomicină niveluri minime.23 În studiul lor, au raportat cu 30% riscul de nefrotoxicitate (definită ca o creștere de 0,5 mg/dL sau creștere de 50% a creatininei serice față de valoarea inițială) la pacienții cu vancomicină niveluri minime de 315 mcg/mL, comparativ cu 13% la pacienții cu niveluri minime <15 mcg/mL.Unele populații de pacienți prezintă un risc mai mare de dezvoltare a nefro-toxicității induse de vancomicină., Acestea includ factori de risc cunoscuți, cum sunt vârsta înaintată, boala critică, funcția renală scăzută și utilizarea concomitentă a altor medicamente nefrotoxice, cum sunt aminoglicozidele. Toți acești factori au dus la o creștere a nevoii și utilizării agenților mai noi.
Linezolid (Zyvox) este primul oxazolidinone aprobat pentru tratamentul pielii și țesuturilor moi infecții, bacteriemie, și comunitatea și pneumonie nosocomială cauzată de MRSA.24 inhibă inițierea sintezei proteinelor la ribozomul 50S; cu toate acestea, spre deosebire de majoritatea celorlalte medicamente, este un agent bacteriostatic., Avantajele utilizării sale includ disponibilitatea unei formulări orale care are proprietăți excelente de biodisponibilitate, fără a fi necesară ajustarea dozei la pacienții cu insuficiență renală, inclusiv la cei care primesc terapii de substituție renală. Un factor limitativ al utilizării sale, în special pentru durata extinsă a tratamentului, este mielosupresia la pacienții care au primit linezolid mai mult de 14 zile.24,25 deși este disponibil ca o formulare orală, nu este utilizat la fel de mult în ambulatoriu datorită costului său., De asemenea, nu este acoperit de multe polițe de asigurare, astfel încât este posibil ca pacienții să fie nevoiți să utilizeze programele de asistență pentru pacienți ale producătorului. Daptomicina (Cubicin), un antibiotic lipopeptidic cu activitate bactericidă rapidă, este aprobat pentru tratamentul infecțiilor complicate ale pielii și țesuturilor moi, precum și a bacteriemiei cauzate de MRSA.26 mecanismul său de acțiune implică depolarizarea peretelui celular bacterian. Efectele secundare ale daptomicinei includ creatinkinaza crescută (CK) și rabdomioliza, în special la pacienții care iau inhibitori concomitenți ai HMG-CoA reductazei (statine)., Prin urmare, nivelurile săptămânale de CK trebuie să fie trase în timp ce un pacient primește daptomicină. De asemenea, trebuie remarcat faptul că au fost raportate cazuri de rezistență MRSA la daptomicină, în special la utilizarea prelungită și la pacienții cu expunere anterioară la vancomicină.26-28 Daptomicina nu trebuie utilizată pentru tratamentul pneumoniei MRSA, deoarece activitatea sa este inhibată de surfactanții pulmonari.
Quinupristin-dalfopristin (Synercid) este un streptogramin care are activitate împotriva MRSA., Deși nu este aprobat de FDA pentru utilizare în infecțiile cu MRSA, este utilizat în infecțiile cutanate și ale țesuturilor moi la pacienții care prezintă intoleranță sau nu la terapia cu vancomicină. Deoarece acest tratament a fost slab tolerat de către pacienți, utilizarea sa este limitată în practica clinică.29 unele dintre evenimentele adverse majore includ hiperbilirubinemia, mialgiile și artralgiile. Pe baza acestor factori, acest agent este utilizat doar ca o ultimă opțiune atunci când pacienții au eșuat sau nu pot tolera alți agenți., tigeciclina (Tygacil) este primul agent bacteriostatic din clasa glicilciclinelor de antibiotice (un derivat sintetic al tetraciclinei). Este indicat pentru tratamentul infecțiilor complicate ale pielii și structurii pielii (cSSSI), infecțiilor intraabdominale complicate și pneumoniei comunitare cauzate de MRSA.30 tigeciclina nu trebuie utilizată în mod obișnuit pentru bacteriemie din cauza preocupărilor legate de atingerea unor niveluri serice inadecvate., Deoarece tigeciclina este un antibiotic cu spectru larg, utilizarea sa trebuie limitată la infecții grave și care pun viața în pericol la pacienții spitalizați. Telavancin (Vibativ) este cel mai nou medicament care urmează să fie aprobat de FDA pentru tratamentul infecțiilor cu MRSA.31 este o lipoglicopeptidă similară cu vancomicina, deși mecanismul său de acțiune diferă. Telavancinul perturbă permeabilitatea membranei celulare prin depolarizarea membranei plasmatice, crescând permeabilitatea și scurgerea adeno-trifosfatului celular și a potasiului (K+)., Momentul acestor modificări se corelează cu pierderea rapidă, dependentă de concentrație a viabilității bacteriene, sugerând că activitatea bactericidă timpurie a telavancinului rezultă din disiparea potențialului membranei celulare și o creștere a permeabilității membranei. studiile clinice au arătat că telavancinul nu este inferior vancomicinei în tratamentul cSSSI.32,33 un avantaj pe care telavancin îl are față de vancomicină este administrarea o dată pe zi și nu este necesară monitorizarea nivelurilor de medicament. Cu toate acestea, ca și vancomicina, doza trebuie ajustată la pacienții cu insuficiență renală.,Funcția renală trebuie monitorizată în timpul și după întreruperea tratamentului la toți pacienții. Telavancinul este asociat cu prelungirea QTc și trebuie utilizat cu precauție la pacienții tratați cu medicamente care ar putea prelungi și QTc. În studiile clinice care au comparat telavancinul cu vancomicina, reacțiile adverse raportate la mai mult de 10% dintre pacienții tratați cu telavancin au inclus tulburări ale gustului, greață, vărsături și urină spumoasă.31 evenimente adverse grave au fost raportate la 7% dintre pacienții tratați cu telavancin și au inclus cel mai frecvent evenimente renale, respiratorii sau cardiace., Există o cutie neagră de avertizare privind fetal risc asociat cu telavancin folosit; astfel, femeile aflate la vârsta fertilă trebuie să aibă un ser test de sarcină înainte de a începe telavancin.31
ceftobiprol (Zeftera) este prima cefalosporină cu activitate bactericidă împotriva MRSA. Activitatea sa antibacteriană include inhibarea proteinelor de legare a penicilinei implicate în sinteza peretelui celular. În studiile clinice, a fost la fel de eficace ca și combinația de vancomicină și ceftazidimă în tratamentul cSSSI.,În general, este bine tolerat, cu principalele evenimente adverse la medicament, inclusiv greață și tulburări ale gustului. Ceftobiprola în prezent nu este aprobat pentru utilizare în SUA, și, deși a fost anterior aprobate pentru utilizare în Canada, producătorul întrerupt vânzarea de droguri din aprilie 16, 2010.35 fost următoarele recomandări de organismele de reglementare din Europa (European Comitetul pentru Produse Medicamentoase de Uz Uman) și SUA (FDA) să nu aprobe droguri., Deși rezultatele de fază III au sugerat beneficii ale ceftobiprolului, au existat preocupări cu privire la integritatea acestor rezultate ale studiului din cauza modificării datelor clinice din unele dintre locurile de studiu. Odată cu această evoluție recentă, viitorul utilizării ceftobiprolului pe piața americană rămâne discutabil.
concluzie
odată cu apariția CA-MRSA, precum și a MRSA hetero-rezistentă, este important ca farmaciștii să fie familiarizați cu toți agenții disponibili pentru tratamentul infecțiilor cu MRSA. De asemenea, este esențial să alegeți agentul antimicrobian adecvat pentru infecția tratată., În plus, medicamentele cu un spectru mai larg de activitate (de exemplu, tigeciclina) trebuie rezervate infecțiilor foarte severe și în contextul infecțiilor multipatogene. De asemenea, este extrem de important să rezervăm agenții mai noi pentru infecții mai severe pentru a minimiza dezvoltarea rezistenței.
1. Boucher HW, Corey GR. Epidemiologia Staphylococcus aureus rezistent la meticilină. Clin Infecta Dis.
2. Styers D, Sheehan DJ, Hogan P, și colab., Supravegherea bazată pe laborator a modelelor și tendințelor actuale de rezistență antimicrobiană în rândul Staphylococcus aureus: statutul 2005 în Statele Unite. Ann Clin Microbiol Antimicrob. 2006;5:2.
3. Chien JW, Kucia ML, Salata RA. Utilizarea linezolidului, o oxazolidinonă, în tratamentul infecțiilor bacteriene gram-pozitive multidrog rezistente. Clin Infecta Dis. 2000;30:146-151.
4. Soriano A, Martinez JA, Mensa J, și colab. Semnificația patogenă a rezistenței la meticilină pentru pacienții cu bacteremie Staphylococcus aureus. Clin Infecta Dis. 2000;30:368-673.
5. Graffunder EM, Venezia RA., Factorii de risc asociați cu infecția nosocomială cu Staphylococcus aureus rezistent la meticilină (MRSA), inclusiv utilizarea anterioară a antimicrobienelor. J Antimicrob Chemother. 2002;49:999-1005.
6. Klevens RM, Edwards JR, Tenover FC, et al. Modificări în epidemiologia Staphylococcus aureus rezistent la meticilină în unitățile de terapie intensivă din spitalele americane, 1992-2003. Clin Infecta Dis.
7. Levine DP, Cushing RD, Jui J, Brown WJ. Endocardită Staphylococcus aureus rezistentă la meticilină dobândită în Comunitate în Centrul Medical din Detroit. Ann Intern Med. 1982;97:330-338.
8., Lodise TP Jr, McKinnon PS, Rybak M. model de predicție pentru identificarea pacienților cu bacteriemie Staphylococcus aureus cu risc de rezistență la meticilină. Infecta Controlul Hosp Epidemiol. 2003;24:655-661.
9. Regele MD, Humphrey BJ, Wang YF, și colab. Apariția clonei Staphylococcus aureus USA 300, rezistentă la meticilină, dobândită în comunitate, ca cauză predominantă a infecțiilor cutanate și ale țesuturilor moi. Ann Intern Med. 2006;144:309-317.
10. Centrele pentru Controlul și Prevenirea Bolilor., Infecții Staphylococcus aureus rezistente la meticilină în rândul participanților sportivi competitivi-Colorado, Indiana, Pennsylvania și județul Los Angeles, 2000-2003. MMWR. 2003;52:793-795.
11. Lowy FD. Infecții cu Staphylococcus aureus. În Engl J Med. 1998;339:520-532.
12. Chambers HF. Epidemiologia în schimbare a Staphylococcus aureus? Emerg Infecta Dis.
13. Informații MRSA asociate comunității pentru clinicieni. CDC. www.cdc.gov/ncidod/dhqp/ar_ 2008; 46 (supl 5): S344-s349. 2006;42:389-391. 2001;7:178-182.doamna doctor.html. Accesat 4 Iulie 2010.
14. Rybak MJ, LaPlante KL., Staphylococcus aureus rezistent la meticilină asociată comunității; o revizuire. Farmacoterapie. 2005;25:74-85.
15. Gornwitz RJ, Jernigan DB, Powers JH, și colab. Strategii pentru managementul clinic al MRSA în comunitate: rezumatul unei întâlniri de experți convocate de Centrele pentru Controlul și Prevenirea Bolilor. Martie 2006. www.cdc.gov/ncidod/dhqp/pdf/ar/CAMRSA_ExpMtgStrategies.pdf. accesat la 4 iulie 2010.
16. Sabol KE, Echevarria KL, Lewis JS II. Staphylococcus aureus rezistent la meticilină asociat comunității: bug nou, medicamente vechi. Ann Pharmacother. 2006;40:1125-1133.
17., Introducerea pachetului Cleocin (clindamycin). New York, NY: Pfizer Inc; noiembrie 2005.
18. Strom BL, Schinnar R, Apter AJ, și colab. Absența sensibilității încrucișate între antibioticele sulfonamide și nonantibioticele sulfonamide. În Engl J Med. 2003;349:1628-1635.
19. Nicolau DP, Freeman CD, Nightingale CH, și colab. Minociclină versus vancomicină pentru tratamentul endocarditei experimentale cauzate de Staphylococcus aureus rezistent la oxacilină. Agenți Antimicrob Chemother. 1994;38:1515-1518.
20. Sakoulas G, Moellering RC Jr., Creșterea rezistenței la antibiotice în rândul tulpinilor de Staphylococcus aureus rezistente la meticilină. Clin Infecta Dis. 2008; 46 (supl 5):S360-s367.
21. Rybak MJ, Akins RL. Apariția Staphylococcus aureus rezistent la meticilină cu rezistență intermediară la glicopeptide: semnificație clinică și opțiuni de tratament. Droguri. 201;61:1-7.
22. Tenover FC, Moellering RC Jr. rațiunea pentru revizuirea Standarde Clinice și de Laborator Institutul de vancomicină concentratiei minime inhibitorii criterii de interpretare pentru Staphylococcus aureus. Clin Infecta Dis. 2007;44:1208-1215.
23., Jeffres MN, Micek ST, Isakow W, și colab. Incidență crescută a nefrotoxicității cu concentrații plasmatice minime mai mari de vancomicină. Programul și rezumatele Conferinței Interscience 46th privind agenții antimicrobieni și chimioterapia (ICAAC); septembrie 27-30, 2006; San Francisco, CA. Rezumat K789.
24. Zyvox (linezolid) prospect. New York, NY: Pfizer Inc; decembrie 2009.
25. Kuter DJ, Tillotson GS. Efectele hematologice ale antimicrobiene, un accent pe oxazolidinona, linezolid. Farmacoterapie. 201;21:1010-1013.
26. Cubicin (daptomicină) prospectul., Lexington, MA: Cubist Pharmaceuticals; January 2010.
27. Murthy MH, Olson ME, Wickert RW, et al. Daptomycin non-susceptible methicillin-resistant Staphylococcus aureus USA 300 isolate. J Med Microbiol. 2008;57:1036-1038.
28. Mangili A, Bica I, Snydman R, Hamer DH. Daptomycin-resistant methicillin-resistant Staphylococcus aureus bacteremia. Clin Infect Dis. 2005;40:1058-1060.
29. Synercid (quinupristin-dalfopristin) package insert. Greenville, NC: Monarch Pharmaceuticals; June 2008.
30. Tygacil (tigecycline) package insert. Philadelphia, PA: Wyeth Pharmaceuticals; September 2009.,
31. Vibativ (telavancin) prospect. Deerfield, IL: Astellas Pharma US, Inc; septembrie 2009.
32. Stryjewski ME, Chu VH, O ‘ Riordan WD, și colab. Telavancin versus terapia standard pentru tratamentul infecțiilor complicate ale pielii și structurii pielii cauzate de bacteriile gram pozitive: studiu FAST 2. Agenți Antimicrob Chemother. 2006;50:862-867.
33. Corey GR. Studii de telavancin în cSSSI. Lucrare prezentată la: al treilea Simpozion Internațional privind infecțiile Gram-pozitive rezistente; 10 octombrie 2006; Niagara-on-the-Lake, Canada.
34. Vidaillac C, Rybak MJ., Ceftobiprole: first cephalosporin with activity against methicillin-resistant Staphylococcus aureus. Pharmacotherapy. 2009;29:511-525.
35. Discontinuation of the sale of ceftobiprole in Canada. Basilea Pharmaceutica. April 9, 2010. http://hugin.info/134390/R/1401931/356785.pdf. Accessed July 12, 2010.
36. Vibramycin (doxycycline) package insert. New York, NY: Pfizer Inc; April 2007.
37. Minocin (minocycline) package insert. Philadelphia, PA: Triax Pharmaceuticals; March 2006.
38. Bactrim (trimethoprim-sulfamethoxazole) package insert. Philadelphia, PA: AR Scientific; November 2006.
39., Vancocin (vancomycin) package insert. Exton, PA: ViroPharma Inc; October 2005.