reacții de precipitare și reguli de solubilitate
o reacție de precipitare este una în care substanțele dizolvate reacționează pentru a forma unul (sau mai multe) produse solide. Multe reacții de acest tip implică schimbul de ioni între compușii ionici în soluție apoasă și sunt uneori denumite reacții de deplasare dublă, înlocuire dublă sau metateză., Aceste reacții sunt comune în natură și sunt responsabile pentru formarea recifelor de corali în apele oceanelor și a pietrelor la rinichi la animale. Ele sunt utilizate pe scară largă în industrie pentru producerea unui număr de produse chimice de bază și de specialitate. Reacțiile de precipitare joacă, de asemenea, un rol central în multe tehnici de analiză chimică, inclusiv teste spot utilizate pentru identificarea ionilor metalici și metode gravimetrice pentru determinarea compoziției materiei (Vezi ultimul modul al acestui capitol).,
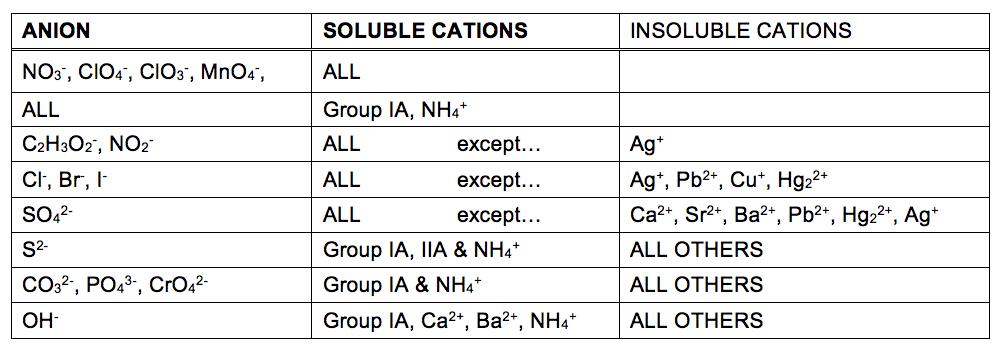
măsura în care o substanță poate fi dizolvată în apă sau orice solvent este exprimată cantitativ ca solubilitate, definită ca concentrația maximă a unei substanțe care poate fi obținută în condiții specificate. Se spune că substanțele cu solubilități relativ mari sunt solubile. O substanță va precipita atunci când condițiile de soluție sunt de așa natură încât concentrația sa depășește solubilitatea. Se spune că substanțele cu solubilități relativ scăzute sunt insolubile, iar acestea sunt substanțele care precipită ușor din soluție., Mai multe informații despre aceste concepte importante sunt furnizate în capitolul text privind soluțiile. În scopul prezicerii identităților solidelor formate prin reacții de precipitare, se poate referi pur și simplu la modele de solubilitate care au fost observate pentru mulți compuși ionici (Tabelul 1).
Un exemplu viu de precipitații se observă atunci când soluții de iodură de potasiu și azotat de plumb sunt amestecate, care rezultă în formarea de pistă solidă iodură:
Această observație este în concordanță cu solubilitate orientări: singurul compus insolubil între toți cei implicați este iodură de plumb, una dintre excepțiile de la general solubilitatea iodurii de săruri.,
net ionic ecuația care reprezintă această reacție este:
iodură de Plumb este de un galben strălucitor solid, care a fost anterior folosit ca un artist pigment cunoscut sub numele de iod galben (Figura 1). Proprietățile cristalelor PbI2 pure le fac utile pentru fabricarea detectoarelor de raze X și gamma.

masa De solubilitate în Tabelul 1 pot fi folosite pentru a prezice dacă un raport de reacție va apărea atunci când soluțiile solubile compuși ionici sunt amestecate împreună. Trebuie doar să identificați toți ionii prezenți în soluție și apoi să luați în considerare dacă este posibil asocierea cation/anion ar putea duce la un compus insolubil.de exemplu, soluțiile de amestec de nitrat de argint și fluorură de sodiu vor produce o soluție care conține ioni Ag+, NO3−, Na+ și F., În afară de cei doi compuși ionici prezenți inițial în soluții, AgNO3 și NaF, doi compuși ionici suplimentari pot fi derivați din această colecție de ioni: NaNO3 și AgF.tabelul de solubilitate indică faptul că toate sărurile de nitrați sunt solubile, dar că AgF este una dintre excepțiile de la solubilitatea generală a sărurilor de fluor. Prin urmare, se preconizează că va apărea o reacție de precipitare, așa cum este descrisă de următoarele ecuații: