Introdução
Um dos mais importantdiscoveries no campo da microscopia fluorescente foi encontrado em uma água-viva na década de 1960. Osamu Shimomura, da Universidade de Princeton estava estudando Aequorea victoria, um bioluminescente água-viva., Ele deve benoted aqui que luminescência não é o mesmo que fluorescência:
- Luminescência: a emissão espontânea de luz a partir de uma substância (quando essa substância é um animal, é chamado de bioluminescência)
- Fluorescência: emissão de luz a partir de uma substância que absorve a luz e torna-se excitado
Através do estudo de A. victoria, duas importantes proteínas foram descobertos: aequorin (um photoprotein), e a proteína verde fluorescente (GFP). A Medusa produz cálcio, que interage com aequorina e produz luminescência azul., Esta luz azul é absorvida pelo GFP e re-emitida como fluorescência verde. Estas proteínas têm sido isoladas e purificadas a partir das medusas e são usadas pesadamente em pesquisa até hoje. Por esta pesquisa, Osamu Shimomura e colegas ganharam o Prêmio Nobel de Química em 2008.
proteína verde fluorescente
GFP é excitada pela luz na porção azul/violeta/ultravioleta do espectro e emite luz na porção verde (daí o nome). A estrutura da proteína pode ser vista na Fig.1., GFP é uma forma de barril com a porção fluorescente (o cromóforo) composta de apenas três aminoácidos. Quando este cromóforo absorve luz azul, emite fluorescência verde.
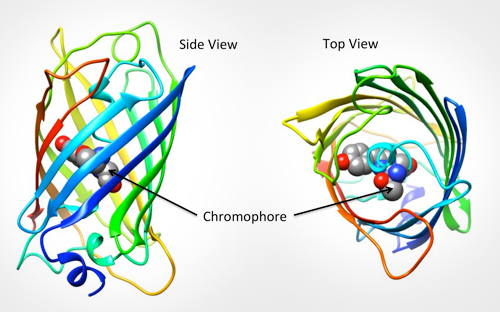
GFP Em Pesquisa
O uso de GFP em pesquisa tornou-se clara uma vez que o gene da GFP foi também isolado e GFP pode ser adicionado às células ou organismos geneticamente enxertados em organismos vivos. Algumas aplicações e vantagens do GFP discutidas abaixo.
GFP como marcador de toxicidade: devido ao fato de que GFP diminui na intensidade de fluorescência com o aumento da toxicidade, ele pode ser usado como marcador de toxicidade ambiental., GFP pode ser adicionado aos organismos hospedeiros sem efeito negativo, e então a intensidade rastreada através de diferentes ambientes em vários organismos.
GFP é hereditária, se um organismo tem GFP bateu em seu genoma, GFP será, naturalmente, ser passados a prole, sem qualquer adicional de processos, permitindo a não-invasiva formas de introduzir um marcador fluorescente e a segui-lo através de gerações de animais ou células. GFP não interfere com nenhum processo biológico., Ratos transgênicos podem ser rotulados com GFP, que é facilmente observado em sua descendência apenas expondo-os à luz azul ou UV, como visto na Fig.2.
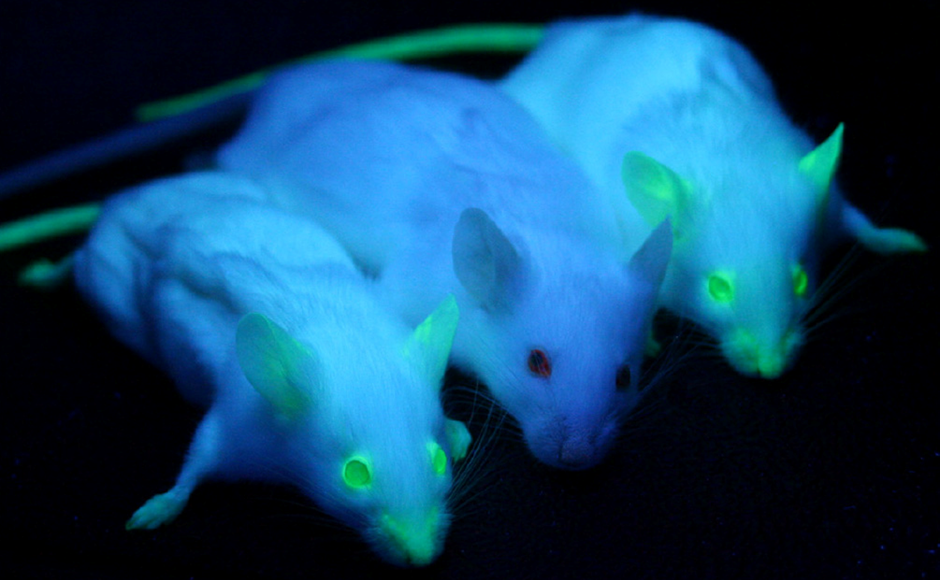
GFP pode ser fundido a outras proteínas, efetivamente tornando essas proteínas fluorescentes. Isto pode ser feito com linkers especiais de modo que GFP não afeta a função da proteína de interesse, e ainda pode se difundir através das células. Isto permite que qualquer proteína seja localizada e rastreada usando microscopia fluorescente padrão, através de uma luz azul sobre as células, a proteína de interesse irá fluorescer de volta com uma luz verde.,
GFP em experimentos com células vivas: a molécula fluorescente verde clássica é o isotiocianato de fluoresceína (FITC), mas isso é tóxico para as células e não pode ser usado diretamente sem primeiro fixar as células ou causar danos inevitáveis. GFP é muito menos prejudicial, pois é uma proteína de ocorrência natural e pode ser usado em experimentos em células vivas, ao mesmo tempo causando praticamente nenhum dano, especialmente se for transmitida para a descendência.GFP em aplicações microscópicas avançadas., Várias aplicações de microscopia de fluorescência, tais como recuperação de fluorescência após fotobleaching (FRAP) e Transferência de energia de ressonância Förster (FRET) foram desenvolvidas com GFP, permitindo aos pesquisadores usar aplicações cada vez mais específicas e poderosas de fluorescência para suas imagens. Estas técnicas são descritas em outros artigos curtos, nomeadamente o que é FRET e o que é FRAP?
GFP é modificável, como o código genético e aminoácido para GFP é bem entendido que tem sido sujeito a várias modificações., Primeiro GFP foi modificado para produzir GFP melhorado (eGFP), que aumentou a intensidade de fluorescência, maior fotostabilidade, picos de excitação mais convenientes e maior eficiência à temperatura ambiente. Modificações diretamente ao cromóforo permitem que o GFP fluoresca com diferentes cores, criando azul (BFP), ciano (CFP), amarelo (YFP), vermelho (RPP) e outros, todos os quais foram melhorados separadamente e têm suas próprias aplicações. Algumas modificações destacadas incluem mCherry (vermelho), Citrina e Vênus (amarelo), e Cerulean (ciano) para nomear alguns., Famílias inteiras de proteínas fluorescentes agora existem, todas derivadas do GFP original, como visto na Fig.3.
Resumo
GFP é uma parte fundamental da microscopia de fluorescência devido à facilidade de uso e as aplicações estão sendo limitado apenas pela pesquisadora da imaginação. Melhorias constantes no GFP ao longo do tempo têm causado microscopia de fluorescência e pesquisa para avançar, devido à natureza altamente flexível do GFP e o grande corpo de pesquisa baseada no uso do GFP e suas muitas variantes.