Reações de Precipitação e a Solubilidade Regras
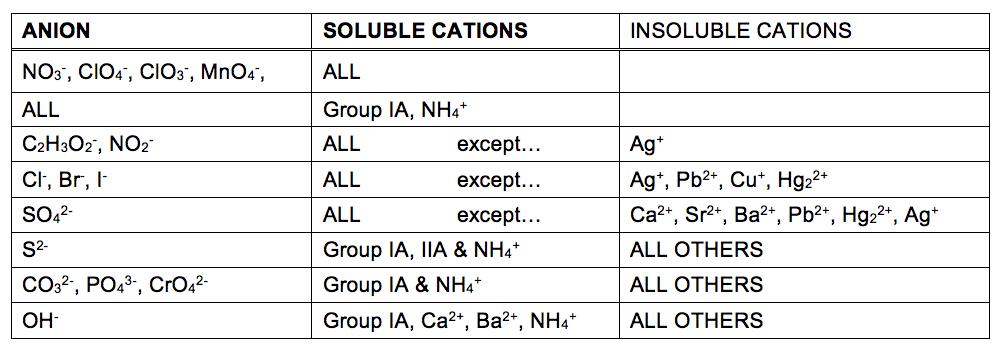
Uma reacção de precipitação é aquele em que as substâncias dissolvidas reagem para formar um (ou mais) de produtos sólidos. Muitas reações deste tipo envolvem a troca de íons entre compostos iônicos em solução aquosa e são por vezes referidas como deslocamento duplo, substituição dupla, ou reações de metatese., Estas reacções são comuns na natureza e são responsáveis pela formação de recifes de coral em águas oceânicas e pedras renais em animais. Eles são amplamente utilizados na indústria para a produção de uma série de produtos e especialidades químicas. Reações de precipitação também desempenham um papel central em muitos químicos técnicas de análise, incluindo o lugar testes utilizados para identificar íons metálicos e gravimétricos métodos para determinar a composição da matéria (ver o último módulo deste capítulo).,a medida em que uma substância pode ser dissolvida em água ou em qualquer solvente é quantitativamente expressa como a sua solubilidade, definida como a concentração máxima de uma substância que pode ser atingida em condições especificadas. Diz-se que substâncias com solubilidades relativamente grandes são solúveis. Uma substância precipita-se quando as condições da solução forem tais que a sua concentração exceda a sua solubilidade. Diz-se que as substâncias com solubilidades relativamente baixas são insolúveis, e estas são as substâncias que precipitam facilmente da solução., Mais informações sobre estes conceitos importantes são fornecidas no capítulo de texto sobre soluções. Para efeitos de previsão das identidades dos sólidos formados por reações de precipitação, pode-se simplesmente referir a padrões de solubilidade que têm sido observados para muitos compostos iônicos (Tabela 1).
Um exemplo vívido de precipitação é observado quando as soluções de iodeto de potássio e nitrato de chumbo são misturados, resultando na formação de liderança sólida iodeto de:
Esta observação é consistente com a solubilidade diretrizes: O único composto insolúvel entre todos os envolvidos é de iodeto de chumbo, uma das exceções gerais de solubilidade do iodeto de sais.,
O líquido iônico equação que representa essa reação é:
iodeto de Chumbo é um sólido amarelo brilhante que antigamente era usado como uma artista de pigmento conhecido como o iodo amarelo (Figura 1). As propriedades dos cristais pbi2 puros tornam-nos úteis para a fabricação de detectores de raios X e gama.

a tabela de solubilidade na Tabela 1 pode ser usada para prever se uma reação de precipitação ocorrerá quando soluções de compostos iônicos solúveis forem misturados entre si. Basta identificar todos os íons presentes na solução e considerar se possível a combinação catião/anião poderia resultar em um composto insolúvel.por exemplo, a mistura de soluções de nitrato de Prata e fluoreto de sódio produz uma solução contendo Ag+, NO3−, na+ E F− iões., Além dos dois compostos iônicos originalmente presentes nas soluções, AgNO3 e NaF, dois compostos iônicos adicionais podem ser derivados desta coleção de íons: NaNO3 e AgF.a tabela de solubilidade indica que todos os sais de nitrato são solúveis, mas que o AgF é uma das excepções à solubilidade geral dos sais de fluoreto. Uma reação de precipitação, portanto, é prevista para ocorrer, conforme descrito pelas seguintes equações: