FUNDO
Princípio: Síntese da aspirina a partir do ácido salicílico ocorre pelo processo de acetilação em ácidos médio. O ácido salicílico interage com anidrido acético na presença de poucas gotas de ácido sulfúrico concentrado para produzir aspirina e uma molécula de ácido acético., O objetivo da adição de ácido sulfúrico (catalisador) é ajudar e aumentar o processo de remoção do íon acetato (CH3COO–) do anidrido acético que, em última análise, fica associado com íon h+ do grupo hidroxi fenólico em ácido salicílico para ser eliminado como um mole de ácido acético.Objectivo: preparar aspirina a partir do ácido salicílico.,
Reação:
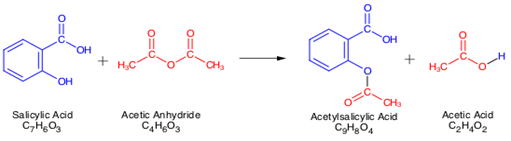
Mecanismo:
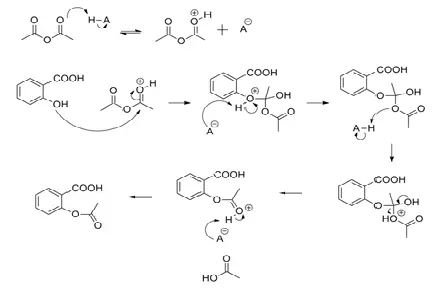
Utilização:
Utilizado para o alívio de pequenas dores/dores e também dor ligeira a moderada. Recomenda-se a profilaxia de enfarte do miocárdio para a artrite e artríticas relacionadas. Reduz o risco de crises isquémicas transitórias no homem.,
REQUIREMENTS
Chemicals: Salicylic acid – 6 g
Acetic anhydride – 8.,5 ml
Concentrated H2SO4 – 3-4 drops
Methylated spirit
Apparatus: Conical flask – 250 ml
Buchner funnel
Glass rod
Beaker
Filter paper
PROCEDURE
Weigh 6 gs of salicylic acid and transfer it to a clean and dry 250 ml conical flask. Add 8.,5 ml de anidrido acético e 3-4 gotas de ácido sulfúrico concentrado no frasco cuidadosamente e misturar cuidadosamente. Aquecer a mistura em banho-maria a 60 graus, cerca de 20 minutos, com agitação frequente. Deixar arrefecer o conteúdo do balão e vertê-lo em 100 ml de água fria, num copo de 250 ml, com agitação constante. Filtrar o produto bruto em um Funil Buchner usando sucção, lavar com água fria. Recrystallize from boiling water along with small quantities of methylated spirit. Secar o produto sintetizado numa estufa a 90 ° C e calcular o rendimento.,
cálculo
Aqui o reagente limitante é o ácido salicílico; portanto, o rendimento deve ser calculado a partir da sua quantidade tomada.
a fórmula Molecular do ácido salicílico = C7H6O3
a fórmula Molecular do ácido acetilsalicílico (aspirina) = C9H8O4
peso Molecular do ácido salicílico = 138 g/mole
peso Molecular de acetil salicílico (aspirina) = 180 g/mole
rendimento Teórico:
138 g de ácido salicílico dá 180 g de ácido acetilsalicílico
Portanto, 6 g de ácido salicílico vai dar ? (X) g de aspirina =( 180 × 6)/138 = 7.,82 g
rendimento Teórico = 7.82 g
Prático rendimento = – – – – – – g
% Rendimento = (Prático de Produção)/(Rendimento Teórico) × 100
CONCLUSÃO
Aspirina foi sintetizada e o rendimento foi encontrado para ser — %. (O produto é obtido na forma de cristais incolores, produzindo 11 g E M. P. 136-137 °C.)