tło
zasada: synteza aspiryny z kwasu salicylowego odbywa się w procesie acetylacji w środowisku kwaśnym. Kwas salicylowy wchodzi w interakcję z bezwodnikiem octowym w obecności kilku kropli stężonego kwasu siarkowego w celu wytworzenia aspiryny i cząsteczki kwasu octowego., Celem dodania kwasu siarkowego (katalizatora) jest wspomaganie i wspomaganie procesu odłączania jonu octanu (CH3COO–) od bezwodnika octowego, który ostatecznie wiąże się z Jonem H+ z fenolowej grupy hydroksylowej w kwasie salicylowym, który ma zostać wyeliminowany jako mol kwasu octowego.1
cel: przygotowanie aspiryny z kwasu salicylowego.,
reakcja:
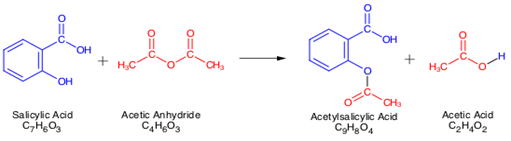
Mechanizm:
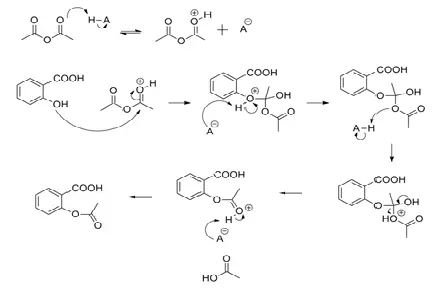
zastosowanie:
stosowany do łagodzenia drobnych bólów/bólów, a także łagodnego do umiarkowanego bólu. Zaleca się w przypadku zapalenia stawów i związanych z nimi Stanów artretycznych, profilaktyki zawału mięśnia sercowego. Zmniejsza ryzyko przemijających ataków niedokrwiennych u mężczyzn.,
REQUIREMENTS
Chemicals: Salicylic acid – 6 g
Acetic anhydride – 8.,5 ml
Concentrated H2SO4 – 3-4 drops
Methylated spirit
Apparatus: Conical flask – 250 ml
Buchner funnel
Glass rod
Beaker
Filter paper
PROCEDURE
Weigh 6 gs of salicylic acid and transfer it to a clean and dry 250 ml conical flask. Add 8.,5 ml bezwodnika octowego i 3-4 krople stężonego kwasu siarkowego do kolby ostrożnie i dokładnie wymieszać. Podgrzać mieszaninę na łaźni wodnej w temperaturze 60 stopni około 20 min z częstym mieszaniem. Pozostawić zawartość kolby do ostygnięcia i wlać do 100 ml zimnej wody w zlewce 250 ml ze stałym mieszaniem. Odfiltrować surowy produkt na lejku Buchnera za pomocą ssania, umyć zimną wodą. Rekrystalizować z wrzącej wody wraz z małymi ilościami spirytusu metylowanego. Wysusz zsyntetyzowany produkt w piekarniku w temperaturze 90 °C i Oblicz wydajność.,
Obliczanie
tutaj odczynnikiem ograniczającym jest kwas salicylowy, stąd wydajność należy obliczać na podstawie jego ilości pobranej.
Wzór cząsteczkowy kwasu salicylowego = C7H6O3
Wzór cząsteczkowy kwasu acetylosalicylowego (aspiryna) = C9H8O4
Masa cząsteczkowa kwasu salicylowego = 138 g/mol
Masa cząsteczkowa kwasu acetylosalicylowego (aspiryna) = 180 g/mol
Wydajność teoretyczna:
138 g kwasu salicylowego daje 180 g aspiryny
dlatego 6 g kwasu salicylowego da ? (X) G aspiryny
X =( 180 × 6)/138 = 7.,82 g
teoretyczna wydajność = 7,82 g
praktyczna wydajność = – – – – g
% wydajność = (praktyczna Wydajność)/(teoretyczna wydajność) × 100
podsumowanie
Aspiryna została zsyntetyzowana, a wydajność ustalono na – – -%. (Produkt otrzymuje się w postaci bezbarwnych kryształów, wydajność 11 g I m.p. 136-137 °C.)