US Pharm. 2010; 35 (8):HS2-HS4.
oporny na metycylinę Staphylococcus aureus (MRSA) jest jedną z głównych przyczyn zakażeń zarówno w opiece zdrowotnej, jak i w społeczności lokalnej.1,2 zakażenia spowodowane MRSA są związane z wysokim ryzykiem zachorowalności i śmiertelności i prowadzą do wysokich kosztów opieki zdrowotnej.3-5 częstość występowania zakażeń MRSA w Stanach Zjednoczonych stale wzrastała w ciągu ostatnich kilku lat z 22% w 1995 r.do 60% w 2003 r.,6 health care–associated MRSA (HA-MRSA) jest związana ze szpitalami i placówkami opieki długoterminowej i jest częsta u pacjentów z długotrwałą hospitalizacją, poprzednim zastosowaniem przeciwdrobnoustrojowym, wrzodami dekubitowymi, dializami, cewnikami zamieszkującymi, karmieniami dojelitowymi lub nadużywaniem narkotyków w wywiadzie.7,8 w ostatnich latach nastąpił jednak wzrost nowego szczepu MRSA o nazwie community-associated MRSA (CA-MRSA)., Wydaje się, że jest to nabywane w warunkach ambulatoryjnych, a transmisja odbywa się poprzez bliski kontakt fizyczny, taki jak w ośrodkach opieki dziennej, rezerwatach indyjskich i zakładach poprawczych oraz wśród sportowców, personelu wojskowego i mężczyzn, którzy uprawiają seks z mężczyznami.7,9,10
rozróżnianie szczepów MRSA
kilka doniesień ujawniło różnice między szczepami HA-MRSA i CA-MRSA, w tym obecność różnych genotypów między tymi dwoma szczepami. CA-MRSA jest wrażliwy na kilka antybiotyków nie-beta-laktamowych, podczas gdy szczepy HA-MRSA nie są., Szczepy CA-MRSA są bardziej narażone na kodowanie pewnych czynników zjadliwych, które były związane z ciężkim zapaleniem płuc (zwłaszcza u dzieci) oraz zakażeniami skóry i tkanek miękkich u dorosłych.8,11,12 CDC ustanowiło kryteria odróżniania CA-MRSA od HA-MRSA. Wytyczne te obejmują izolację pozytywnej kultury MRSA w ciągu 48 godzin od przyjęcia pacjenta do szpitala. Aby zostać uznanym za CA-MRSA, pacjent nie może mieć żadnej z następujących czynności: niedawna hospitalizacja; przyjęcie do domu opieki, hospicjum lub wykwalifikowanego zakładu pielęgniarskiego; dializa; lub niedawna operacja., Pacjent nie może również posiadać cewników ani innych wyrobów medycznych.13
leczenie CA-MRSA
CDC zaleca, aby zarządzanie i zapobieganie ognisk CA-MRSA obejmować pokrycie infekcji, które wytwarzają ropę, mycie rąk często, nie dzielenie się rzeczami osobistymi, mycie zabrudzonej pościeli i odzieży gorącą wodą oraz suszenie tkanin w suszarce na gorąco w porównaniu z suszeniem powietrzem.W przypadku ropni skórnych leczenie obejmuje nacięcie i drenaż ropni z antybiotykami ogólnoustrojowymi lub bez nich, w zależności od ciężkości zakażenia.,14
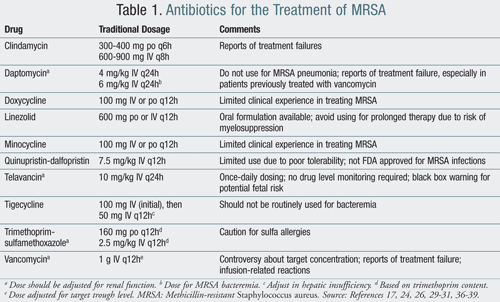
leczenie CA-MRSA zwykle obejmuje stosowanie środków takich jak klindamycyna, tetracykliny i trimetoprim-sulfametoksazol (TMP-SMX). Antybiotyk ryfampicyna nigdy nie powinna być stosowana w monoterapii w leczeniu MRSA. Oporność rozwija się szybko z ryfampicyną w monoterapii; jednak, gdy stosuje się ją w połączeniu z innym środkiem przeciw MRSA, może skuteczniej eliminować organizmy z miejsc nośnych.15 wyżej wymienione antybiotyki są zwykle wykonalnymi opcjami leczenia u pacjentów leczonych w warunkach ambulatoryjnych., W ciężkich zakażeniach wymagających hospitalizacji odpowiednie terapie można zastosować antybiotyki dożylne, w tym wankomycynę, linezolid, chinuprystynę-dalfoprystynę, daptomycynę, tygecyklinę i telawancynę (tabela 1).
chociaż klindamycyna (Kleocin) może być stosowana w leczeniu CA-MRSA, zgłaszano oporność do 19% u pacjentów leczonych tym lekiem. Dlatego pacjenci leczeni klindamycyną muszą być dokładniej monitorowani pod kątem rozwoju oporności wywołanej przez siebie.,Klindamycyna jest również związana z rozwojem zakażeń Clostridium difficile, co ogranicza jej stosowanie przez dłuższy czas.17
TMP-SMX (Bactrim) może być uważany za alternatywę dla leczenia wankomycyną w niektórych przypadkach zakażeń MRSA. Jednakże, podobnie jak w przypadku klindamycyny, istnieją doniesienia o niepowodzeniach leczenia. Terapia ta ma również ograniczone zastosowanie ze względu na wysoką częstość alergii na sulfonamidy, które donoszono o wystąpieniu do 10% populacji.,18
Minocyklina (Minocyna) i doksycyklina (Wibramycyna) są antybiotykami tetracyklinowymi stosowanymi w leczeniu MRSA. Dane dotyczące stosowania tych leków w MRSA są ograniczone, ale zgłaszano sukces kliniczny.19
leczenie HA-MRSA
antybiotyki pozajelitowe są uważane za złoty standard leczenia HA-MRSA. Od kilkudziesięciu lat szeroko stosowany jest antybiotyk glikopeptydowy wankomycyna.
Wankomycyna (Wankocyna) hamuje syntezę ścian komórkowych, jednak w warunkach in vitro wykazuje wolniejsze działanie bakteriobójcze., W związku z jej nadużywaniem zgłaszano zmniejszoną wrażliwość na wankomycynę oraz pojawienie się heterorezygacji wankomycyny U S aureus.20,21 wzrost subpopulacji S aureus o minimalnym stężeniu hamującym (Mic) >2 mcg / mL do wankomycyny (określanej jako MIC creep) jest związany zarówno z niepowodzeniem mikrobiologicznym, jak i klinicznym. National Committee for Clinical Laboratory Standards (NCCLS) zaproponował nowe wartości graniczne dla wankomycyny—zmiana MIC dla „wrażliwych” z ≤4 mcg/mL do ≤2 mcg/mL.,Uzasadnienie tego wniosku opiera się częściowo na anegdotycznych obserwacjach klinicznych niepowodzeń leczenia podczas leczenia standardowymi dawkami wankomycyny u pacjentów z MIC 4 µg / mL. Ponadto, wyższe minimalne poziomy (tj. minimalne poziomy 15-20 µg/mL) mogą być wymagane w przypadku ciężkich zakażeń, takich jak zapalenie płuc i zapalenie szpiku z powodu słabej penetracji tkanek przez wankomycynę. Istnieją niepotwierdzone doniesienia o możliwej nefrotoksyczności związanej z tymi wysokimi minimalnymi stężeniami.,
Jeffres i wsp.przedstawili streszczenie na konferencji Interscience Conference on Antimicrobial Agents and Chemotherapy (ICAAC) w 2006 r., która dokonała przeglądu ryzyka nefrotoksyczności przy wyższych poziomach minimalnych wankomycyny.W swoim badaniu zgłaszali oni 30% ryzyko nefrotoksyczności (definiowane jako zwiększenie o 0, 5 mg/dL lub zwiększenie stężenia kreatyniny w surowicy o 50% w stosunku do wartości wyjściowych) u pacjentów, u których minimalne stężenie wankomycyny wynosiło 315 µg/mL, w porównaniu do 13% u pacjentów, u których minimalne stężenie wankomycyny wynosiło <15 µg/mL.Niektóre populacje pacjentów są narażone na większe ryzyko wystąpienia nefrotoksyczności wywołanej wankomycyną., Należą do nich znane czynniki ryzyka, takie jak podeszły wiek, krytyczna choroba, upośledzenie czynności nerek oraz jednoczesne stosowanie innych leków nefrotoksycznych, takich jak aminoglikozydy. Wszystkie te czynniki doprowadziły do wzrostu zapotrzebowania i wykorzystania nowszych agentów.
Linezolid (Zyvox) jest pierwszym oksazolidynonem dopuszczonym do leczenia zakażeń skóry i tkanek miękkich, bacter-emia oraz miejscowego i szpitalnego zapalenia płuc wywołanego przez MRSA.Hamuje inicjację syntezy białek w rybosomie 50S; jednak, w przeciwieństwie do większości innych leków, jest środkiem bakteriostatycznym., Do zalet jego stosowania należy dostępność postaci doustnej o doskonałych właściwościach biodostępności, bez konieczności dostosowywania dawki u pacjentów z niewydolnością nerek, w tym u pacjentów otrzymujących terapie nerkozastępcze. Jednym z czynników ograniczających jego stosowanie, zwłaszcza przez dłuższy czas leczenia, jest zahamowanie czynności szpiku kostnego u pacjentów otrzymujących linezolid przez ponad 14 dni.24,25 chociaż dostępny jako preparat doustny, nie jest stosowany tak często w warunkach ambulatoryjnych ze względu na jego koszt., Nie jest również objęty wieloma polisami ubezpieczeniowymi, więc pacjenci mogą potrzebować skorzystać z programów pomocy pacjenta producenta.
Daptomycyna (Cubicin), antybiotyk lipopeptydowy o szybkim działaniu bakteriobójczym, jest dopuszczona do leczenia skomplikowanych infekcji skóry i tkanek miękkich, a także bakteriemii wywołanych przez MRSA.Jego mechanizm działania polega na depolaryzacji ściany komórkowej bakterii. Działania niepożądane daptomycyny obejmują zwiększenie aktywności kinazy kreatynowej (CK) i rabdomiolizy, zwłaszcza u pacjentów przyjmujących jednocześnie inhibitory reduktazy HMG-CoA (statyny)., W związku z tym, podczas przyjmowania daptomycyny przez pacjenta, należy cotygodniowe stężenie CK. Należy również zauważyć, że odnotowano przypadki oporności MRSA na daptomycynę, zwłaszcza przy długotrwałym stosowaniu i u pacjentów uprzednio narażonych na wankomycynę.26-28 Daptomycyny nie należy stosować w leczeniu zapalenia płuc wywołanego przez MRSA, ponieważ jej aktywność jest hamowana przez surfaktanty płucne.
Chinuprystyna-dalfoprystyna (Synercid) jest streptograminą wykazującą aktywność przeciwko MRSA., Chociaż nie jest zatwierdzony przez FDA do stosowania w zakażeniach MRSA, jest stosowany w zakażeniach skóry i tkanek miękkich u pacjentów, którzy nie tolerują lub nie stosują wankomycyny. Ponieważ leczenie to jest słabo tolerowane przez pacjentów, jego stosowanie jest ograniczone w praktyce klinicznej.Niektóre z głównych działań niepożądanych obejmują hiperbilirubinemię, bóle mięśniowe i bóle stawów. Na podstawie tych czynników lek ten jest stosowany tylko jako ostatnia opcja, gdy pacjenci zawiodli lub nie tolerują innych leków.,
Tygecyklina (Tygacil) jest pierwszym środkiem bakteriostatycznym z klasy glicylocyklin antybiotyków (syntetyczna pochodna tetracykliny). Jest wskazany w leczeniu powikłanych zakażeń skóry i struktury skóry( cSSSI), powikłanych zakażeń wewnątrzbrzusznych i zapalenia płuc wywołanego przez MRSA.Tygecykliny nie należy rutynowo stosować w przypadku bakteriemii ze względu na obawy dotyczące osiągnięcia niedostatecznego stężenia w surowicy., Ponieważ tygecyklina jest antybiotykiem o szerokim spektrum działania, należy ograniczyć jej stosowanie do ciężkich i zagrażających życiu zakażeń u pacjentów hospitalizowanych.
Telawancyna (Vibativ) jest najnowszym lekiem zatwierdzonym przez FDA do leczenia zakażeń MRSA.Jest to lipoglikopeptyd podobny do wankomycyny, chociaż jego mechanizm działania jest różny. Telawancyna zaburza przepuszczalność błony komórkowej poprzez depolaryzację błony plazmatycznej, zwiększając przepuszczalność i wyciek komórkowego trójfosforanu adeno-sinusoidalnego i potasu (K+)., Czas tych zmian koreluje z szybką, zależną od stężenia utratą żywotności bakterii, co sugeruje, że wczesne działanie bakteriobójcze telawancyny wynika z rozproszenia potencjału błony komórkowej i wzrostu przepuszczalności błon.
badania kliniczne wykazały, że telawancyna nie jest gorsza od wankomycyny w leczeniu cSSSI.Jedną z zalet telawancyny nad wankomycyną jest dawkowanie raz na dobę i brak konieczności monitorowania stężenia leku. Jednak, podobnie jak wankomycyna, dawka musi być dostosowana u pacjentów z niewydolnością nerek.,U wszystkich pacjentów podczas przerwania leczenia i po jego zakończeniu należy monitorować czynność nerek. Telawancyna jest związana z wydłużeniem odstępu QTc i należy ją stosować ostrożnie u pacjentów przyjmujących leki, które również mogą wydłużać odstęp QTc. W badaniach klinicznych porównujących telawancynę z wankomycyną działania niepożądane zgłaszane u ponad 10% pacjentów leczonych telawancyną obejmowały zaburzenia smaku, nudności, wymioty i spieniony mocz.Ciężkie działania niepożądane zgłaszano u 7% pacjentów leczonych telawancyną i najczęściej obejmowały zdarzenia dotyczące nerek, dróg oddechowych lub serca., Istnieje ostrzeżenie dotyczące ryzyka płodu związanego ze stosowaniem telawancyny; dlatego kobiety w wieku rozrodczym muszą wykonać test ciążowy w surowicy przed rozpoczęciem stosowania telawancyny.Ceftobiprol (Zeftera) jest pierwszą cefalosporyną o działaniu bakteriobójczym przeciwko MRSA. Jego działanie przeciwbakteryjne obejmuje hamowanie białek wiążących penicylinę biorących udział w syntezie ściany komórkowej. W badaniach klinicznych lek był równie skuteczny jak skojarzenie wankomycyny i ceftazydymu w leczeniu cSSSI.,Jest na ogół dobrze tolerowany, z głównymi działaniami niepożądanymi leku, w tym nudnościami i zaburzeniami smaku. Ceftobiprol nie jest obecnie dopuszczony do stosowania w USA, i chociaż wcześniej został dopuszczony do stosowania w Kanadzie, producent zaprzestał sprzedaży leku z dniem 16 kwietnia 2010 r. 35 było to zgodne z zaleceniami organów regulacyjnych w Europie (Europejski Komitet ds. Produktów Leczniczych Stosowanych u ludzi) i USA (FDA), aby nie zatwierdzić leku., Chociaż wyniki III fazy sugerowały korzyści ze stosowania ceftobiprolu, istniały obawy co do integralności tych wyników z powodu manipulacji danymi klinicznymi z niektórych miejsc badań. Dzięki temu niedawnemu rozwojowi przyszłość stosowania ceftobiprolu na rynku amerykańskim pozostaje wątpliwa.
wnioski
wraz z pojawieniem się CA-MRSA oraz heteroopornego MRSA ważne jest, aby farmaceuci zapoznali się ze wszystkimi dostępnymi środkami do leczenia zakażeń MRSA. Istotne jest również, aby wybrać odpowiedni środek przeciwbakteryjny dla leczonego zakażenia., Ponadto leki o szerszym spektrum działania (np. tygecyklina) powinny być zarezerwowane dla bardzo ciężkich zakażeń oraz w przypadku zakażeń wielogatunkowych. Niezwykle ważne jest również, aby zarezerwować nowsze leki na cięższe infekcje w celu zminimalizowania rozwoju oporności.
1. Boucher HW, Corey gr. Epidemiologia opornego na metycylinę Staphylococcus aureus. / Align = „Left” /
2 . Styers D, Sheehan DJ, Hogan P, et al., Laboratory-based surveillance of current antimicrobial resistance patterns and trends among Staphylococcus aureus: 2005 status in the United States. Ann Clinton 2006;5:2.
3. Chien JW, Kucia ML, Salata RA. Stosowanie linezolidu, oksazolidynonu, w leczeniu opornych na wiele leków zakażeń bakteryjnych gram-dodatnich. / Align = „Left” / 2000;30:146-151.
4. Soriano A, Martinez JA, Mensa J, et al. Patogenne znaczenie oporności na metycylinę u pacjentów z bakteriemią Staphylococcus aureus. / Align = „Left” / 2000;30:368-673.
5. Graffunder EM, Venezia RA., Czynniki ryzyka związane z zakażeniem szpitalnym opornym na metycylinę Staphylococcus aureus (MRSA), w tym wcześniejsze stosowanie środków przeciwdrobnoustrojowych. J Antymikrob Chemother. 2002;49:999-1005.
6. Klevens RM, Edwards JR, TENOVER FC, et al. Zmiany w epidemiologii opornego na metycylinę Staphylococcus aureus na oddziałach intensywnej terapii w szpitalach USA, 1992-2003. / Align = „Left” /
7. Levine DP, Cushing RD, Jui J, Brown WJ. Staphylococcus aureus endocarditis nabyte przez społeczność w Detroit Medical Center. Anna Intern Med. 1982;97:330-338.
8., Lodise TP Jr, McKinnon PS, Rybak M. Prediction model to identify patients with Staphylococcus aureus bacteremia at risk for metycilin resistance. Infect Control Hosp Epidemiol. 2003;24:655-661.
9. King MD, Humphrey BJ, Wang YF, et al. Pojawienie się klonu Staphylococcus aureus USA 300 opornego na metycylinę jako głównej przyczyny zakażeń skóry i tkanek miękkich. Anna Intern Med. 2006;144:309-317.
10. Centrum Kontroli i profilaktyki chorób., Zakażenia Staphylococcus aureus oporne na metycylinę wśród uczestników sportów wyczynowych-Kolorado, Indiana, Pensylwania i Los Angeles County, 2000-2003. MMWR. 2003;52:793-795.
11. Lowy FD. Zakażenia Staphylococcus aureus. N Engl J Med. 1998;339:520-532.
12. Chambers HF. Zmiana epidemiologii Staphylococcus aureus? Emergency Infect Dis.
13. Informacje dotyczące MRSA dla klinicystów. CDC. www.cdc.gov/ncidod/dhqp/ar_ 2008; 46 (suppl 5): S344-S349. 2006;42:389-391. 2001;7:178-182.mrsa_ca_clinicihtml. Dodano: 4 Lipca 2010 / 16: 00
14. Rybak MJ, kl. LaPlante, Staphylococcus aureus-oporny na metycylinę Staphylococcus aureus; przegląd. Farmakoterapia. 2005;25:74-85.
15. Gorwitz RJ, Jernigan DB, Powers JH, et al. Strategie klinicznego zarządzania MRSA w społeczności: podsumowanie spotkania ekspertów zwołanego przez centra kontroli i Zapobiegania Chorobom. Marzec 2006. www.cdc.gov/ncidod/dhqp/pdf/ar/CAMRSA_ExpMtgStrategies.pdf. [Dostęp 4 lipca 2010].
16. Sabol KE, Echevarria KL, Lewis JS II. Community-associated methicilin-resistant Staphylococcus aureus: new bug, old drugs. / Align = „Left” / 2006;40:1125-1133.
17., Kleocin (klindamycyna). Nowy Jork, NY: Pfizer Inc; listopad 2005.
18. Strom BL, Schinnar R, Apter AJ, et al. Brak wrażliwości krzyżowej między antybiotykami sulfonamidowymi a nieantybiotykami sulfonamidowymi. N Engl J Med. 2003;349:1628-1635.
19. Nicolau DP, Freeman CD, Nightingale CH, et al. Minocyklina w porównaniu z wankomycyną w leczeniu doświadczalnego zapalenia wsierdzia wywołanego przez oporny na oksacylinę Staphylococcus aureus. Środki Antymikrobowe Chemother. 1994;38:1515-1518.
20. Sakoulas G, Moellering RC Jr., Zwiększenie oporności na antybiotyki wśród szczepów Staphylococcus aureus opornych na metycylinę. / Align = „Left” / 2008; 46 (suppl 5): S360-S367.
21 . Rybak MJ, Akins RL. Pojawienie się opornego na metycylinę Staphylococcus aureus o pośredniej oporności na glikopeptydy: znaczenie kliniczne i możliwości leczenia. Narkotyki. 201;61:1-7.
22 . Tenover FC, Moellering RC Jr. the rationale for reviewing the Clinical and Laboratory Standards Institute for Staphylococcus aureus. / Align = „Left” / 2007;44:1208-1215.
23 ., Jeffres MN, Micek ST, Isakow W, et al. Zwiększenie częstości występowania nefrotoksyczności przy wyższych minimalnych stężeniach wankomycyny w surowicy. Program i streszczenia 46th Interscience Conference on Antimicrobial Agents and Chemotherapy (ICAAC); 27-30 września 2006; San Francisco, CA. Abstract K789
24 . Zyvox (linezolid) ulotka dla pacjenta. Nowy Jork, NY: Pfizer Inc; grudzień 2009.
25 . Kuter DJ, Tillotson GS. Hematologiczne działanie środków przeciwdrobnoustrojowych, koncentrując się na oksazolidynonie, linezolidzie. Farmakoterapia. 201;21:1010-1013.
26 . Cubicin (daptomycyna) ulotka informacyjna., Lexington, MA: Cubist Pharmaceuticals; January 2010.
27. Murthy MH, Olson ME, Wickert RW, et al. Daptomycin non-susceptible methicillin-resistant Staphylococcus aureus USA 300 isolate. J Med Microbiol. 2008;57:1036-1038.
28. Mangili A, Bica I, Snydman R, Hamer DH. Daptomycin-resistant methicillin-resistant Staphylococcus aureus bacteremia. Clin Infect Dis. 2005;40:1058-1060.
29. Synercid (quinupristin-dalfopristin) package insert. Greenville, NC: Monarch Pharmaceuticals; June 2008.
30. Tygacil (tigecycline) package insert. Philadelphia, PA: Wyeth Pharmaceuticals; September 2009.,
31. Vibativ (telawancyna) ulotka dla pacjenta. Astellas Pharma US, Inc; wrzesień 2009.
32. Stryjewski ME, Chu VH, O ' Riordan WD, et al. Telawancyna a standardowa terapia w leczeniu powikłanych infekcji skóry i struktury skóry wywołanych przez bakterie gram-dodatnie: badanie FAST 2. Środki Antymikrobowe Chemother. 2006;50:862-867.
33. Corey gr. Badania telawancyny w cSSSI. Referat wygłoszony na: Third International Symposium on oporne Gram-dodatnie infekcje; październik 10, 2006; Niagara-on-the-Lake, Kanada.
34. Vidaillac C, Rybak MJ., Ceftobiprole: first cephalosporin with activity against methicillin-resistant Staphylococcus aureus. Pharmacotherapy. 2009;29:511-525.
35. Discontinuation of the sale of ceftobiprole in Canada. Basilea Pharmaceutica. April 9, 2010. http://hugin.info/134390/R/1401931/356785.pdf. Accessed July 12, 2010.
36. Vibramycin (doxycycline) package insert. New York, NY: Pfizer Inc; April 2007.
37. Minocin (minocycline) package insert. Philadelphia, PA: Triax Pharmaceuticals; March 2006.
38. Bactrim (trimethoprim-sulfamethoxazole) package insert. Philadelphia, PA: AR Scientific; November 2006.
39., Vancocin (vancomycin) package insert. Exton, PA: ViroPharma Inc; October 2005.