reakcje strącania i zasady rozpuszczalności
reakcja strącania to reakcja, w której rozpuszczone substancje reagują tworząc jeden (lub więcej) stałych produktów. Wiele reakcji tego typu wiąże się z wymianą jonów między związkami jonowymi w roztworze wodnym i są czasami określane jako podwójne przemieszczenie, Podwójna wymiana lub reakcje metatezy., Reakcje te są powszechne w przyrodzie i są odpowiedzialne za powstawanie raf koralowych w wodach oceanicznych i kamieni nerkowych u zwierząt. Są one szeroko stosowane w przemyśle do produkcji wielu chemikaliów towarowych i specjalistycznych. Reakcje strącania odgrywają również kluczową rolę w wielu technikach analizy chemicznej, w tym badaniach punktowych stosowanych do identyfikacji jonów metali i metod grawimetrycznych do określania składu materii (patrz ostatni moduł tego rozdziału).,
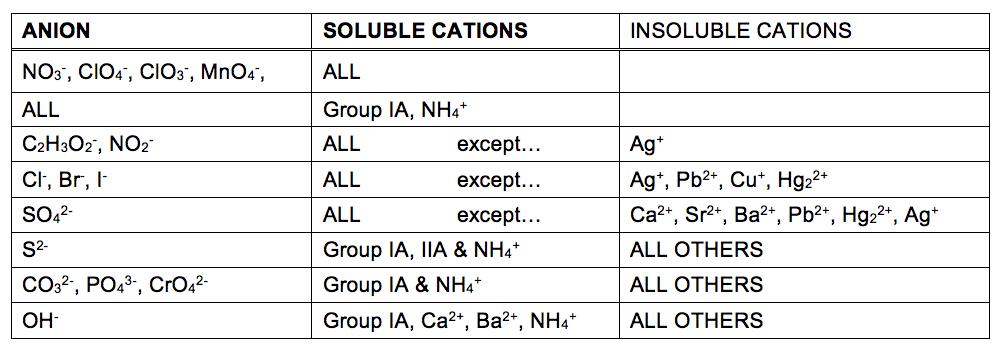
zakres, w jakim substancja może zostać rozpuszczona w wodzie lub dowolnym rozpuszczalniku, jest ilościowo wyrażony jako jej rozpuszczalność, zdefiniowana jako maksymalne stężenie substancji, które można osiągnąć w określonych warunkach. Mówi się, że substancje o stosunkowo dużej rozpuszczalności są rozpuszczalne. Substancja wytrąci się, gdy warunki roztworu są takie, że jego stężenie przekracza jego rozpuszczalność. Substancje o stosunkowo niskiej rozpuszczalności są uważane za nierozpuszczalne i są to substancje, które łatwo wytrącają się z roztworu., Więcej informacji na temat tych ważnych pojęć znajduje się w rozdziale tekstowym dotyczącym rozwiązań. Dla celów przewidywania tożsamości ciał stałych powstałych w wyniku reakcji wytrącania, można po prostu odnieść się do wzorców rozpuszczalności, które zaobserwowano dla wielu związków jonowych(Tabela 1).
żywy przykład wytrącania obserwuje się, gdy roztwory jodku potasu i azotanu ołowiu są mieszane, w wyniku czego powstaje stały jodek ołowiu:
ta obserwacja jest zgodna z wytycznymi dotyczącymi rozpuszczalności: jedynym nierozpuszczalnym Związkiem wśród wszystkich zaangażowanych jest jodek ołowiu, jeden z wyjątków od ogólnej rozpuszczalności soli jodkowych.,
równanie jonowe netto reprezentujące tę reakcję to:
jodek ołowiu jest jasnożółtym ciałem stałym, które wcześniej było używane jako barwnik artysty znany jako JOD yellow (Rysunek 1). Właściwości czystych kryształów PbI2 sprawiają, że są one przydatne do wytwarzania detektorów rentgenowskich i gamma.

tabela rozpuszczalności w tabeli 1 może być używana do przewidywania, czy reakcja wytrącania wystąpi, gdy roztwory rozpuszczalnych związków jonowych są mieszane razem. Wystarczy zidentyfikować wszystkie jony obecne w roztworze, a następnie rozważyć, czy możliwe parowanie kationów/anionów może spowodować powstanie nierozpuszczalnego związku.
na przykład, mieszanie roztworów azotanu srebra i fluorku sodu daje roztwór zawierający jony Ag+, NO3−, na+ I F−., Oprócz dwóch związków jonowych pierwotnie obecnych w roztworach, AgNO3 i NAf, z tego zbioru jonów mogą pochodzić dwa dodatkowe związki jonowe: NaNO3 i AgF.
tabela rozpuszczalności wskazuje, że wszystkie sole azotanowe są rozpuszczalne, ale AgF jest jednym z wyjątków od ogólnej rozpuszczalności soli fluorkowych. W związku z tym przewiduje się wystąpienie reakcji strącania, opisanej następującymi równaniami: