12.7 bufory
cele uczenia się
- Zdefiniuj bufor.
- poprawnie identyfikuje dwa komponenty bufora.
jak wskazano w punkcie 12.4 „silne i słabe kwasy, zasady i ich sole”, słabe kwasy są stosunkowo powszechne, nawet w żywności, którą spożywamy. Ale czasami napotykamy silny kwas lub zasadę, taką jak kwas żołądkowy, który ma silnie kwaśne pH 1,7. Z definicji silne kwasy i zasady mogą wytwarzać stosunkowo dużą ilość jonów H + lub OH-i w związku z tym mają zaznaczoną aktywność chemiczną., Ponadto bardzo małe ilości silnych kwasów i zasad mogą bardzo szybko zmienić pH roztworu. Gdyby do krwioobiegu Dodano 1 mL kwasu żołądkowego i nie było mechanizmu korygującego, pH krwi zmniejszyłoby się z około 7,4 do około 4,7—pH, które nie sprzyja dalszemu życiu. Na szczęście organizm ma mechanizm minimalizacji tak dramatycznych zmian pH.
mechanizm polega na zastosowaniu roztworu buforowego odpornego na dramatyczne zmiany pH., roztworu odpornego na dramatyczne zmiany pH., Bufory robią to, ponieważ składają się z pewnych par substancji rozpuszczonych: albo słaby kwas plus sól pochodząca z tego słabego kwasu lub słaba zasada plus sól tej słabej zasady. Na przykład bufor może składać się z rozpuszczonego HC2H3O2 (słaby kwas) i NaC2H3O2 (sól pochodząca z tego słabego kwasu). Innym przykładem bufora jest roztwór zawierający NH3 (słabą zasadę) i NH4Cl (sól pochodząca z tej słabej zasady).
użyjmy bufora HC2H3O2 / NaC2H3O2, aby zademonstrować działanie buforów., Jeśli mocna zasada – źródło jonów OH—(aq)− zostanie dodana do roztworu buforowego, jony OH-będą reagować z HC2H3O2 w reakcji kwasowo-zasadowej:
HC2H3O2 ( AQ) + OH−(AQ) → H2O(ℓ) + C2H3O2−(AQ)
zamiast radykalnie zmieniać pH, czyniąc roztwór podstawowym, dodane jony OH− reagują, tworząc H2O, więc pH nie zmienia się zbytnio.
Jeśli do roztworu buforowego zostanie dodany silny kwas—źródło jonów H+, jony H+ będą reagować z anionem z soli. Ponieważ HC2H3O2 jest słabym kwasem, nie jest zbytnio zjonizowany., Oznacza to, że jeśli wiele jonów H+ i jonów C2H3O2 jest obecnych w tym samym roztworze, będą one razem tworzyć HC2H3O2:
h+(aq) + C2H3O2 – (AQ) → HC2H3O2 (AQ)
zamiast radykalnie zmieniać pH i powodować kwasowość roztworu, dodane jony H+ reagują, tworząc cząsteczki słabego kwasu. Rysunek 12.2 „działania buforów” ilustruje oba działania bufora.
rysunek 12.2 działanie buforów
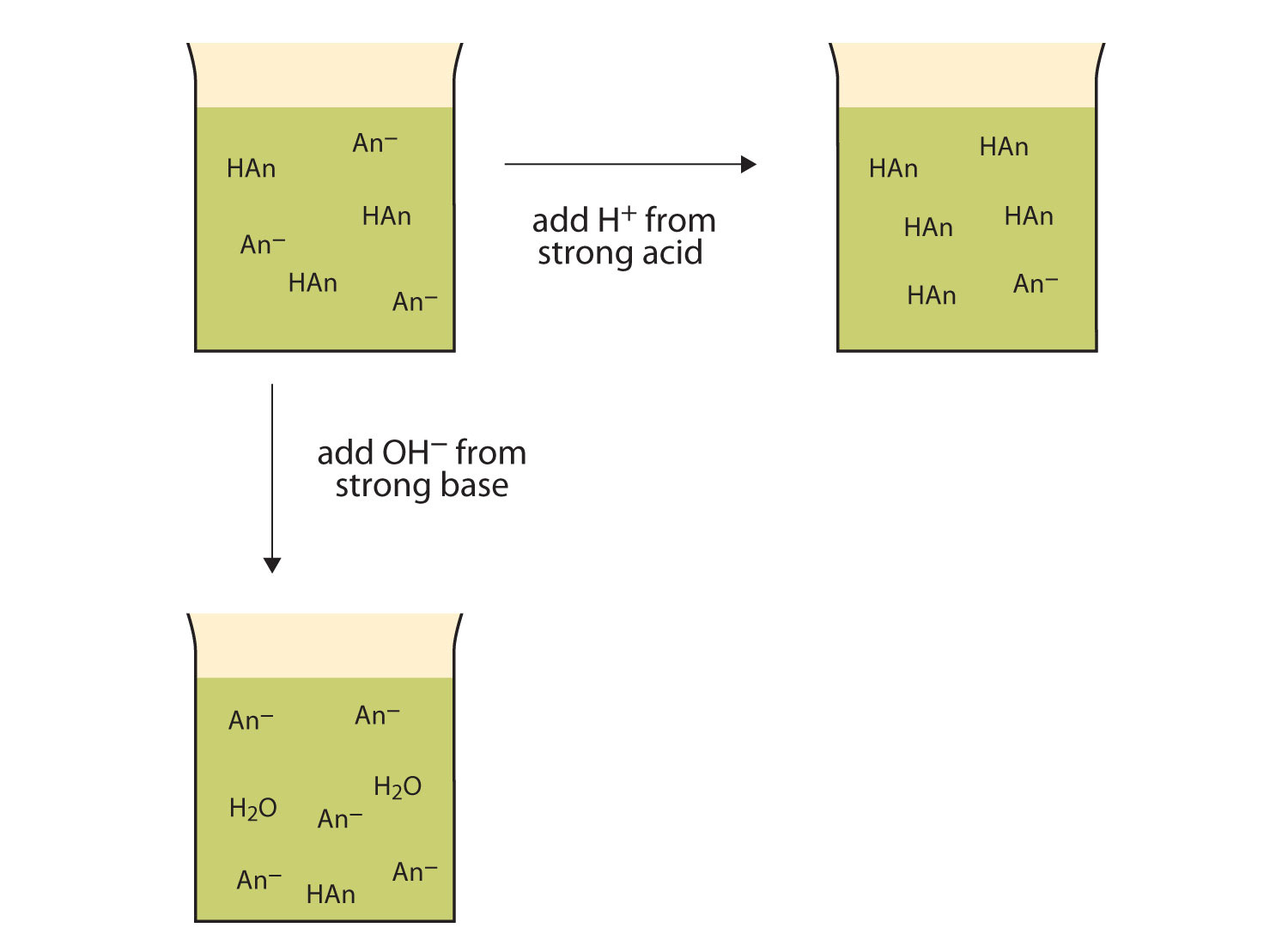
bufory mogą reagować zarówno z silnymi kwasami (Góra), jak i silnymi zasadami (strona), aby zminimalizować duże zmiany pH.,
bufory wykonane ze słabych zasad i sole słabych zasad działają podobnie. Na przykład w buforze zawierającym NH3 i NH4Cl cząsteczki NH3 mogą reagować z nadmiarem jonów H+ wprowadzanych przez silne kwasy:
NH3(aq) + H+(AQ) → NH4+(AQ)
podczas gdy NH4+(AQ) może reagować z dowolnymi jonami OH− wprowadzanymi przez silne zasady:
NH4+(AQ) + OH−(AQ) → NH3(AQ) + H2O(ℓ)
przykład 15
Jakie kombinacje związków mogą tworzyć roztwór buforowy?,
- Hcho2 i nacho2
- HCl i NaCl
- CH3NH2 i CH3NH3Cl
- NH3 i NaOH
roztwór
- Hcho2 to kwas mrówkowy, słaby kwas, podczas gdy nacho2 to sól wytworzona z anionu słabego kwasu (jonu mrówczanowego ). Połączenie tych dwóch roztworów tworzy roztwór buforowy.
- HCl jest silnym kwasem, a nie słabym kwasem, więc połączenie tych dwóch roztworów nie tworzy roztworu buforowego.
- CH3NH2 jest metyloaminą, która jest podobna do NH3 z jednym z jej atomów H podstawionym grupą CH3. Ponieważ nie jest wymieniony w Tabeli 12.,2 „Silne kwasy i zasady”, możemy założyć, że jest to słaba zasada. Związek CH3NH3Cl jest solą wykonaną z tej słabej zasady, więc połączenie tych dwóch substancji rozpuszczalnych stworzyłoby roztwór buforowy.
- NH3 jest słabą bazą, ale NaOH jest silną bazą. Połączenie tych dwóch roztworów nie tworzy roztworu buforowego.
Sprawdź się
Jakie kombinacje związków mogą stworzyć roztwór buforowy?,
- NaHCO3 i NaCl
- H3PO4 i NaH2PO4
- NH3 i (NH4)3po4
- NaOH i NaCl
odpowiedzi
- nie
- tak
- nie
bufory działają dobrze tylko w przypadku ograniczonych ilości dodanego mocnego kwasu lub zasady. Po całkowitej reakcji roztworu roztwór nie jest już buforem i mogą wystąpić gwałtowne zmiany pH. Mówimy, że bufor ma pewną pojemnośćilość silnego kwasu lub zasady bufor może przeciwdziałać.., Bufory, które mają więcej rozpuszczonej rozpuszczonej w nich na początek mają większe pojemności, jak można się spodziewać.
ludzka krew ma system buforujący, aby zminimalizować ekstremalne zmiany pH. jeden bufor we krwi opiera się na obecności HCO3− i H2CO3 . Przy obecnym buforze, nawet jeśli kwas żołądkowy trafiłby bezpośrednio do krwiobiegu, zmiana pH krwi byłaby minimalna. Wewnątrz wielu komórek organizmu znajduje się system buforujący oparty na jonach fosforanowych.,
aplikacja do jedzenia i picia: kwas, który łagodzi ból
chociaż leki nie są dokładnie „jedzeniem i piciem”, spożywamy je, więc spójrzmy na kwas, który jest prawdopodobnie najczęstszym lekiem: kwas acetylosalicylowy, znany również jako aspiryna. Aspiryna jest dobrze znana jako lek przeciwbólowy i przeciwgorączkowy (reduktor gorączki).
struktura aspiryny pokazana jest na załączonym rysunku. Część kwasowa jest okrążona; jest to atom H w tej części, który można oddać, ponieważ aspiryna działa jako kwas Brønsted-Lowry. Ponieważ nie podano go w Tabeli 12.,2 „Silne kwasy i zasady”, kwas acetylosalicylowy jest słabym kwasem. Jednak nadal jest to kwas, a biorąc pod uwagę, że niektórzy ludzie spożywają stosunkowo duże ilości aspiryny codziennie, jego kwaśny charakter może powodować problemy w błonie śluzowej żołądka, pomimo obrony żołądka przed własnym kwasem żołądkowym.
rysunek 12.3 Struktura molekularna aspiryny
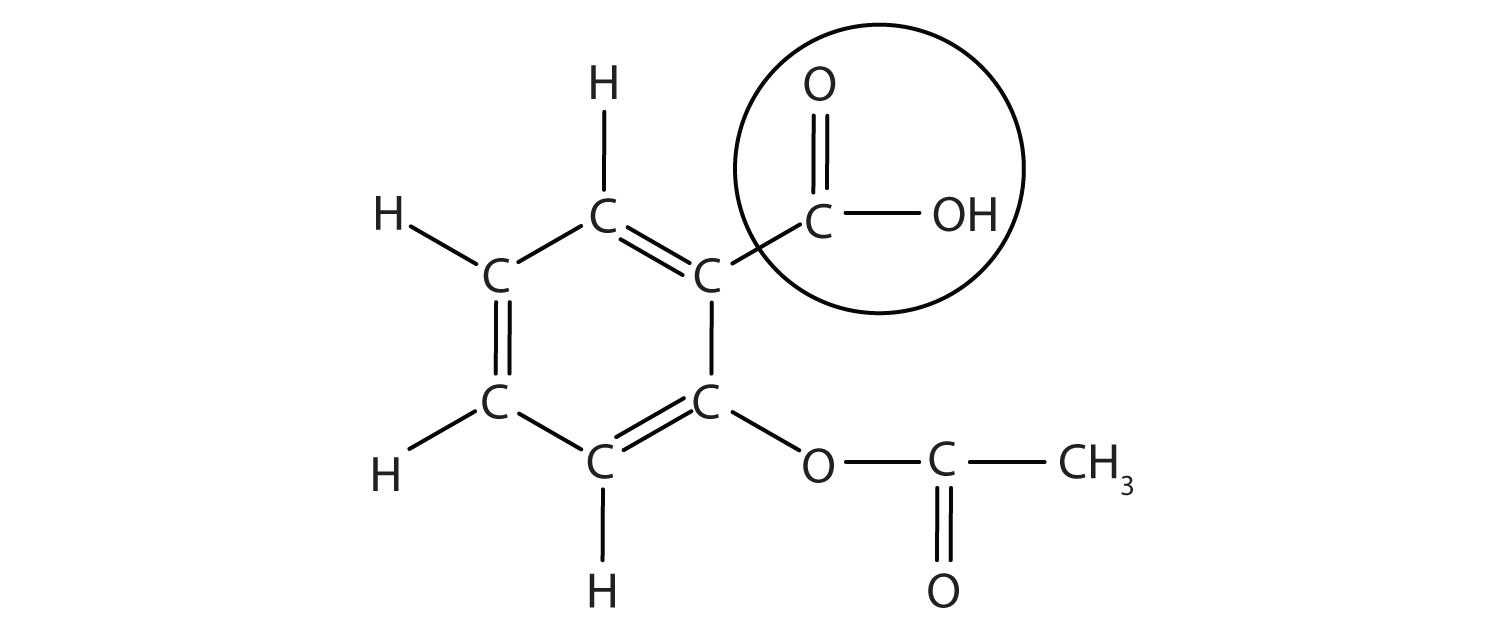
okrężone atomy są kwaśną częścią cząsteczki.
ponieważ kwasowe właściwości aspiryny mogą być problematyczne, wiele marek aspiryny oferuje „buforowaną aspirynę” formę leku., W takich przypadkach aspiryna zawiera również środek buforujący-Zwykle MgO – który reguluje kwasowość aspiryny, aby zminimalizować jej kwaśne skutki uboczne.
chociaż aspiryna jest przydatna i powszechna, została oficjalnie wprowadzona do obrotu jako lek od 1899 roku. Amerykańska Agencja Żywności i Leków (FDA), agencja rządowa odpowiedzialna za nadzorowanie i zatwierdzanie leków w Stanach Zjednoczonych, powstała dopiero w 1906 roku., Niektórzy twierdzili, że jeśli FDA została utworzona przed wprowadzeniem aspiryny, aspiryna może nigdy nie uzyskać zgody ze względu na jej potencjalne skutki uboczne—krwawienie z przewodu pokarmowego, dzwonienie w uszach, zespół Reye ' a (problem z wątrobą) i niektóre reakcje alergiczne. Jednak ostatnio aspiryna została reklamowana ze względu na jej skutki w zmniejszaniu zawałów serca i udarów mózgu, więc prawdopodobnie aspiryna zostanie tutaj.
bufor jest rozwiązaniem odpornym na nagłe zmiany pH.
-
Zdefiniuj bufor., Jakie Dwa powiązane składniki chemiczne są wymagane do utworzenia bufora?
-
Czy można wykonać bufor łącząc mocny kwas z mocną zasadą? Dlaczego czy nie?
-
Jakie kombinacje związków mogą tworzyć bufor? Przyjąć roztwory wodne.
- HCl i NaCl
- HNO2 i NaNO2
- NH4NO3 i HNO3
- NH4NO3 i NH3
-
Jakie kombinacje związków mogą utworzyć bufor? Przyjąć roztwory wodne.,
- H3PO4 i Na3PO4
- NaHCO3 i Na2CO3
- NaNO3 i Ca(NO3)2
- HN3 i NH3
-
dla każdej kombinacji w ćwiczeniu 3, która jest buforem, napisz równania chemiczne dla reakcji składników bufora, gdy dodaje się silny kwas i mocną zasadę.
-
dla każdej kombinacji w Ćwiczeniu 4, która jest buforem, napisz równania chemiczne dla reakcji składników bufora, gdy dodaje się silny kwas i mocną zasadę.,
-
kompletny system buforów fosforanowych oparty jest na czterech substancjach: H3PO4, H2PO4 -− HPO42-i PO43 -. Jakie roztwory buforowe można wytwarzać z tych substancji?
-
wyjaśnij, dlaczego NaBr nie może być składnikiem bufora kwaśnego lub zasadowego.
-
powstają dwa roztwory zawierające te same stężenia rozpuszczonych substancji. Jeden roztwór składa się z H3PO4 i Na3PO4, podczas gdy drugi składa się z HCN i NaCN. Które rozwiązanie powinno mieć większą pojemność jako bufor?,
-
powstają dwa roztwory zawierające te same stężenia rozpuszczonych substancji. Jeden roztwór składa się z NH3 i NH4NO3, podczas gdy drugi składa się z H2SO4 i Na2SO4. Które rozwiązanie powinno mieć większą pojemność jako bufor?
odpowiedzi
-
bufor jest połączeniem słabego kwasu lub zasady i soli tego słabego kwasu lub zasady.,
-
-
- nie
- nie
- tak
-
-
3b: silny kwas: NO2− + H+ → HNO2; mocna baza: HNO2 + Oh− → no2− + H2O; 3D: mocna baza: NH4+ + Oh− → NH3 + H2O; mocna baza: NH3 + H+ → NH4+
-
bufory mogą być wykonane z trzech kombinacji: (1) H3PO4 i H2PO4−, (2) H2PO4− i HPO42− oraz (3) HPO42− i PO43−. (Technicznie, bufor może być wykonany z dowolnych dwóch komponentów.,)
bufor fosforanowy powinien mieć większą pojemność.