US Pharm. 2010; 35 (8): HS2-HS4.
methicilline-resistente Staphylococcus aureus (MRSA) is een van de belangrijkste oorzaken van zowel in de gezondheidszorg als in de gemeenschap verworven infecties.1,2 infecties als gevolg van MRSA worden geassocieerd met een hoog risico op morbiditeit en mortaliteit en leiden tot hoge kosten voor de gezondheidszorg.3-5 de incidentie van MRSA-infecties in de Verenigde Staten is de afgelopen jaren gestaag gestegen van 22% in 1995 tot 60% in 2003.,6 gezondheidszorg-geassocieerde MRSA (HA-MRSA) is gerelateerd aan ziekenhuizen en langdurige zorg faciliteiten en is gemeenschappelijk bij patiënten met langdurige ziekenhuisopname, verleden antimicrobiële gebruik, decubitus ulcera, dialyse, inwonende katheters, enterale voedingen, of geschiedenis van IV drugsmisbruik.7,8 in de afgelopen jaren is er echter een toename geweest in een nieuwe stam van MRSA genaamd community-associated MRSA (CA-MRSA)., Dit lijkt te worden verworven in de poliklinische setting, en overdracht is door middel van nauw fysiek contact, zoals in dagverblijven, Indiase reserveringen, en correctionele faciliteiten en onder atleten, militair personeel, en mannen die seks hebben met mannen.7,9,10
onderscheidende MRSA-stammen
verschillende rapporten hebben verschillen aangetoond tussen Ha-MRSA-en CA-MRSA-stammen, waaronder de aanwezigheid van verschillende genotypes tussen de twee stammen. CA-MRSA is gevoelig voor verschillende niet-bèta-lactam antibiotica, terwijl ha-MRSA stammen dat niet zijn., CA-MRSA stammen coderen eerder bepaalde virulente factoren die geassocieerd zijn met ernstige pneumonie (vooral bij kinderen) en infecties van de huid en weke delen bij volwassenen.8,11,12 de CDC heeft de criteria vastgesteld voor het onderscheid tussen CA-MRSA en HA-MRSA. Deze richtlijnen omvatten het isoleren van een positieve MRSA cultuur binnen 48 uur na de opname van een patiënt in het ziekenhuis. Om te worden beschouwd als CA-MRSA, mag de patiënt geen van de volgende: recente ziekenhuisopname; opname in een verpleeghuis, hospice, of geschoolde verpleeginstelling; dialyse; of recente operatie., De patiënt mag ook geen inwonende katheters of andere medische hulpmiddelen hebben.13
behandeling van CA-MRSA
de CDC beveelt aan dat het beheer en de preventie van uitbraken van CA-MRSA ook betrekking moeten hebben op infecties die pus veroorzaken, regelmatig handen wassen, geen persoonlijke spullen delen, Vuil beddengoed en kleding wassen met warm water, en doeken drogen in een warme droger in vergelijking met drogen aan de lucht.Voor huidabcessen omvat de behandeling incisie en drainage van de abcessen met of zonder systemische antibiotica, afhankelijk van de ernst van de infectie.,De behandeling van CA-MRSA omvat gewoonlijk het gebruik van middelen zoals clindamycine, tetracyclinen en trimethoprim-sulfamethoxazol (tmp-SMX). Het antibioticum rifampine mag nooit als monotherapie voor de behandeling van MRSA worden gebruikt. Resistentie ontwikkelt zich snel bij rifampine monotherapie; wanneer het echter wordt gebruikt in combinatie met een ander anti-MRSA-middel, kan het organismen effectiever uitroeien van dragerplaatsen.15 de bovengenoemde antibiotica zijn meestal levensvatbare behandelingsopties bij patiënten behandeld op een poliklinische basis., Bij ernstige infecties waarvoor ziekenhuisopname noodzakelijk is, zijn IV antibiotica waaronder vancomycine, linezolide, quinupristine-dalfopristine, daptomycine, tigecycline en telavancine geschikte therapieën die kunnen worden gebruikt (tabel 1).
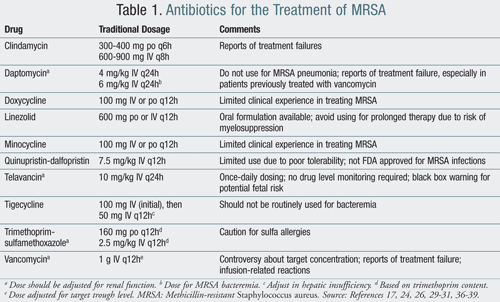
hoewel clindamycine (Cleocin) kan worden gebruikt voor CA-MRSA, is gemeld dat resistentie tot 19% bedraagt bij patiënten die ermee worden behandeld. Daarom moeten patiënten die met clindamycine worden behandeld, nauwkeuriger worden gecontroleerd op de ontwikkeling van zelfgeïnduceerde resistentie.,16 clindamycine is ook geassocieerd met de ontwikkeling van Clostridium difficile infecties, het beperken van het gebruik ervan over een langere periode.
TMP-SMX (Bactrim) kan worden beschouwd als een alternatief voor vancomycine-therapie in sommige gevallen van MRSA-infecties. Net als bij clindamycine zijn er echter meldingen geweest van falende behandeling. Deze therapie heeft ook beperkt gebruik toe te schrijven aan de hoge weerslag van sulfonamideallergieën, die hebben gemeld om in tot 10% van de bevolking voor te komen.,18
Minocycline (Minocin) en doxycycline (Vibramycine) zijn tetracyclineantibiotica die zijn gebruikt voor de behandeling van MRSA. Deze middelen hebben slechts beperkte gegevens over het gebruik bij MRSA, maar klinisch succes is gemeld.19
behandeling van HA-MRSA
parenterale antibiotica worden beschouwd als de gouden standaard voor de behandeling van HA-MRSA. Gedurende verscheidene decennia, is het glycopeptide antibioticum vancomycine wijd gebruikt.
vancomycine (vancocin) remt de celwandsynthese; in vitro heeft het echter een tragere bactericide activiteit., Met zijn overgebruik, zijn er meldingen van verminderde gevoeligheid en de opkomst van vancomycine heteroresistance in s aureus geweest.20,21 de toename in een subpopulatie van s aureus met minimale remmende concentratie (Mic) van >2 mcg/mL tot vancomycine (aangeduid als mic kruip) is geassocieerd met zowel microbiologisch als klinisch falen. Het National Committee for Clinical Laboratory Standards (NCCLS) heeft nieuwe breekpunten voorgesteld voor vancomycine—waarbij de MIC voor “gevoelig” wordt gewijzigd van ≤4 mcg/mL naar ≤2 mcg/mL.,De motivering voor dit voorstel is gedeeltelijk gebaseerd op anekdotische klinische waarnemingen van falende behandeling tijdens behandeling met standaarddoses vancomycine bij patiënten met een MIC van 4 mcg/mL. Bovendien kunnen hogere dalspiegels (d.w.z. dalspiegels van 15-20 mcg/mL) nodig zijn voor ernstige infecties zoals pneumonie en osteomyelitis als gevolg van een slechte weefselpenetratie door vancomycine. Er zijn enkele anekdotische meldingen geweest van mogelijke nefrotoxiciteit geassocieerd met deze hoge dalspiegels.,
Jeffres et al presenteerde een samenvatting op de 2006 Interscience Conference on Antimicrobial Agents and Chemotherapy (ICAAC), waarin het risico op nefrotoxiciteit met hogere vancomycine dalspiegels werd beoordeeld.In hun studie rapporteerden zij een 30% risico op nefrotoxiciteit (gedefinieerd als een toename van 0,5 mg/dL of 50% toename van serumcreatinine ten opzichte van de uitgangswaarde) bij patiënten met vancomycine dalspiegels van 315 mcg/mL vergeleken met 13% bij patiënten met dalspiegels <15 mcg/mL.Sommige patiëntenpopulaties lopen een hoger risico op de ontwikkeling van door vancomycine geïnduceerde nefrotoxiciteit., Deze omvatten bekende risicofactoren zoals hogere leeftijd, ernstig ziek zijn, lagere nierfunctie hebben, en gelijktijdig gebruik van andere nefrotoxische middelen zoals aminoglycosiden. Al deze factoren hebben geleid tot een toename van de behoefte en het gebruik van de nieuwere middelen.
Linezolid (Zyvox) is het eerste oxazolidinon dat is goedgekeurd voor de behandeling van infecties van de huid en weke delen, bacter-emia, en gemeenschap en nosocomiale pneumonie veroorzaakt door MRSA.Het remt de initiatie van eiwitsynthese bij het jaren ‘ 50 ribosoom; echter, in tegenstelling tot de meeste andere geneesmiddelen, is het een bacteriostatische agent., Voordelen aan het gebruik ervan zijn onder meer de beschikbaarheid van een orale formulering met uitstekende biologische eigenschappen, zonder dosisaanpassing gerechtvaardigd bij patiënten met nierinsufficiëntie, met inbegrip van degenen die niervervangende therapieën. Een beperkende factor voor het gebruik, met name voor langere duur van de behandeling, is myelosuppressie bij patiënten die langer dan 14 dagen linezolid kregen.24,25 hoewel verkrijgbaar als een orale formulering, wordt het niet zo veel gebruikt in de poliklinische omgeving als gevolg van de kosten., Het is ook niet gedekt onder veel verzekeringspolissen, dus patiënten kunnen nodig zijn om de fabrikant van de patiënt bijstand programma ‘ s te gebruiken.
Daptomycine (Cubicin), een lipopeptide-antibioticum met een snelle bactericide werking, is goedgekeurd voor de behandeling van gecompliceerde infecties van de huid en weke delen, evenals bacteriëmie veroorzaakt door MRSA.26 zijn werkingsmechanisme impliceert depolarisatie van de bacteriële celwand. Bijwerkingen van daptomycine zijn onder meer verhoogd creatinekinase (CK) en rabdomyolyse, vooral bij patiënten die gelijktijdig HMG-CoA-reductaseremmers (statines) gebruiken., Daarom moeten wekelijkse CK-spiegels worden getrokken terwijl een patiënt daptomycine krijgt. Er moet ook worden opgemerkt dat er gevallen van MRSA-resistentie tegen daptomycine zijn gemeld, vooral bij langdurig gebruik en bij patiënten die eerder aan vancomycine waren blootgesteld.26-28 Daptomycine mag niet worden gebruikt voor de behandeling van MRSA-pneumonie omdat de activiteit ervan wordt geremd door pulmonale oppervlakteactieve stoffen.
Quinupristin-dalfopristin (Synercid) is een streptogramine die werkzaam is tegen MRSA., Hoewel het niet door de FDA is goedgekeurd voor gebruik bij MRSA-infecties, wordt het gebruikt bij infecties van de huid en weke delen bij patiënten die intolerant zijn voor of falen bij vancomycine-therapie. Omdat deze behandeling slecht wordt verdragen door patiënten, is het gebruik ervan beperkt in de klinische praktijk.Enkele van de belangrijkste bijwerkingen zijn hyperbilirubinemie, myalgieën en artralgieën. Op basis van deze factoren, wordt dit middel alleen gebruikt als een laatste optie wanneer patiënten hebben gefaald of andere middelen niet kunnen verdragen.,
nieuwere therapieën
Tigecycline (Tygacil) is de eerste bacteriostatische stof in de glycylcycline klasse van antibiotica (een synthetisch derivaat van tetracycline). Het is geïndiceerd voor de behandeling van gecompliceerde infecties van de huid en de huidstructuur (csssi), gecompliceerde intra-abdominale infecties en door MRSA veroorzaakte longontsteking.Tigecycline dient niet routinematig te worden gebruikt voor bacteriëmie vanwege bezorgdheid over het bereiken van onvoldoende serumspiegels., Omdat tigecycline een breedspectrumantibioticum is, dient het gebruik ervan beperkt te worden tot ernstige en levensbedreigende infecties bij gehospitaliseerde patiënten.
telavancine (Vibativ) is het nieuwste geneesmiddel dat door de FDA wordt goedgekeurd voor de behandeling van MRSA-infecties.Het is een lipoglycopeptide vergelijkbaar met vancomycine, hoewel het werkingsmechanisme verschilt. Telavancine verstoort de permeabiliteit van het celmembraan door depolarisatie van het plasmamembraan, waardoor de permeabiliteit en lekkage van cellulair adeno-sininetrifosfaat en kalium (K+) toeneemt., De timing van deze veranderingen correleert met een snel, concentratie-afhankelijk verlies van bacteriële levensvatbaarheid, wat erop wijst dat de vroege bactericide activiteit van telavancine het gevolg is van dissipatie van het celmembraan potentieel en een toename van de membraanpermeabiliteit.
klinische studies hebben aangetoond dat telavancine niet-inferieur is aan vancomycine bij de behandeling van cSSSI.Eén voordeel dat telavancine heeft ten opzichte van vancomycine is eenmaal daags doseren en er is geen noodzaak voor het monitoren van geneesmiddelconcentraties. Echter, net als vancomycine, moet de dosis worden aangepast bij patiënten met nierinsufficiëntie.,Bij alle patiënten moet de nierfunctie gecontroleerd worden tijdens en na stopzetting van de behandeling. Telavancine wordt geassocieerd met QTc-verlenging en moet met voorzichtigheid worden gebruikt bij patiënten die geneesmiddelen gebruiken die ook QTc kunnen verlengen. In klinische onderzoeken waarin telavancine werd vergeleken met vancomycine, waren de bijwerkingen die werden gemeld bij meer dan 10% van de met telavancine behandelde patiënten onder meer smaakstoornissen, misselijkheid, braken en schuimige urine.Ernstige bijwerkingen werden gemeld bij 7% van de patiënten behandeld met telavancine en omvatten meestal nier -, respiratoire of cardiale bijwerkingen., Er is een “black box” – waarschuwing met betrekking tot het foetale risico geassocieerd met het gebruik van telavancine; daarom moeten vrouwen in de vruchtbare leeftijd vóór het begin van telavancine een zwangerschapstest in serum ondergaan.
Ceftobiprole (Zeftera) is het eerste cefalosporine met bactericide werking tegen MRSA. Zijn antibacteriële activiteit omvat het remmen van de penicilline-bindende proteã nen betrokken bij de synthese van de celwand. In klinische studies was het bij de behandeling van cSSSI even werkzaam als de combinatie van vancomycine en ceftazidim.,Het wordt over het algemeen goed verdragen, met de belangrijkste bijwerkingen waaronder misselijkheid en smaakstoornissen. Ceftobiprole is momenteel niet goedgekeurd voor gebruik in de V. S., en hoewel het eerder voor gebruik in Canada werd goedgekeurd, beëindigde de fabrikant de verkoop van de drug vanaf 16 April 2010.35 dit volgde aanbevelingen van regelgevende instanties in Europa (Europees Comité voor geneesmiddelen voor menselijk gebruik) en de V. S. (FDA) niet om de drug goed te keuren., Hoewel de resultaten van Fase III op het voordeel van ceftobiprole duidden, waren er zorgen over de integriteit van deze studieresultaten als gevolg van knoeien met klinische gegevens van sommige van de studieplaatsen. Met deze recente ontwikkeling, de toekomst van ceftobiprole gebruik in de Amerikaanse markt blijft twijfelachtig.
conclusie
met het ontstaan van zowel CA-MRSA als heteroresistente MRSA is het belangrijk dat apothekers bekend zijn met alle middelen die beschikbaar zijn voor de behandeling van MRSA-infecties. Het is ook essentieel om het geschikte antimicrobiële middel voor de besmetting te kiezen die wordt behandeld., Daarnaast dienen middelen met een breder activiteitenspectrum (bijv. tigecycline) gereserveerd te worden voor zeer ernstige infecties en in de setting van multipathogene infecties. Het is ook van het grootste belang om de nieuwere middelen te reserveren voor ernstigere infecties om de ontwikkeling van resistentie te minimaliseren.
1. Boucher HW, Corey GR. Epidemiologie van methicilline-resistente Staphylococcus aureus. Clin Infecteert Dis.
2. Styers D, Sheehan DJ, Hogan P, et al., Laboratorium-gebaseerde surveillance van huidige antimicrobiële resistentie patronen en trends onder Staphylococcus aureus: 2005 status in de Verenigde Staten. Ann Clin Microbiol Antimicrob. 2006;5:2.
3. Chien JW, Kucia ML, Salata RA. Gebruik van linezolid, een oxazolidinon, bij de behandeling van multidrug-resistente gram-positieve bacteriële infecties. Clin Infecteert Dis. 2000;30:146-151.
4. Soriano A, Martinez JA, Mensa J, et al. Pathogene betekenis van methicilline resistentie voor patiënten met Staphylococcus aureus bacteriëmie. Clin Infecteert Dis. 2000;30:368-673.
5. Graffunder EM, Venezia RA., Risicofactoren geassocieerd met nosocomiale methicilline-resistente Staphylococcus aureus (MRSA) infectie, waaronder eerder gebruik van antimicrobiële stoffen. J Antimicrob Chemotherium. 2002;49:999-1005.
6. Klevens RM, Edwards JR, TENOVER FC, et al. Veranderingen in de epidemiologie van methicilline-resistente Staphylococcus aureus in intensive care units in Amerikaanse ziekenhuizen, 1992-2003. Clin Infecteert Dis.
7. Levine DP, Cushing RD, Jui J, Brown WJ. Door de gemeenschap verworven methicilline-resistente Staphylococcus aureus endocarditis in het Detroit Medical Center. Ann Stagiair Med. 1982;97:330-338.
8., Lodise TP Jr, McKinnon PS, Rybak M. Prediction model to identify patients with Staphylococcus aureus bacteremia at risk for methicillin resistance. Infecteren Controle Hosp Epidemiol. 2003;24:655-661.
9. King MD, Humphrey BJ, Wang YF, et al. Opkomst van in de gemeenschap verworven methicilline-resistente Staphylococcus aureus USA 300 kloon als de belangrijkste oorzaak van huid-en weke delen infecties. Ann Stagiair Med. 2006;144:309-317.
10. Centres for Disease Control and Prevention., Methicilline-resistente Staphylococcus aureus infecties onder concurrerende sport deelnemers-Colorado, Indiana, Pennsylvania, en Los Angeles County, 2000-2003. MMWR. 2003;52:793-795.
11. Lowy FD. Staphylococcus aureus infecties. N Engl J Med. 1998;339:520-532.
12. Chambers HF. De veranderende epidemiologie van Staphylococcus aureus? Emerg Infecteert Dis.
13. Community-associated MRSA informatie voor clinici. CDC. www.cdc.gov/ncidod/dhqp/ar_ 2008; 46 (suppl 5): S344-S349. 2006;42:389-391. 2001;7:178-182.mrsa_ca_clinicians.HTML. Geraadpleegd Op 4 Juli 2010.
14. Rybak MJ, LaPlante KL., Community-associated methicilline-resistente Staphylococcus aureus; een overzicht. Farmacotherapie. 2005;25:74-85.
15. Gorwitz RJ, Jernigan DB, Powers JH, et al. Strategies for clinical management of MRSA in the community: samenvatting van een deskundigenvergadering bijeengeroepen door de Centers for Disease Control and Prevention. Maart 2006. www.cdc.gov/ncidod/dhqp/pdf/ar/CAMRSA_ExpMtgStrategies.pdf. Geraadpleegd op 4 juli 2010.
16. Sabol KE, Echevarria KL, Lewis JS II. Community-associated methicillin-resistente Staphylococcus aureus: new bug, old drugs. Ann Pharmacother. 2006;40:1125-1133.
17., Cleocin (clindamycin) bijsluiter. New York, NY: Pfizer Inc; November 2005.
18. Strom BL, Schinnar R, Apter AJ, et al. Afwezigheid van kruisgevoeligheid tussen sulfonamide antibiotica en sulfonamide nonantibiotica. N Engl J Med. 2003;349:1628-1635.
19. Nicolau DP, Freeman CD, Nightingale CH, et al. Minocycline versus vancomycine voor de behandeling van experimentele endocarditis veroorzaakt door oxacilline-resistente Staphylococcus aureus. Antimicrob Middelen Chemotheric. 1994;38:1515-1518.
20. Sakoulas G, Moellering RC Jr., Toenemende antibioticaresistentie onder methicilline-resistente Staphylococcus aureus stammen. Clin Infecteert Dis. 2008; 46 (suppl 5): S360-S367.
21. Rybak MJ, Akins RL. Opkomst van methicilline-resistente Staphylococcus aureus met intermediaire glycopeptiden resistentie: klinische significantie en behandelingsopties. Drugs. 201;61:1-7.
22. Tenover FC, Moellering RC Jr. de reden voor de herziening van de klinische en laboratorium Standards Institute vancomycine minimal inhibitory concentration interpretive criteria voor Staphylococcus aureus. Clin Infecteert Dis. 2007;44:1208-1215.
23., Jeffres MN, Micek ST, Isakow W, et al. Verhoogde incidentie van nefrotoxiciteit bij hogere dalconcentraties in het serum van vancomycine. Programma en samenvattingen van de 46e Interscience Conference on Antimicrobial Agents and Chemotherapy (ICAAC); 27-30 September 2006; San Francisco, CA. Abstract K789.
24. Zyvox (linezolide) bijsluiter. New York, NY: Pfizer Inc; December 2009.
25. Kuter DJ, Tillotson GS. Hematologische effecten van antimicrobiële stoffen, een focus op de oxazolidinon, linezolide. Farmacotherapie. 201;21:1010-1013.
26. Cubicin (daptomycine) bijsluiter., Lexington, MA: Cubist Pharmaceuticals; January 2010.
27. Murthy MH, Olson ME, Wickert RW, et al. Daptomycin non-susceptible methicillin-resistant Staphylococcus aureus USA 300 isolate. J Med Microbiol. 2008;57:1036-1038.
28. Mangili A, Bica I, Snydman R, Hamer DH. Daptomycin-resistant methicillin-resistant Staphylococcus aureus bacteremia. Clin Infect Dis. 2005;40:1058-1060.
29. Synercid (quinupristin-dalfopristin) package insert. Greenville, NC: Monarch Pharmaceuticals; June 2008.
30. Tygacil (tigecycline) package insert. Philadelphia, PA: Wyeth Pharmaceuticals; September 2009.,
31. VIBATIV (telavancine) bijsluiter. Deerfield, IL: Astellas Pharma US, Inc; September 2009.
32. Stryjewski ME, Chu VH, O ‘ Riordan WD, et al. Telavancine versus standaardtherapie voor de behandeling van gecompliceerde huid-en huidstructuur infecties veroorzaakt door grampositieve bacteriën: FAST 2 studie. Antimicrob Middelen Chemotheric. 2006;50:862-867.
33. Corey GR. Studies van telavancine bij cSSSI. Paper presented at: Third International Symposium on Resistant Gram-Positive Infections; October 10, 2006; Niagara-on-the-Lake, Canada.
34. Vidaillac C, Rybak MJ., Ceftobiprole: first cephalosporin with activity against methicillin-resistant Staphylococcus aureus. Pharmacotherapy. 2009;29:511-525.
35. Discontinuation of the sale of ceftobiprole in Canada. Basilea Pharmaceutica. April 9, 2010. http://hugin.info/134390/R/1401931/356785.pdf. Accessed July 12, 2010.
36. Vibramycin (doxycycline) package insert. New York, NY: Pfizer Inc; April 2007.
37. Minocin (minocycline) package insert. Philadelphia, PA: Triax Pharmaceuticals; March 2006.
38. Bactrim (trimethoprim-sulfamethoxazole) package insert. Philadelphia, PA: AR Scientific; November 2006.
39., Vancocin (vancomycin) package insert. Exton, PA: ViroPharma Inc; October 2005.