leerdoelen
- beschrijven een antilichaammolecuul.
- teken de” stokfiguur ” – structuur van IgG, met vermelding van het Fab-gedeelte (variabel gebied) en het Fc-gedeelte (constant gebied).
- vermeld de functies van de Fab-en de Fc-delen van een antilichaam.
- Wat wordt bedoeld met de biologische activiteit van een antilichaam.
- vergelijk de structuur van IgM en secretoire IgA met die van IgG.
In deze sectie zullen we kijken naar de structuur van antilichamen., Er zijn vijf klassen of ISO-types van humane antilichamen:
- immunoglobuline G (IgG),
- immunoglobuline M (IgM),
- immunoglobuline A (IgA),
- immunoglobuline D (IgD) en
- immunoglobuline E (IgE).
De eenvoudigste antilichamen, zoals IgG, IgD en IgE, zijn “Y”-vormige macromoleculen die monomeren worden genoemd. Een monomeer bestaat uit vier glycoproteïnekettingen: twee identieke zware ketens en twee identieke lichte ketens. De twee zware kettingen hebben een hoog molecuulgewicht dat met de klasse van antilichaam varieert., De lichte kettingen zijn er in twee varianten: kappa of lambda en hebben een lager molecuulgewicht dan de zware kettingen. De vier glycoproteïnekettingen zijn met elkaar verbonden door disulfide (S-S) bindingen en niet-covalente bindingen (figuur \(\Paginindex{1}\)).
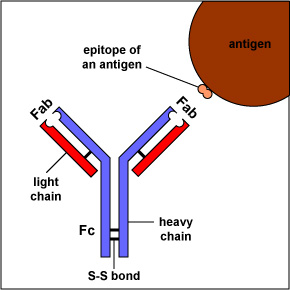
aanvullende S-S-bindingen vouwen de afzonderlijke glycoproteïneketens in een aantal afzonderlijke bolvormige domeinen (figuur \(\Paginindex{2}\)). Het gebied waar de bovenkant van de ” Y ” de bodem verbindt wordt het scharnier genoemd. Dit gebied is flexibel om het antilichaam toe te laten om aan paren van epitopes diverse afstanden apart op een antigeen te binden.
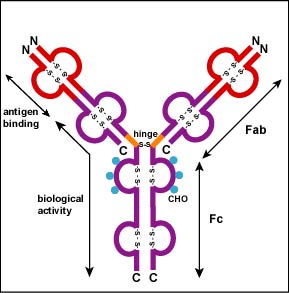
de twee uiteinden van het” Y ” -monomeer worden aangeduid als de antigeen-bindende fragmenten of Fab-delen van het antilichaam (figuren 1-3)., De eerste 110 aminozuren of het eerste domein van zowel de zware als lichte ketting van het Fab-gebied van het antilichaam verstrekken specificiteit voor het binden van een epitope op een antigeen. De aminozuuropeenvolging van dit eerste domein van zowel de lichte keten als de zware ketting toont enorme variatie van antilichaam aan antilichaam en vormt het variabele gebied (V-gebied)., Dit is omdat elke B-lymfocyt, vroeg in zijn ontwikkeling, genetisch wordt geprogrammeerd door een reeks gen-verbindende reacties om Fab met een unieke 3-dimensionale vorm te produceren geschikt om één of andere epitope aan een overeenkomstige vorm te passen.
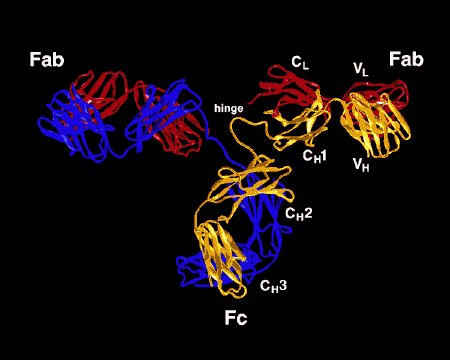
figuur \(\Paginindex{3}\): Linttekening van het Antilichaammolecuul IgG2a, een linttekening van het eerste intacte antilichaammolecuul ooit gekristalliseerd (IgG2a). Het Fab-gedeelte van het antilichaam heeft specificiteit voor het binden van een epitope van een antigeen. Het Fc-gedeelte leidt de biologische activiteit van het antilichaam.,
de verschillende genen de celsplitsen samen bepalen de volgorde van aminozuren van het Fab-gedeelte van zowel de lichte als de zware keten; de aminozuurvolgorde bepaalt de uiteindelijke 3-dimensionale vorm (figuur \(\Pagindex{4}\)). Daarom zullen de verschillende antilichaammolecules door verschillende B-lymfocyten worden geproduceerd verschillende orden van aminozuren bij de uiteinden van Fab hebben om hen unieke vormen voor bindende epitope te geven. De antigeen-bindende plaats is groot genoeg om een epitope van ongeveer 5-7 aminozuren of 3-4 suikerresiduen te houden., Epitopen binden aan het Fab-gedeelte van het antilichaam door reversibele, niet-covalente bindingen.
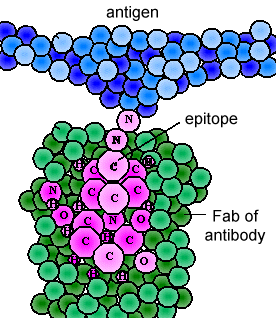
het onderste deel van de “Y”, Het C terminale gebied van elke glycoproteïneketen, is het FC-gedeelte., Het Fc-gedeelte, evenals één domein van zowel de zware als lichte keten van het Fab-gebied heeft een constante aminozuuropeenvolging en als constant gebied (c-gebied) van het antilichaam wordt bedoeld en definieert de klasse en de subklasse van elk antilichaam. Het Fc-gedeelte is verantwoordelijk voor de biologische activiteit van het antilichaam (figuren 1-3), echter, wordt het Fc-gedeelte pas biologisch actief nadat de Fab-component aan zijn overeenkomstige antigeen heeft gebonden., Afhankelijk van de klasse en subklasse van antilichaam, biologische activiteiten van het Fc-gedeelte van antilichamen omvatten de mogelijkheid om:
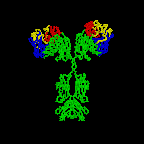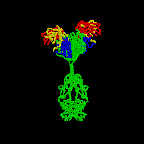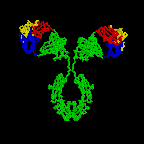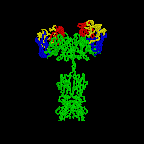
Individuele “Y”-vormige antilichaam moleculen zijn de zogenaamde monomeren en kan binden aan twee identieke epitopen. De antilichamen van de klassen IgG, IgD, en IgE zijn monomeren.
twee klassen antilichamen zijn complexer., IgM (zie figuur \(\Paginindex{10}\)) is een pentamer, bestaande uit 5 “Y”-achtige moleculen verbonden aan hun Fc-delen door een “J” of verbindingsketen. Secretoire IgA (zie figuur \(\Pagindex{11}\)) is een dimeer bestaande uit 2 “Y”-achtige moleculen verbonden aan hun Fc-delen door een “J” – keten en gestabiliseerd om enzymatische spijsvertering in lichaamsafscheiding te weerstaan door middel van een secretoire component.
samenvatting
- Er zijn 5 klassen of ISO-types van humane antilichamen of immunoglobulinen: IgG, IgM, IgA, IgD en IgE.,
- de eenvoudigste antilichamen, zoals IgG, IgD en IgE, zijn “Y”-vormige macromoleculen die monomeren worden genoemd en bestaan uit vier glycoproteïnekettingen: twee identieke zware ketens en twee identieke lichte ketens.
- de twee uiteinden van het” Y ” -monomeer worden aangeduid als de antigeen-bindende fragmenten of Fab-delen van het antilichaam en deze delen bieden specificiteit voor het binden van een epitoop op een antigeen.,in het begin van zijn ontwikkeling wordt elke B-lymfocyt genetisch geprogrammeerd door middel van een reeks gen-splicing reacties om een Fab te produceren met een unieke 3-dimensionale vorm die in staat is om een epitoop met een overeenkomstige vorm aan te passen.
- Het Fc-gedeelte wordt pas biologisch actief nadat de Fab-component aan het overeenkomstige antigeen is gebonden. De biologische activiteiten omvatten het activeren van de complementwegen, en het binden aan receptoren op fagocyten en andere defensiecellen om aanpassingsimmuniteit te bevorderen.
- IgM is een pentamer, bestaande uit 5 monomeren die bij hun Fc-porties zijn gevoegd.,
- IgA is een dimeer, bestaande uit 2 monomeren die bij hun Fc-porties zijn gevoegd.
vragen
bestudeer het materiaal in deze sectie en schrijf de antwoorden op deze vragen op. Klik niet alleen op de antwoorden en schrijf ze uit. Dit zal uw begrip van deze tutorial niet testen.
- Beschrijf een antilichaammolecuul. (ans)
- komen als volgt overeen:
_____ het gebied van het antilichaam dat specificiteit biedt voor het binden van een epitoop aan een antigeen., (ans)
_____ het gebied van het antilichaam dat verantwoordelijk is voor de biologische activiteit van het antilichaam. (ans)
_____ bestaat uit vier glycoproteïneketens. Er zijn twee identieke zware kettingen met een hoog molecuulgewicht en twee identieke lichte kettingen. (ans)
_____ een pentamer, bestaande uit 5 “Y”-achtige moleculen verbonden aan hun Fc-delen door een “J” of verbindingsketen. (ans)
_____ een dimeer bestaande uit 2 “Y”-achtige moleculen verbonden aan hun Fc-delen door een “J” – keten en gestabiliseerd om weerstand te bieden aan enzymatische spijsvertering., (ans)
- IgM
- secretory IgA
- IgG
- Fab
- Fc
- Multiple Choice (ans)
bijdragers en Attributies
Dr. Gary Kaiser (Community College of Baltimore County, Catonsville campus)