Nedbør Reaksjoner og Løselighet Regler
En nedbør reaksjon er en som oppløste stoffer reagerer med å danne ett (eller flere) faste produkter. Mange reaksjoner av denne typen innebærer utveksling av ioner mellom ioniske forbindelser i vandig løsning og er noen ganger referert til som dobbelt vekt, dobbel erstatning, eller metatese reaksjoner., Disse reaksjonene er vanlig i naturen og er ansvarlig for dannelsen av korallrev i havet farvann og nyrestein i dyr. De brukes mye i industrien for produksjon av en rekke råvarer og spesialitet kjemikalier. Nedbør reaksjoner også spille en sentral rolle i mange kjemiske analyse-teknikker, inkludert spot tester som brukes til å identifisere metall ioner og gravimetrisk metoder for å bestemme sammensetningen av saken (se siste modul av dette kapitlet).,
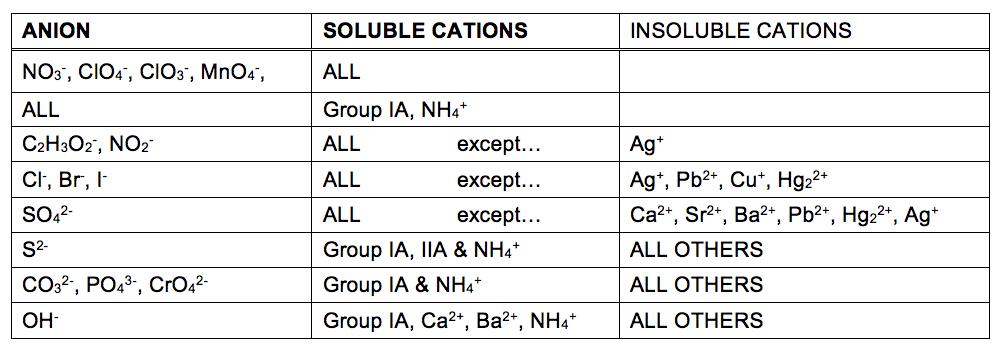
Den grad et stoff kan være oppløst i vann eller løsemidler, er kvantitativt uttrykt som sin løselighet, definert som maksimal konsentrasjon av et stoff som kan oppnås under spesifiserte betingelser. Stoffer med relativt store solubilities er sagt å være løselig. Et stoff vil bunnfall når løsningen forholdene er slik at konsentrasjonen overstiger sin løselighet. Stoffer med relativt lave solubilities er sagt å være uløselig, og dette er stoffer som lett bunnfall fra løsning., Mer informasjon om disse viktige begreper er gitt i teksten, kapittel på løsninger. Med henblikk på å forutsi identiteter av faste stoffer dannet av nedbør reaksjoner, kan man bare se mønstre av løselighet som har vært observert i mange ioniske forbindelser (Tabell 1).
Et levende eksempel på nedbør er observert når løsninger av kalium jodid og føre nitrat er blandet, noe som resulterer i dannelsen av solid ledelse jodid:
Denne observasjonen er i samsvar med oppløselig retningslinjer: bare uløselige forbindelsen mellom alle de involverte er føre jodid, en av de unntak fra den generelle løseligheten av jodid salter.,
nettet ioniske ligningen som representerer denne reaksjonen er:
Føre jodid er en lys gul solid som tidligere ble brukt som en kunstners pigment kjent som jod gul (Figur 1). Egenskapene til rent PbI2 krystaller gjøre dem nyttige for fabrikasjon av røntgen og gamma ray-detektorer.

løselighet tabell i Tabell 1 kan brukes til å forutsi om en ventet reaksjon oppstår når løsninger av løselig ioniske forbindelser er blandet sammen. Man bare trenger å identifisere alle ioner tilstede i løsningen, og deretter vurdere om det er mulig kation/anion sammenkobling kan resultere i et uløselig stoff.
For eksempel, å blande løsninger av silver nitrat og sodium fluorid, vil gi en løsning som inneholder Ag+, NO3−, Na+, og F− ioner., Bortsett fra de to ioniske forbindelser, som opprinnelig er til stede i løsninger, AgNO3 og NaF, to ekstra ioniske forbindelser som kan være avledet fra denne samlingen av ioner: NaNO3 og AgF.
løselighet tabellen viser alle nitrat salter er løselig, men at AgF er en av de unntak fra den generelle løseligheten av fluor salter. En nedbør reaksjon, derfor er spådd til å skje, som beskrevet ved følgende ligninger: