12.7 Buffere
Mål
- Definere buffer.
- identifisere de to komponentene i en buffer.
Som angitt i Avsnitt 12.4 «Sterke og Svake Syrer og Baser og Deres Salter», svake syrer er relativt vanlig, selv i maten vi spiser. Men vi opplever en sterk syre eller base, for eksempel mage syre, som har et sterkt sure pH-verdi på 1.7. Ved definisjon, sterke syrer og baser kan produsere et relativt store mengden av H+ eller OH− ioner og følgelig har merket kjemiske aktiviteter., I tillegg, svært små mengder av sterke syrer og baser kan endre pH i en løsning raskt. Hvis 1 mL av magen syre ble lagt til blodet og ingen korrigerende mekanisme var til stede, og pH i blodet vil reduseres fra om lag 7,4 til om 4.7—en pH som ikke bidrar til fortsatt levende. Heldigvis, kroppen har en mekanisme for å minimere slike dramatiske pH-endringer.
mekanismen innebærer en bufferA løsning som motstår dramatiske endringer i pH., en løsning som motstår dramatiske endringer i pH., Buffere gjøre det ved å være sammensatt av visse par av solutes: enten en svak syre, pluss et salt som er avledet fra at svak syre eller en svak base, pluss et salt av at svak base. For eksempel, en buffer som kan være sammensatt av oppløst HC2H3O2 (en svak syre) og NaC2H3O2 (salt avledet fra at svak syre). Et annet eksempel på en buffer er en løsning som inneholder NH3 (en svak base) og NH4Cl (et salt som er avledet fra at svak base).
La oss bruke en HC2H3O2/NaC2H3O2 buffer for å demonstrere hvordan buffere arbeid., Hvis en sterk base—en kilde til OH−(aq) ioner—er lagt til bufferløsning, de som OH− ioner vil reagere med HC2H3O2 i en syre-base-reaksjon:
HC2H3O2(aq) + OH−(aq) → H2O(står) + C2H3O2−(aq)
Snarere enn å endre pH dramatisk ved å gjøre løsningen grunnleggende, som er lagt til OH− ioner reagerer med å gjøre H2O, slik at pH-verdien og endrer seg ikke mye.
Hvis en sterk syre—en kilde av H+ – ioner—er lagt til buffer løsning, H+ – ioner vil reagere med anion fra salt. Fordi HC2H3O2 er en svak syre, det er ikke ionisert mye., Dette betyr at hvis det er massevis av H+ – ioner og C2H3O2− ioner er tilstede i samme løsning, de vil komme sammen for å gjøre HC2H3O2:
H+(aq) + C2H3O2−(aq) → HC2H3O2(aq)
Snarere enn å endre pH dramatisk og gjør at løsningen er sur, er lagt til H+ – ioner reagerer med å lage molekyler av en svak syre. Figur 12.2 «Handlinger av Buffere» illustrerer både handlinger av en buffer.
Figur 12.2 Handlinger av Buffere
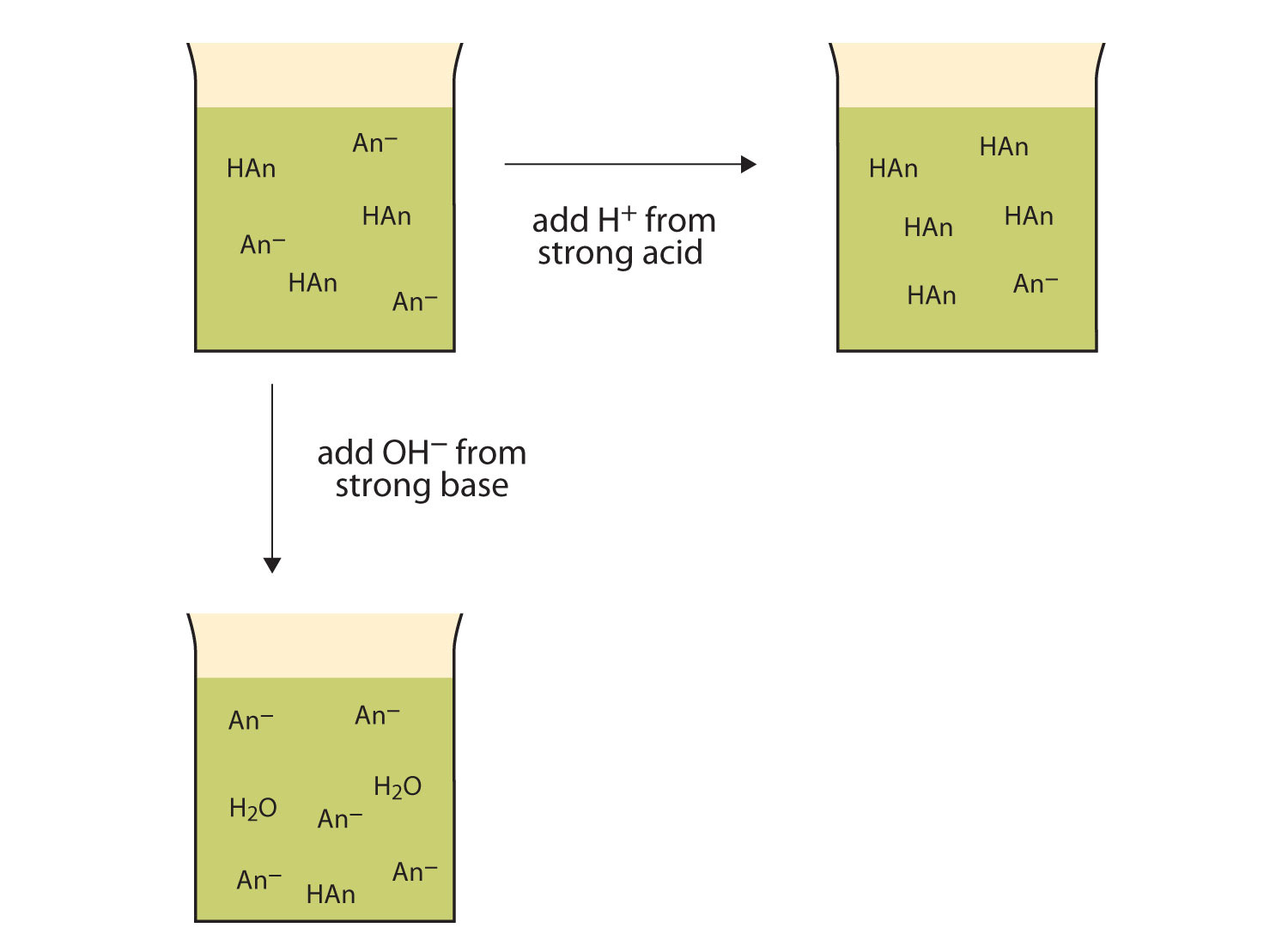
– Bufferen, kan reagere med både sterke syrer (øverst) og sterke baser (side) for å minimere store endringer i pH.,
Buffere laget fra svake baser og salter av svake baser handle på samme måte. For eksempel, i en buffer som inneholder NH3 og NH4Cl, NH3 molekyler som kan reagere med noe overskudd av H+ – ioner introdusert av sterke syrer:
NH3(aq) + H+(aq) → NH4+(aq)
mens NH4+(aq) ion kan reagere med noen OH− ioner introdusert av sterke baser:
NH4+(aq) + OH−(aq) → NH3(aq) + H2O(står)
Eksempel 15
Hvilke kombinasjoner av forbindelser kan gjøre en buffer løsning?,
- HCHO2 og NaCHO2
- HCl og NaCl
- CH3NH2 og CH3NH3Cl
- NH3 og NaOH
Løsningen
- HCHO2 er maursyre, en svak syre, mens NaCHO2 er salt laget fra anion av svak syre (den formiat ion ). Kombinasjonen av disse to solutes ville gjøre en bufferløsning.
- HCl er en sterk syre, ikke en svak syre, så kombinasjonen av disse to solutes ville ikke gjøre en bufferløsning.
- CH3NH2 er methylamine, som er som NH3 med en av sine H-atomer erstattet med en CH3-gruppe. Fordi det er ikke listet opp i Tabell 12.,2 «Sterke Syrer og Baser», kan vi anta at det er en svak base. Det sammensatte CH3NH3Cl er en salt-laget fra at svak base, så kombinasjonen av disse to solutes ville gjøre en bufferløsning.
- NH3 er en svak base, men NaOH er en sterk base. Kombinasjonen av disse to solutes ville ikke gjøre en bufferløsning.
Test deg Selv
Hvilke kombinasjoner av forbindelser kan gjøre en buffer løsning?,
- NaHCO3 og NaCl
- H3PO4 og NaH2PO4
- NH3 og (NH4)3PO4
- NaOH og NaCl
Svar
- nei
- ja
- ja
- nei
Bufrer jobber vel bare for begrensede mengder lagt sterk syre eller base. Når enten oppløst stoff er helt reagerte, løsningen er ikke lenger en buffer, og raske endringer i pH kan oppstå. Vi sier at en buffer har en viss capacityThe mengden av sterk syre eller base en buffer som kan motvirke.., Buffere som har mer oppløst stoff oppløst i dem til å begynne med har større kapasitet, som kan forventes.
Humant blod har et nytt system for å minimere store endringer i pH. En buffer i blodet er basert på tilstedeværelsen av HCO3− og H2CO3 . Med denne bufferen til stede, selv om noen av magen syre var å finne veien direkte inn i blodbanen, endring i pH i blodet ville være minimal. Inne i mange av kroppens celler, det er et nytt system basert på fosfat ioner.,
Mat og Drikke App: Syre Som Demper Smerte
Selv om medisinene er ikke akkurat «mat og drikke,» vi gjør sluker dem, så la oss ta en titt på en syre som er trolig den mest vanlig medisin: acetylsalisylsyre, også kjent som aspirin. Aspirin er godt kjent som et smertestillende og febernedsettende (feber redusering).
strukturen av aspirin er vist i etterfølgende figur. Syre del er omringet; det er på H-atom i den delen som kan bli donert som aspirin fungerer som en Brønsted-Lowry syre. Fordi det ikke er gitt i Tabell 12.,2 «Sterke Syrer og Baser», acetylsalisylsyre er en svak syre. Det er imidlertid fortsatt en syre, og gitt at noen mennesker bruker relativt store mengder av aspirin daglig, sin sure naturen kan føre til problemer i mageslimhinnen, til tross for magen forsvar mot sin egen mage syre.
Figur 12.3 Den Molekylære Strukturen av Aspirin
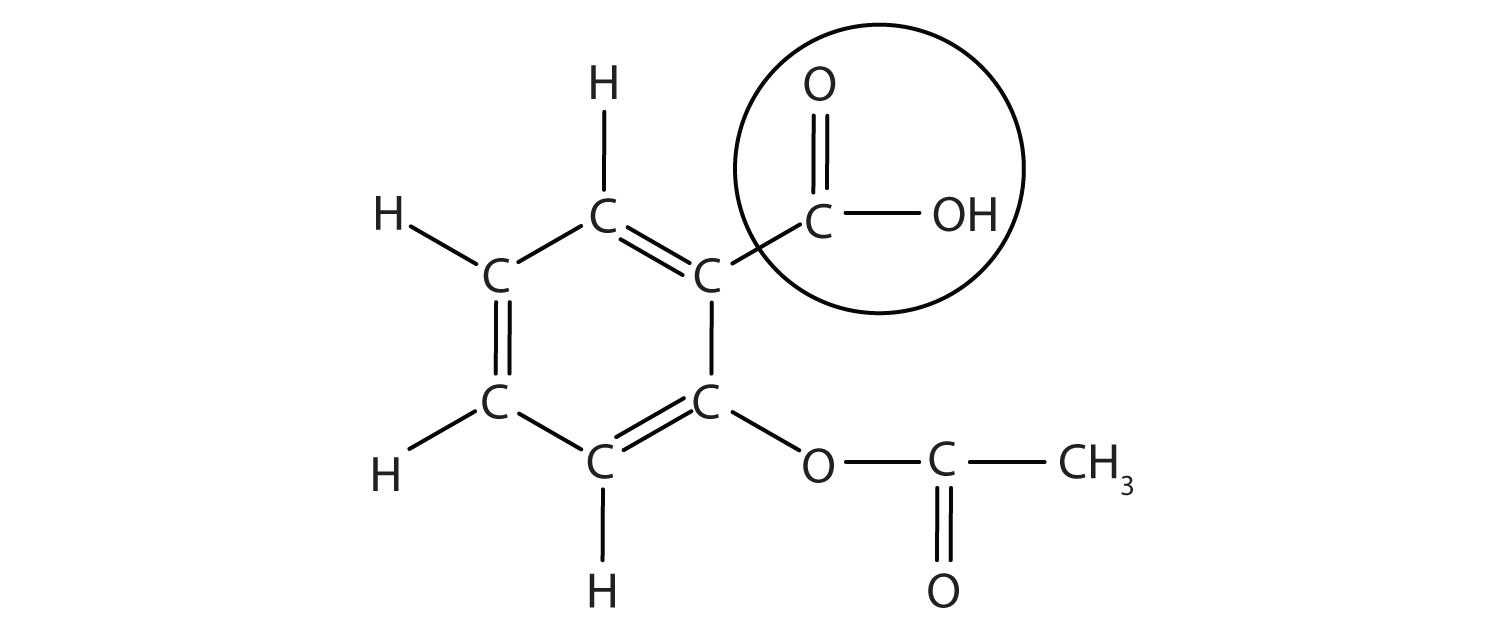
sirklet atomer er den avgjørende delen av molekylet.
Fordi acid egenskaper av aspirin kan være problematisk, mange aspirin merker tilbyr en «bufret aspirin» form for medisin., I disse tilfellene, aspirin inneholder også en buffering agent—vanligvis MgO—som regulerer surhet av aspirin for å minimere sin sure bivirkninger.
Som nyttig og vanlig som aspirin er det formelt ble markedsført som et stoff som starter i 1899. US Food and Drug Administration (FDA), den statlig etat belastet med tilsyn og godkjenning av legemidler i Usa, ble ikke dannet før i 1906., Noen har hevdet at hvis FDA hadde blitt dannet før aspirin ble innført, aspirin kan aldri ha fått godkjenning på grunn av dens potensial for bivirkninger—gastrointestinal blødning, ringing i ørene, Reye syndrom (en lever problem), og noen allergiske reaksjoner. Men nylig aspirin har vært spioneringen for dens virkninger i lessening hjerteinfarkt og slag, så er det sannsynlig at aspirin er her for å bli.
– Tasten Takeaway
- en buffer er En løsning som tåler plutselige endringer i pH.
Øvelser
-
Angi buffer., Hva to beslektede kjemiske komponentene som kreves for å lage en buffer?
-
Kan en buffer gjøres ved å kombinere en sterk syre med en sterk base? Hvorfor eller hvorfor ikke?
-
Hvilke kombinasjoner av forbindelser kan gjøre en buffer? Anta vandige løsninger.
- HCl og NaCl
- HNO2 og NaNO2
- NH4NO3 og HNO3
- NH4NO3 og NH3
-
Hvilke kombinasjoner av forbindelser kan gjøre en buffer? Anta vandige løsninger.,
- H3PO4 og Na3PO4
- NaHCO3 og Na2CO3
- NaNO3 og Ca(NO3)2
- HN3 og NH3
-
For hver kombinasjon i Øvelse 3 som er en buffer, skriv den kjemiske ligninger for reaksjoner av buffer-komponenter når en sterk syre og sterk base er lagt til.
-
For hver kombinasjon i Øvelse 4, som er en buffer, skriv den kjemiske ligninger for reaksjoner av buffer-komponenter når en sterk syre og sterk base er lagt til.,
-
hele fosfat buffer system er basert på fire stoffer: H3PO4, H2PO4−, HPO42− og PO43−. Hva ulike buffer-løsninger kan være laget av disse stoffene?
-
Forklar hvorfor NaBr kan ikke være en komponent i en syreholdig eller en grunnleggende buffer.
-
To løsningene er laget med den samme konsentrasjoner av solutes. En løsning er sammensatt av H3PO4 og Na3PO4, mens den andre består av HCN og NaCN. Hvilken løsning som bør ha større kapasitet som en buffer?,
-
To løsningene er laget med den samme konsentrasjoner av solutes. En løsning er sammensatt av NH3 og NH4NO3, mens den andre består av H2SO4 og Na2SO4. Hvilken løsning som bør ha større kapasitet som en buffer?
Svar
-
En buffer er kombinasjonen av en svak syre eller base og et salt av at svak syre eller base.,
-
-
- nei
- ja
- nei
- ja
-
-
3b: sterk syre: NO2− + H+ → HNO2; sterk base: HNO2 + OH− → NO2 + H2O; 3d: sterk base: NH4+ + OH− → NH3 + H2O; sterk syre: NH3 + H+ → NH4+
-
-
– Bufferen kan være laget av tre kombinasjoner: (1) H3PO4 og H2PO4−, (2) H2PO4− og HPO42−, og (3) HPO42− og PO43−. (Teknisk sett, en buffer kan være laget av to komponenter.,)
-
-
fosfat buffer bør ha større kapasitet.
-