US Pharm. 2010; 35(8):HS2-HS4.
Lo Staphylococcus aureus meticillino-resistente (MRSA) è una delle principali cause di infezioni sia sanitarie che acquisite in comunità.1,2 Le infezioni dovute a MRSA sono associate ad un alto rischio di morbilità e mortalità e portano a costi sanitari elevati.3-5 L’incidenza delle infezioni da MRSA negli Stati Uniti è aumentata costantemente negli ultimi anni dal 22% nel 1995 al 60% nel 2003.,6 L’MRSA associato all’assistenza sanitaria (HA-MRSA) è correlato agli ospedali e alle strutture di assistenza a lungo termine ed è comune nei pazienti con ospedalizzazione prolungata, uso antimicrobico passato, ulcere da decubito, dialisi, cateteri interni, poppate enterali o storia di abuso di droghe IV.7,8 Negli ultimi anni, tuttavia, c’è stato un aumento di un nuovo ceppo di MRSA chiamato MRSA associato alla comunità (CA-MRSA)., Questo sembra essere acquisito in ambito ambulatoriale, e la trasmissione avviene attraverso uno stretto contatto fisico, come nei centri diurni, riserve indiane, e strutture correzionali e tra gli atleti, personale militare, e gli uomini che hanno sesso con gli uomini.7,9,10
Distinguere i ceppi MRSA
Diversi rapporti hanno rivelato differenze tra i ceppi HA-MRSA e CA-MRSA, compresa la presenza di diversi genotipi tra i due ceppi. CA-MRSA è suscettibile a diversi antibiotici non beta-lattamici, mentre i ceppi HA-MRSA non lo sono., I ceppi di CA-MRSA hanno maggiori probabilità di codificare alcuni fattori virulenti che sono stati associati a polmonite grave (specialmente nei bambini) e infezioni della pelle e dei tessuti molli negli adulti.8,11,12 Il CDC ha stabilito i criteri per differenziare CA-MRSA da HA-MRSA. Queste linee guida includono l’isolamento di una cultura MRSA positiva entro 48 ore dal ricovero di un paziente in ospedale. Per essere considerato CA-MRSA, il paziente non deve avere uno dei seguenti: ricovero recente; ammissione a una casa di cura, hospice o struttura di cura qualificata; dialisi; o chirurgia recente., Inoltre, il paziente non deve avere cateteri interni o altri dispositivi medici.13
Trattamento di CA-MRSA
Il CDC raccomanda che la gestione e la prevenzione dei focolai di CA-MRSA includa la copertura di infezioni che producono pus, il lavaggio frequente delle mani, la non condivisione di oggetti personali, il lavaggio di biancheria e indumenti sporchi con acqua calda e l’asciugatura di panni in un essiccatore caldo rispetto all’essiccazione all’aria.13 Per gli ascessi cutanei, il trattamento comprende l’incisione e il drenaggio degli ascessi con o senza antibiotici sistemici, a seconda della gravità dell’infezione.,14
Il trattamento di CA-MRSA di solito include l’uso di agenti come clindamicina, tetracicline e trimetoprim-sulfametossazolo (TMP-SMX). L’antibiotico rifampicina non deve mai essere usato in monoterapia per la gestione dell’MRSA. La resistenza si sviluppa rapidamente con rifampicina in monoterapia; tuttavia, se usato in combinazione con un altro agente anti-MRSA, può sradicare gli organismi dai siti di trasporto in modo più efficace.15 Gli antibiotici di cui sopra sono di solito opzioni di trattamento praticabili in pazienti trattati su base ambulatoriale., Nelle infezioni gravi che richiedono il ricovero in ospedale, gli antibiotici IV inclusi vancomicina, linezolid, quinupristin-dalfopristin, daptomicina, tigeciclina e telavancina sono terapie appropriate che possono essere utilizzate (TABELLA 1).
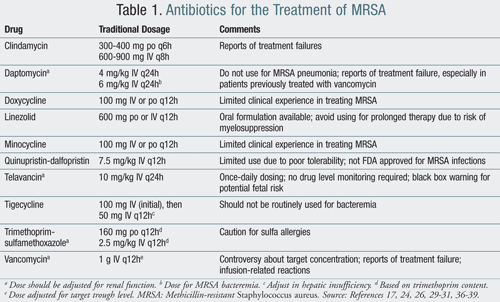
Sebbene la clindamicina (Cleocina) possa essere usata per CA-MRSA, è stata riportata resistenza fino al 19% nei pazienti trattati con essa. Pertanto, i pazienti trattati con clindamicina devono essere monitorati più attentamente per lo sviluppo di resistenza autoindotta.,16 La clindamicina è stata anche associata allo sviluppo di infezioni da clostridium difficile, limitandone l’uso per un periodo prolungato.
TMP-SMX (Bactrim) può essere considerato un’alternativa alla terapia con vancomicina in alcuni casi di infezioni da MRSA. Tuttavia, come con clindamicina, ci sono state segnalazioni di fallimenti del trattamento. Questa terapia ha anche un uso limitato a causa dell’elevata incidenza di allergie sulfamidiche, che sono state segnalate fino al 10% della popolazione.,18
Minociclina (Minocina) e doxiciclina (Vibramicina) sono antibiotici tetracicline che sono stati utilizzati per il trattamento di MRSA. Questi agenti hanno solo dati limitati sull’uso in MRSA, ma è stato riportato un successo clinico.19
Trattamento di HA-MRSA
Gli antibiotici parenterali sono considerati il gold standard per il trattamento di HA-MRSA. Per diversi decenni, l’antibiotico glicopeptide vancomicina è stato ampiamente utilizzato.
La vancomicina (Vancocina) inibisce la sintesi della parete cellulare; tuttavia, ha un’attività battericida più lenta in vitro., Con il suo uso eccessivo, ci sono state segnalazioni di ridotta suscettibilità e l’emergere di vancomicina eteroresistenza in S aureus.20,21 L’aumento di una sottopopolazione di S aureus con concentrazione inibitoria minima (MIC) di>2 mcg/mL alla vancomicina (indicata come MIC creep) è associato a fallimento sia microbiologico che clinico. Il National Committee for Clinical Laboratory Standards (NCCLS) ha proposto nuovi punti di interruzione per vancomicina—cambiando il MIC per “sensibili” da ≤4 mcg/mL a ≤2 mcg/mL.,22 La motivazione di questa proposta si basa in parte su osservazioni cliniche aneddotiche di fallimenti del trattamento durante il trattamento con dosi standard di vancomicina in pazienti con MIC di 4 mcg/mL. Inoltre, livelli minimi più elevati (cioè livelli minimi di 15-20 mcg/mL) possono essere necessari per infezioni gravi come polmonite e osteomielite a causa della scarsa penetrazione dei tessuti da parte della vancomicina. Ci sono state alcune segnalazioni aneddotiche di possibile nefrotossicità associata a questi alti livelli di valle.,
Jeffres et al hanno presentato un abstract alla Conferenza Interscience del 2006 sugli agenti antimicrobici e la chemioterapia (ICAAC) che ha esaminato il rischio di nefrotossicità con livelli minimi di vancomicina più elevati.Nel loro studio, hanno riportato un rischio del 30% di nefrotossicità (definito come un aumento di 0,5 mg/dL o un aumento del 50% della creatinina sierica rispetto al basale) in pazienti con livelli minimi di vancomicina di 315 mcg/mL rispetto al 13% in pazienti con livelli minimi <15 mcg/mL.Alcune popolazioni di pazienti sono a maggior rischio di sviluppare nefro-tossicità indotta dalla vancomicina., Questi includono fattori di rischio noti come l’età avanzata, l’essere in condizioni critiche, la funzione renale inferiore e l’uso concomitante di altri agenti nefrotossici come gli aminoglicosidi. Tutti questi fattori hanno portato ad un aumento della necessità e l’uso degli agenti più recenti.
Linezolid (Zyvox) è il primo ossazolidinone approvato per il trattamento di infezioni della pelle e dei tessuti molli, bacter-emia e polmonite comunitaria e nosocomiale causata da MRSA.24 Inibisce l’inizio della sintesi proteica al ribosoma 50S; tuttavia, a differenza della maggior parte degli altri farmaci, è un agente batteriostatico., I vantaggi del suo utilizzo includono la disponibilità di una formulazione orale che ha eccellenti proprietà di biodisponibilità, senza alcun aggiustamento della dose nei pazienti con insufficienza renale, compresi quelli che ricevono terapie sostitutive renali. Un fattore limitante al suo uso, specialmente per una durata prolungata della terapia, è la mielosoppressione tra i pazienti che hanno ricevuto linezolid per più di 14 giorni.24,25 Sebbene disponibile come formulazione orale, non viene utilizzato tanto in ambito ambulatoriale a causa del suo costo., Inoltre, non è coperto da molte polizze assicurative, quindi i pazienti potrebbero dover utilizzare i programmi di assistenza ai pazienti del produttore.
Daptomicina (Cubicin), un antibiotico lipopeptidico con rapida attività battericida, è approvato per il trattamento di infezioni complicate della pelle e dei tessuti molli, nonché batteriemia causata da MRSA.26 Il suo meccanismo d’azione comporta la depolarizzazione della parete cellulare batterica. Gli effetti collaterali della daptomicina includono creatina chinasi elevata (CK) e rabdomiolisi, specialmente nei pazienti che assumono inibitori concomitanti della HMG-CoA reduttasi (statine)., Quindi, i livelli settimanali di CK devono essere disegnati mentre un paziente sta ricevendo daptomicina. Va anche notato che sono stati riportati casi di resistenza all’MRSA alla daptomicina, specialmente con l’uso prolungato e in pazienti con precedente esposizione alla vancomicina.26-28 La daptomicina non deve essere utilizzata per il trattamento della polmonite da MRSA perché la sua attività è inibita dai tensioattivi polmonari.
Quinupristin – dalfopristin (Synercid) è una streptogramina che ha attività contro MRSA., Anche se non approvato dalla FDA per l’uso nelle infezioni da MRSA, è usato nelle infezioni della pelle e dei tessuti molli in pazienti intolleranti o che non riescono la terapia con vancomicina. Poiché questo trattamento è stato scarsamente tollerato dai pazienti, il suo uso è limitato nella pratica clinica.29 Alcuni dei principali eventi avversi includono iperbilirubinemia, mialgie e artralgie. Sulla base di questi fattori, questo agente viene utilizzato solo come ultima opzione quando i pazienti hanno fallito o non possono tollerare altri agenti.,
Terapie più recenti
Tigeciclina (Tygacil) è il primo agente batteriostatico nella classe di antibiotici glicilciclina (un derivato sintetico della tetraciclina). È indicato per il trattamento delle infezioni complicate della struttura della pelle e della pelle (cSSSI), delle infezioni intraddominali complicate e della polmonite comunità-acquisita causata da MRSA.30 Tigeciclina non deve essere usata di routine per la batteriemia a causa di preoccupazioni sul raggiungimento di livelli sierici inadeguati., Poiché la tigeciclina è un antibiotico ad ampio spettro, il suo uso dovrebbe essere limitato a infezioni gravi e pericolose per la vita nei pazienti ospedalizzati.
Telavancin (Vibativ) è il più nuovo farmaco per essere approvato dalla FDA per il trattamento delle infezioni da MRSA.31 È un lipoglicopeptide simile alla vancomicina, sebbene il suo meccanismo d’azione differisca. La telavancina interrompe la permeabilità della membrana cellulare mediante depolarizzazione della membrana plasmatica, aumentando la permeabilità e la perdita di trifosfato adeno-sinusale cellulare e potassio (K+)., La tempistica di questi cambiamenti è correlata con una rapida perdita della vitalità batterica dipendente dalla concentrazione, suggerendo che l’attività battericida precoce della telavancina deriva dalla dissipazione del potenziale della membrana cellulare e da un aumento della permeabilità della membrana.
Studi clinici hanno dimostrato che la telavancina non è inferiore alla vancomicina nel trattamento della cSSSI.32,33 Un vantaggio che telavancin ha rispetto alla vancomicina è la somministrazione una volta al giorno e non è necessario il monitoraggio dei livelli di farmaco. Tuttavia, come la vancomicina, la dose deve essere aggiustata nei pazienti con insufficienza renale.,La funzionalità renale deve essere monitorata durante e dopo l ‘ interruzione della terapia in tutti i pazienti. La telavancina è associata al prolungamento del QTc e deve essere usata con cautela nei pazienti che assumono farmaci che potrebbero anche prolungare il QTc. Negli studi clinici di confronto tra telavancina e vancomicina, le reazioni avverse riportate in più del 10% dei pazienti trattati con telavancina hanno incluso disturbi del gusto, nausea, vomito e urina schiumosa.31 Eventi avversi gravi sono stati riportati nel 7% dei pazienti trattati con telavancina e più comunemente inclusi eventi renali, respiratori o cardiaci., Esiste un ‘avvertenza della scatola nera riguardante il rischio fetale associato all’ uso di telavancina; pertanto, le donne in età fertile devono sottoporsi ad un test di gravidanza sierico prima di iniziare l ‘ uso di telavancina.31
Ceftobiprolo (Zeftera) è la prima cefalosporina con attività battericida contro MRSA. La sua attività antibatterica include l’inibizione delle proteine leganti la penicillina coinvolte nella sintesi della parete cellulare. Negli studi clinici, è stato efficace quanto la combinazione di vancomicina e ceftazidima nel trattamento di cSSSI.,34 È generalmente ben tollerato, con i principali eventi avversi del farmaco tra cui nausea e disturbi del gusto. Ceftobiprole non è attualmente approvato per l’uso negli stati UNITI, e anche se è stato precedentemente approvato per l’uso in Canada, il produttore ha interrotto la vendita del farmaco: aprile 16, 2010.35 Questo era seguenti raccomandazioni da organismi di regolamentazione in Europa (Comitato Europeo per i Medicinali per Uso Umano) e gli stati UNITI (FDA) di non approvare il farmaco., Sebbene i risultati di fase III suggerissero il beneficio di ceftobiprolo, vi erano preoccupazioni circa l’integrità di questi risultati dello studio a causa della manomissione dei dati clinici da alcuni siti dello studio. Con questo recente sviluppo, il futuro dell’uso di ceftobiprole nel mercato statunitense rimane discutibile.
Conclusione
Con l’emergere di CA-MRSA e di MRSA etero-resistenti, è importante che i farmacisti abbiano familiarità con tutti gli agenti disponibili per la gestione delle infezioni da MRSA. È anche essenziale scegliere l’agente antimicrobico appropriato per l’infezione da trattare., Inoltre, gli agenti con uno spettro di attività più ampio (ad es. tigeciclina) devono essere riservati alle infezioni molto gravi e nel contesto di infezioni multipatogene. E ‘ anche della massima importanza per riservare i nuovi agenti per le infezioni più gravi al fine di ridurre al minimo lo sviluppo di resistenza.
1. B. Boucher HW, Corey GR. Epidemiologia dello Staphylococcus aureus meticillino-resistente. Clin Infettare Dis.
2. Styers D, Sheehan DJ, Hogan P, et al., Sorveglianza basata su laboratorio degli attuali modelli e tendenze di resistenza antimicrobica tra Staphylococcus aureus: stato 2005 negli Stati Uniti. Ann Clin Microbiol Antimicrob. 2006;5:2.
3. Chien JW, Kucia ML, Salata RA. Uso di linezolid, un oxazolidinone, nel trattamento delle infezioni batteriche gram-positive multiresistenti. Clin Infettare Dis. 2000;30:146-151.
4. Soriano A, Martinez JA, Mensa J, et al. Significato patogeno della resistenza alla meticillina per i pazienti con batteriemia da Staphylococcus aureus. Clin Infettare Dis. 2000;30:368-673.
5. Graffunder EM, Venezia RA., Fattori di rischio associati all’infezione nosocomiale da Staphylococcus aureus resistente alla meticillina (MRSA), incluso l’uso precedente di antimicrobici. J Chemother Antimicrob. 2002;49:999-1005.
6. I nostri servizi sono a vostra disposizione. Cambiamenti nell’epidemiologia dello Staphylococcus aureus resistente alla meticillina nelle unità di terapia intensiva negli ospedali statunitensi, 1992-2003. Clin Infettare Dis.
7. Levine DP, Cushing RD, Jui J, Brown WJ. Endocardite da Staphylococcus aureus resistente alla meticillina acquisita in comunità nel Detroit Medical Center. Ann Stagista Med. 1982;97:330-338.
8., Lodise TP Jr, McKinnon PS, Rybak M. Modello di previsione per identificare i pazienti con batteriemia da Staphylococcus aureus a rischio di resistenza alla meticillina. Infettare il controllo Hosp Epidemiol. 2003;24:655-661.
9. Re MD, Humphrey BJ, Wang YF, et al. Emersione del clone di Staphylococcus aureus 300 meticillino-resistente acquisito in comunità come causa predominante di infezioni della pelle e dei tessuti molli. Ann Stagista Med. 2006;144:309-317.
10. Centri per il controllo e la prevenzione delle malattie., Infezioni da Staphylococcus aureus resistenti alla meticillina tra i partecipanti sportivi competitivi-Colorado, Indiana, Pennsylvania e contea di Los Angeles, 2000-2003. MMR. 2003;52:793-795.
11. FD basso. Infezioni da Staphylococcus aureus. N Ingl J Med. 1998;339:520-532.
12. Chambers HF. La mutevole epidemiologia dello Staphylococcus aureus? Emerg Infect Dis.
13. Informazioni MRSA associate alla comunità per i medici. CDC. www.cdc.gov/ncidod/dhqp/ar_ 2008; 46 (suppl 5): S344-S349. 2006;42:389-391. 2001;7:178-182.mrsa_ca_clinicians.HTML. Accesso 4 luglio 2010.
14. Rybak MJ, LaPlante KL., Staphylococcus aureus resistente alla meticillina associato alla comunità; una recensione. Farmacoterapia. 2005;25:74-85.
15. Il sito utilizza cookie tecnici e di terze parti. Strategie per la gestione clinica dell’MRSA nella comunità: sintesi di una riunione di esperti convocata dai Centers for Disease Control and Prevention. Marzo 2006. www.cdc.gov/ncidod/dhqp/pdf/ar/CAMRSA_ExpMtgStrategies.pdf. Accesso 4 luglio 2010.
16. Sabol KE, Echevarria KL, Lewis JS II. Staphylococcus aureus resistente alla meticillina associato alla comunità: nuovo bug, vecchi farmaci. Ann Pharmacother. 2006;40:1125-1133.
17., Cleocin (clindamicina) foglietto illustrativo. New York, NY: Pfizer Inc; Novembre 2005.
18. Strom BL, Schinnar R, Apter AJ, et al. Assenza di sensibilità crociata tra antibiotici sulfonamidi e nonantibiotici sulfonamidi. N Ingl J Med. 2003;349:1628-1635.
19. I nostri servizi sono sempre a portata di mano. Minociclina contro vancomicina per il trattamento dell’endocardite sperimentale causata da Staphylococcus aureus resistente all’oxacillina. Agenti antimicrobici Chemother. 1994;38:1515-1518.
20. I nostri servizi, Aumento della resistenza agli antibiotici tra i ceppi di Staphylococcus aureus resistenti alla meticillina. Clin Infettare Dis. 2008; 46 (suppl 5): S360-S367.
21. Rybak MJ, Akins RL. Emergere di Staphylococcus aureus meticillina-resistente con glicopeptidi intermedi resistenza: significato clinico e opzioni di trattamento. Droga. 201;61:1-7.
22. Tenover FC, Moellering RC Jr. La logica per la revisione degli standard clinici e di laboratorio Institute vancomicina minima concentrazione inibitoria criteri interpretativi per Staphylococcus aureus. Clin Infettare Dis. 2007;44:1208-1215.
23., Il sito è stato pubblicato nel 2007. Aumento dell ‘ incidenza di nefrotossicità con concentrazioni minime sieriche di vancomicina più elevate. Programma e abstracts della 46th Interscience Conference on Antimicrobial Agents and Chemotherapy( ICAAC); 27-30 settembre 2006; San Francisco, CA. Estratto K789.
24. Foglietto illustrativo di Zyvox (linezolid). New York, NY: Pfizer Inc; Dicembre 2009.
25. Kuter DJ, Tillotson GS. Effetti ematologici degli antimicrobici, un focus sull’ossazolidinone, linezolid. Farmacoterapia. 201;21:1010-1013.
26. Cubicin (daptomicina) foglietto illustrativo., Lexington, MA: Cubist Pharmaceuticals; January 2010.
27. Murthy MH, Olson ME, Wickert RW, et al. Daptomycin non-susceptible methicillin-resistant Staphylococcus aureus USA 300 isolate. J Med Microbiol. 2008;57:1036-1038.
28. Mangili A, Bica I, Snydman R, Hamer DH. Daptomycin-resistant methicillin-resistant Staphylococcus aureus bacteremia. Clin Infect Dis. 2005;40:1058-1060.
29. Synercid (quinupristin-dalfopristin) package insert. Greenville, NC: Monarch Pharmaceuticals; June 2008.
30. Tygacil (tigecycline) package insert. Philadelphia, PA: Wyeth Pharmaceuticals; September 2009.,
31. Vibativ (telavancina) foglietto illustrativo. Deerfield, IL: Astellas Pharma US, Inc; Settembre 2009.
32. Stryjewski ME, Chu VH, O’Riordan WD, et al. Telavancina rispetto alla terapia standard per il trattamento di infezioni complicate della pelle e della struttura cutanea causate da batteri gram positivi: studio FAST 2. Agenti antimicrobici Chemother. 2006;50:862-867.
33. Corey GR. Studi di telavancina in cSSSI. Paper presentato a: Terzo Simposio internazionale sulle infezioni Gram-positive resistenti; 10 ottobre 2006; Niagara-on-the-Lake, Canada.
34. Vidaillac C, Rybak MJ., Ceftobiprole: first cephalosporin with activity against methicillin-resistant Staphylococcus aureus. Pharmacotherapy. 2009;29:511-525.
35. Discontinuation of the sale of ceftobiprole in Canada. Basilea Pharmaceutica. April 9, 2010. http://hugin.info/134390/R/1401931/356785.pdf. Accessed July 12, 2010.
36. Vibramycin (doxycycline) package insert. New York, NY: Pfizer Inc; April 2007.
37. Minocin (minocycline) package insert. Philadelphia, PA: Triax Pharmaceuticals; March 2006.
38. Bactrim (trimethoprim-sulfamethoxazole) package insert. Philadelphia, PA: AR Scientific; November 2006.
39., Vancocin (vancomycin) package insert. Exton, PA: ViroPharma Inc; October 2005.