SFONDO
Principio: La sintesi di aspirina da acido salicilico avviene mediante processo di acetilazione in mezzo acido. L’acido salicilico interagisce con l’anidride acetica in presenza di poche gocce di acido solforico concentrato per produrre aspirina e una molecola di acido acetico., Lo scopo dell’aggiunta di acido solforico (catalizzatore) è quello di aiutare e aumentare il processo di distacco dello acetate acetato (CH3COO–) dall’anidride acetica che alla fine viene associato allo ion H+ dal gruppo idrossi fenolico nell’acido salicilico per essere eliminato come mole di acido acetico.1
Obiettivo: Preparare l’aspirina dall’acido salicilico.,
Reazione:
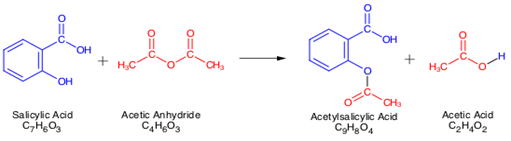
Meccanismo:
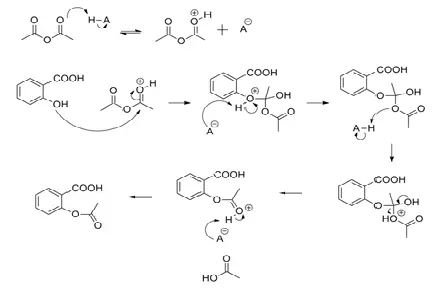
Uso:
Usato per il sollievo dei lievi dolori/fastidi e anche dolore da lieve a moderata. È raccomandato per l’artrite e le condizioni artritiche correlate, la profilassi dell’infarto miocardico. Riduce il rischio di attacchi ischemici transitori negli uomini.,
REQUIREMENTS
Chemicals: Salicylic acid – 6 g
Acetic anhydride – 8.,5 ml
Concentrated H2SO4 – 3-4 drops
Methylated spirit
Apparatus: Conical flask – 250 ml
Buchner funnel
Glass rod
Beaker
Filter paper
PROCEDURE
Weigh 6 gs of salicylic acid and transfer it to a clean and dry 250 ml conical flask. Add 8.,5 ml di anidride acetica e 3-4 gocce di acido solforico concentrato nel pallone con cura e mescolare accuratamente. Riscaldare la miscela a bagnomaria a 60 gradi circa 20 min con frequente agitazione. Lasciare raffreddare il contenuto nel pallone e versare in 100 ml di acqua fredda in un becher da 250 ml con costante agitazione. Filtrare il prodotto grezzo su un imbuto Buchner con aspirazione, lavare con acqua fredda. Ricristallizzare dall’acqua bollente insieme a piccole quantità di spirito metilato. Asciugare il prodotto sintetizzato in un forno a 90 °C e calcolare la resa.,
Calcolo
Qui il reagente limitante è l’acido salicilico; quindi la resa dovrebbe essere calcolata dalla sua quantità presa.
la formula Molecolare di acido salicilico = C7H6O3
la formula Molecolare di acido acetilsalicilico (aspirina) = C9H8O4
peso Molecolare di acido salicilico = 138 g/mole
peso Molecolare di acido acetilsalicilico (aspirina) = 180 g/mole
rendimento Teorico:
138 g di acido salicilico dà 180 g di aspirina
Perciò, 6 g di acido salicilico darà ? (X) g di aspirina
X =( 180 × 6)/138 = 7.,82 g
Resa teorica = 7,82 g
Resa pratica = —– g
% Resa = (Resa pratica)/(Resa teorica) × 100
CONCLUSIONE
L’aspirina è stata sintetizzata e la resa è risultata essere — %. (Il prodotto è ottenuto come cristalli incolori, resa 11 g e m. p. 136-137 °C.)