Reazioni di precipitazione e regole di solubilità
Una reazione di precipitazione è quella in cui le sostanze disciolte reagiscono per formare uno (o più) prodotti solidi. Molte reazioni di questo tipo comportano lo scambio di ioni tra composti ionici in soluzione acquosa e sono talvolta indicate come reazioni di doppio spostamento, doppia sostituzione o metatesi., Queste reazioni sono comuni in natura e sono responsabili della formazione di barriere coralline nelle acque oceaniche e calcoli renali negli animali. Sono ampiamente utilizzati nell’industria per la produzione di una serie di prodotti chimici per materie prime e specialità. Le reazioni di precipitazione svolgono anche un ruolo centrale in molte tecniche di analisi chimica, tra cui test spot utilizzati per identificare gli ioni metallici e metodi gravimetrici per determinare la composizione della materia (vedere l’ultimo modulo di questo capitolo).,
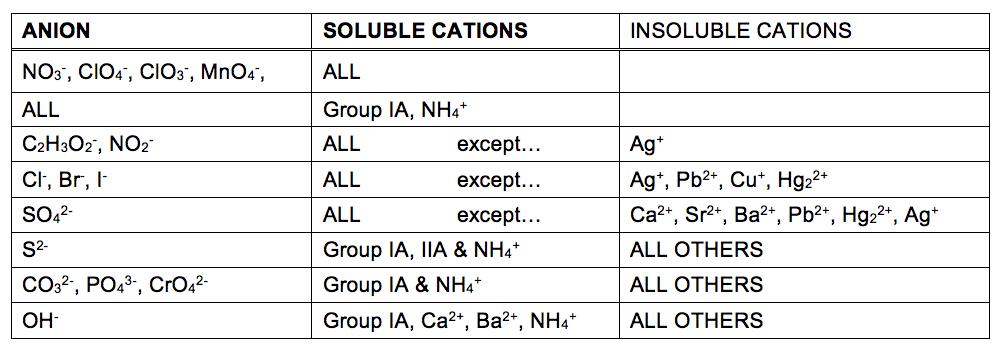
La misura in cui una sostanza può essere disciolta in acqua, o in qualsiasi solvente, è espressa quantitativamente come la sua solubilità, definita come la concentrazione massima di una sostanza che può essere raggiunta in condizioni specificate. Si dice che le sostanze con solubilità relativamente grandi siano solubili. Una sostanza precipiterà quando le condizioni della soluzione sono tali che la sua concentrazione supera la sua solubilità. Si dice che le sostanze con solubilità relativamente bassa siano insolubili e queste sono le sostanze che precipitano facilmente dalla soluzione., Maggiori informazioni su questi importanti concetti sono fornite nel capitolo testo sulle soluzioni. Ai fini della previsione delle identità dei solidi formati da reazioni di precipitazione, si può semplicemente fare riferimento a modelli di solubilità che sono stati osservati per molti composti ionici (Tabella 1).
Un esempio lampante di precipitazione osservati quando la soluzione di ioduro di potassio e nitrato di piombo sono mescolati, con conseguente formazione di un solido vantaggio ioduro di:
Questa osservazione è coerente con la solubilità linee guida: L’unico composto insolubile tra tutti coloro che sono coinvolti è ioduro di piombo, una delle eccezioni alla regola generale che la solubilità di ioduro di sali.,
ionica netta equazione che rappresenta questa reazione è:
ioduro di Piombo è un giallo brillante solido che è stato precedentemente utilizzato come un artista del pigmento noto come iodio giallo (Figura 1). Le proprietà dei cristalli puri PbI2 li rendono utili per la fabbricazione di rivelatori di raggi X e raggi gamma.

La tabella di solubilità nella Tabella 1 può essere utilizzata per prevedere se si verificherà una reazione di precipitazione quando le soluzioni di composti ionici solubili vengono mescolate insieme. Basta identificare tutti gli ioni presenti nella soluzione e quindi considerare se possibile l’accoppiamento catione/anione potrebbe portare a un composto insolubile.
Ad esempio, miscelando soluzioni di nitrato d’argento e fluoruro di sodio si ottiene una soluzione contenente ioni Ag+, NO3−, Na+ e F., A parte i due composti ionici originariamente presenti nelle soluzioni, AgNO3 e NaF, due composti ionici aggiuntivi possono essere derivati da questa raccolta di ioni: NaNO3 e AgF.
La tabella di solubilità indica che tutti i sali di nitrato sono solubili, ma che l’AgF è una delle eccezioni alla solubilità generale dei sali di fluoro. Si prevede quindi che si verifichi una reazione di precipitazione, come descritto dalle seguenti equazioni: