Introduzione
Una delle scoperte più importanti nel campo della microscopia fluorescente è stata trovata in una medusa negli anni ‘ 60. Osamu Shimomura dell’Università di Princeton stava studiando Aequorea victoria, una medusa bioluminescente., Dovrebbe benoted qui che luminescenza non è la stessa come la fluorescenza:
- Luminescenza: l’emissione spontanea di luce da parte di una sostanza (quando la sostanza è un animale, è chiamato chemiluminescenza)
- Fluorescenza: l’emissione di luce da parte di una sostanza che ha assorbito la luce e diventa eccitato
Attraverso lo studio di A. victoria, due proteine principali sono stati scoperti: l’equorina (un photoprotein), e la proteina fluorescente verde (GFP). La medusa produce calcio, che interagisce con aequorina e produce luminescenza blu., Questa luce blu viene assorbita dalla GFP e riemessa come fluorescenza verde. Queste proteine sono state isolate e purificate dalle meduse e sono utilizzate pesantemente nella ricerca fino ad oggi. Per questa ricerca, Osamu Shimomura e colleghi hanno vinto il premio Nobel per la chimica nel 2008.
Proteina fluorescente verde
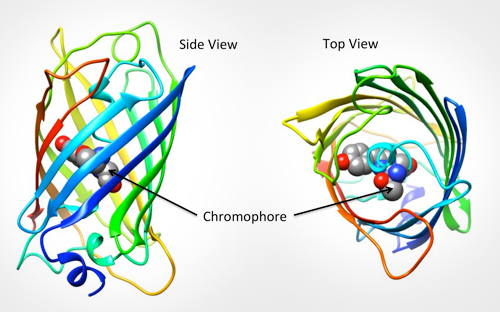
La GFP è eccitata dalla luce nella porzione blu/viola / ultravioletta dello spettro ed emette luce nella porzione verde (da cui il nome). La struttura della proteina può essere vista in Fig.1., GFP è una forma a botte con la porzione fluorescente (il cromoforo) composta da soli tre aminoacidi. Quando questo cromoforo assorbe la luce blu, emette fluorescenza verde.
GFP Nella ricerca
L’uso di GFP nella ricerca è diventato chiaro una volta che il gene per GFP è stato anche isolato e GFP potrebbe essere aggiunto alle cellule o geneticamente innestato in organismi vivi. Alcune applicazioni e vantaggi di GFP discussi di seguito.
GFP come marcatore di tossicità: a causa del fatto che GFP diminuisce l’intensità della fluorescenza con l’aumentare della tossicità, può essere utilizzato come marcatore per la tossicità ambientale., GFP può essere aggiunto agli organismi ospiti senza effetto negativo e quindi l’intensità seguita in diversi ambienti in vari organismi.
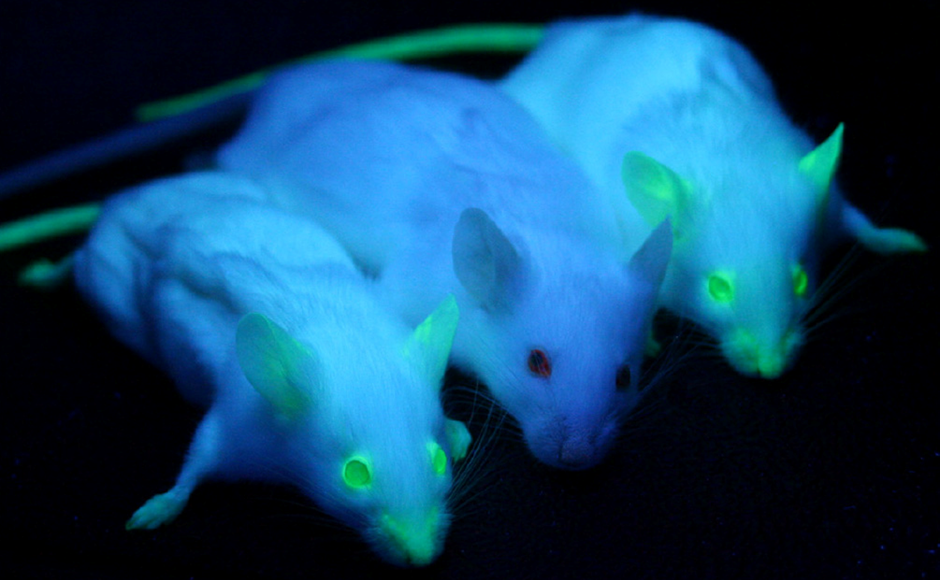
La GFP è ereditabile, se un organismo ha GFP bussato al suo genoma, la GFP sarà naturalmente trasmessa alla prole senza ulteriori processi, consentendo modi non invasivi di introdurre un marcatore fluorescente e seguirlo attraverso generazioni di animali o cellule. La GFP non interferisce con alcun processo biologico., I topi transgenici possono essere etichettati con GFP, che viene quindi facilmente osservato nella loro prole semplicemente esponendoli alla luce blu o UV, come visto in Fig.2.
GFP può essere fuso ad altre proteine, rendendo efficacemente quelle proteine fluorescenti. Questo può essere fatto con linker speciali in modo che GFP non influenzi la funzione della proteina di interesse e possa ancora diffondersi attraverso le cellule. Ciò consente a qualsiasi proteina di essere localizzata e monitorata utilizzando la microscopia fluorescente standard, brillando una luce blu sulle cellule, la proteina di interesse tornerà a fluorescenza con una luce verde.,
GFP in esperimenti con cellule vive: la classica molecola fluorescente verde è l’isotiocianato di fluoresceina (FITC), ma questo è tossico per le cellule e non può essere usato direttamente senza prima fissare le cellule o causare danni inevitabili. La GFP è molto meno dannosa in quanto è una proteina naturale e può essere utilizzata in esperimenti su cellule vive senza causare praticamente alcun danno, specialmente se viene trasmessa alla prole.
GFP nelle applicazioni avanzate di microscopia., Diverse applicazioni di microscopia a fluorescenza come il recupero della fluorescenza dopo il photobleaching (FRAP) e il trasferimento di energia di risonanza di Förster (FRET) sono state sviluppate con GFP, consentendo ai ricercatori di utilizzare applicazioni sempre più specifiche e potenti della fluorescenza per la loro imaging. Queste tecniche sono descritte in altri brevi articoli, vale a dire cos’è FRET e cos’è FRAP?
GFP è modificabile, poiché il codice genetico e aminoacidico per GFP è ben compreso che è stato soggetto a diverse modifiche., In primo luogo GFP è stato modificato per produrre GFP migliorato (eGFP), che ha aumentato l’intensità della fluorescenza, maggiore fotostabilità, picchi di eccitazione più convenienti e maggiore efficienza a temperatura ambiente. Le modifiche direttamente al cromoforo consentono a GFP di fluorescenza con colori diversi, creando blu (BFP), ciano (CFP), giallo (YFP), rosso (RFP) e altri, che sono stati migliorati separatamente e hanno le proprie applicazioni. Alcune modifiche standout includono mCherry (rosso), Citrino e Venere (giallo), e Ceruleo (ciano) per citarne alcuni., Esistono ora intere famiglie di proteine fluorescenti, tutte derivate dalla GFP originale, come si vede in Fig.3.
Sommario
La GFP è una parte fondamentale della microscopia a fluorescenza a causa della facilità d’uso e delle applicazioni limitate solo dall’immaginazione del ricercatore. I miglioramenti costanti su GFP col passare del tempo hanno indotto la microscopia e la ricerca di fluorescenza ad andare avanti, dovuto la natura altamente flessibile di GFP e del grande corpo di ricerca basato su usando GFP e le sue molte varianti.
Ulteriori letture