Obiettivi formativi
- Descrivere una molecola anticorpale.
- Disegna la struttura “stick figure” di IgG, indicando la porzione Fab (regione variabile) e la porzione Fc (regione costante).
- Dichiarare le funzioni del Fab e le porzioni Fc di un anticorpo.
- Indicare cosa si intende per attività biologica di un anticorpo.
- Confrontare la struttura di IgM e IGA secretoria con quella di IgG.
In questa sezione vedremo la struttura degli anticorpi., Esistono cinque classi o isotipi di anticorpi umani:
- immunoglobulina G (IgG),
- immunoglobulina M (IgM),
- immunoglobulina A (IgA),
- immunoglobulina D (IgD) e
- immunoglobulina E (IgE).
Gli anticorpi più semplici, come IgG, IgD e IgE, sono macromolecole a forma di “Y”chiamate monomeri. Un monomero è composto da quattro catene di glicoproteina: due catene pesanti identiche e due catene leggere identiche. Le due catene pesanti hanno un alto peso molecolare che varia con la classe di anticorpi., Le catene leggere sono disponibili in due varietà: kappa o lambda e hanno un peso molecolare inferiore rispetto alle catene pesanti. Le quattro catene glicoproteiche sono collegate tra loro da legami disolfuro (S-S) e legami non covalenti (Figura \(\PageIndex{1}\)).
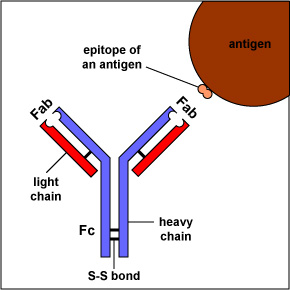
Ulteriori legami S-S piegano le singole catene glicoproteiche in un numero di domini globulari distinti (Figura \(\PageIndex{2}\)). L’area in cui la parte superiore della “Y” si unisce al fondo è chiamata cerniera. Questa zona è flessibile per consentire all’anticorpo di legarsi a coppie di epitopi diverse distanze su un antigene.
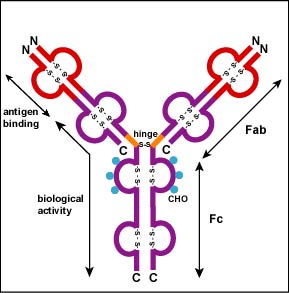
Le due punte del monomero” Y ” sono indicate come frammenti leganti l’antigene o porzioni Fab dell’anticorpo (Figure 1-3)., I primi 110 aminoacidi o primo dominio della catena pesante e leggera della regione Fab dell’anticorpo forniscono specificità per legare un epitopo su un antigene. La sequenza aminoacidica di questo primo dominio sia della catena leggera che della catena pesante mostra un’enorme variazione da anticorpo a anticorpo e costituisce la regione variabile (regione V)., Questo perché ogni linfocita B, all’inizio del suo sviluppo, diventa geneticamente programmato attraverso una serie di reazioni di splicing genico per produrre un Fab con una forma tridimensionale unica in grado di montare un epitopo con una forma corrispondente.
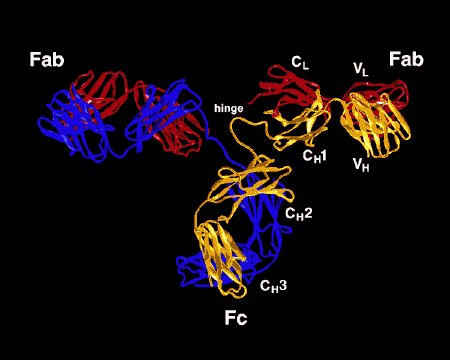
Figura \(\PageIndex{3}\): Disegno a nastro della molecola Anticorpale I2a, un disegno a nastro della prima molecola anticorpale intatta mai cristallizzata (I2a). La porzione Fab dell’anticorpo ha specificità per legare un epitopo di un antigene. La porzione Fc dirige l’attività biologica dell’anticorpo.,
I vari geni che le giunzioni cellulari insieme determinano l’ordine degli amminoacidi della porzione Fab della catena leggera e pesante; la sequenza aminoacidica determina la forma finale 3-dimensionale (Figura \(\PageIndex{4}\)). Di conseguenza, le molecole differenti dell’anticorpo prodotte dai linfociti B differenti avranno ordini differenti degli amminoacidi alle punte del Fab per dare loro le forme uniche per epitopo legante. Il sito di legame dell’antigene è abbastanza grande da contenere un epitopo di circa 5-7 aminoacidi o 3-4 residui di zucchero., Gli epitopi si legano alla porzione Fab dell’anticorpo mediante legami reversibili non covalenti.
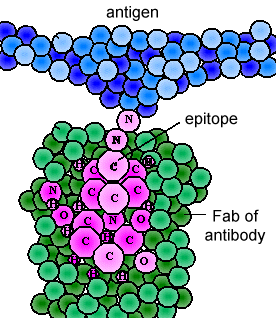
La parte inferiore della “Y”, il C regione terminale di ogni glicoproteina catena, è chiamato porzione Fc., La porzione Fc, così come un dominio della catena pesante e leggera della regione Fab ha una sequenza aminoacidica costante e viene indicata come la regione costante (regione C) dell’anticorpo e definisce la classe e la sottoclasse di ciascun anticorpo. La porzione Fc è responsabile dell’attività biologica dell’anticorpo (Figure 1-3), tuttavia, la porzione Fc diventa biologicamente attiva solo dopo che il componente Fab si è legato al suo antigene corrispondente., A seconda della classe e sottoclasse di anticorpi, attività biologica di Fc porzione di anticorpi includono la capacità di:
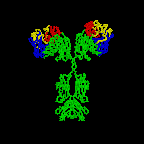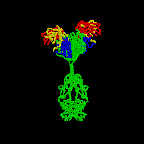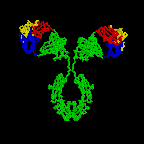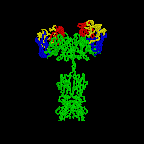
i Singoli “Y”a forma di anticorpi molecole sono dette monomeri e possibile associare due identiche epitopi. Gli anticorpi delle classi IgG, IgD e IgE sono monomeri.
Due classi di anticorpi sono più complesse., IgM (vedi Figura \(\PageIndex{10}\)) è un pentamero, costituito da 5 molecole simili a”Y “collegate alle loro porzioni Fc da una” J ” o catena di giunzione. L’IgA secretoria (vedi Figura \(\PageIndex{11}\)) è un dimero costituito da 2 molecole simili a”Y “collegate alle loro porzioni Fc da una catena” J ” e stabilizzate per resistere alla digestione enzimatica nelle secrezioni corporee per mezzo di una componente secretoria.
Sommario
- Esistono 5 classi o isotipi di anticorpi o immunoglobuline umane: IgG, IgM, IgA, IgD e IgE.,
- Gli anticorpi più semplici, come IgG, IgD e IgE, sono macromolecole a forma di “Y”chiamate monomeri e sono composti da quattro catene glicoproteiche: due catene pesanti identiche e due catene leggere identiche.
- Le due punte del monomero “Y” sono indicate come frammenti di legame dell’antigene o porzioni Fab dell’anticorpo e queste porzioni forniscono specificità per legare un epitopo su un antigene.,
- All’inizio del suo sviluppo, ogni linfocita B viene programmato geneticamente attraverso una serie di reazioni di splicing genico per produrre un Fab con una forma tridimensionale unica in grado di montare un epitopo con una forma corrispondente.
- La porzione Fc diventa biologicamente attiva solo dopo che il componente Fab si è legato al suo antigene corrispondente. Le attività biologiche includono l’attivazione dei percorsi del complemento e il legame con i recettori sui fagociti e altre cellule di difesa per promuovere l’immunità adattativa.
- IgM è un pentamero, costituito da 5 monomeri uniti alle loro porzioni Fc.,
- IgA è un dimero, costituito da 2 monomeri uniti alle loro porzioni Fc.
Domande
Studia il materiale in questa sezione e poi scrivi le risposte a queste domande. Non basta cliccare sulle risposte e scriverle. Questo non metterà alla prova la vostra comprensione di questo tutorial.
- Descrivere una molecola anticorpale. (ans)
- Corrispondono a quanto segue:
_____ La regione dell’anticorpo che fornisce specificità per legare un epitopo su un antigene., (ans)
_____ La regione dell’anticorpo responsabile dell’attività biologica dell’anticorpo. (ans)
_____ Composto da quattro catene glicoproteiche. Esistono due catene pesanti identiche ad alto peso molecolare e due catene leggere identiche. (ans)
_____ Un pentamero, costituito da 5 molecole simili a “Y”collegate alle loro porzioni Fc da una “J” o catena di giunzione. (ans)
_____ Un dimero costituito da 2 molecole simili a “Y”collegate alle loro porzioni Fc da una catena “J” e stabilizzate per resistere alla digestione enzimatica., (ans)
- IgM
- IgA secretorie
- IgG
- Fab
- Fc
- Scelta Multipla (ans)
Collaboratori e Attribuzioni
-
Dr. Gary Kaiser (università di COMUNITÀ DELLA CONTEA di BALTIMORA, CATONSVILLE CAMPUS)