US Pharm. 2010;35 (8):HS2-HS4.
a meticillin-rezisztens Staphylococcus aureus (MRSA) mind az egészségügyi ellátás, mind a közösség által szerzett fertőzések egyik vezető oka.1,2 az MRSA okozta fertőzések magas morbiditási és mortalitási kockázattal járnak, és magas egészségügyi költségekhez vezetnek.3-5 az MRSA-fertőzések előfordulása az Egyesült Államokban az elmúlt években folyamatosan nőtt az 1995-ös 22% – ról 2003-ra 60% – ra.,6 Egészségügyi ellátással összefüggő MRSA (HA-MRSA) kapcsolódó kórházakban, illetve hosszú távú ellátást, valamint gyakori a betegek hosszan tartó kórházi ápolás, elmúlt antibiotikum használat, decubitus, fekélyek, dialízis, beültetett katéter, enterális etetők, vagy történelem IV kábítószerrel való visszaélés.7,8 az elmúlt években azonban nőtt az MRSA egy új törzse, a közösségi vonatkozású MRSA (CA-MRSA)., Úgy tűnik, hogy ezt a járóbeteg-ellátásban szerezték be, és az átvitel szoros fizikai kapcsolaton keresztül történik, mint például a napköziben, az indiai fenntartásokban, a korrekciós létesítményekben, valamint a sportolók, a katonai személyzet és a férfiakkal szexuális férfiak körében.7,9,10
megkülönböztető MRSA törzsek
Több jelentés is különbséget tárt fel a HA-MRSA és a CA-MRSA törzsek között, beleértve a két törzs különböző genotípusainak jelenlétét. A CA-MRSA számos nem béta-laktám antibiotikumra érzékeny, míg a HA-MRSA törzsek nem., A CA-MRSA törzsek nagyobb valószínűséggel kódolnak bizonyos virulens tényezőket, amelyek súlyos tüdőgyulladással (különösen gyermekeknél), valamint felnőttek bőr-és lágyszöveti fertőzéseivel kapcsolatosak.8,11,12 a CDC meghatározta a CA-MRSA és a HA-MRSA megkülönböztetésének kritériumait. Ezek az iránymutatások magukban foglalják a pozitív MRSA-kultúra izolálását a beteg kórházba való belépésétől számított 48 órán belül. Figyelembe kell venni a CA-MRSA, a beteg nem rendelkezik az alábbi: legutóbbi kórházi; felvételi egy idősek otthonában, hospice, vagy képzett ápolási létesítmény; dialízis; vagy legutóbbi műtét., A betegnek nem lehetnek bentlakásos katéterei vagy más orvostechnikai eszközei.13
Kezel CA-MRSA
A CDC azt javasolja, hogy a menedzsment, illetve megelőzése, a járványok, a CA-MRSA tartalmaznia, amely a fertőzések, hogy a termék genny, megmosta a kezét, gyakran nem megosztási személyes tárgyak, mosás szennyes ágynemű, ruházat forró vízzel, majd szárítás ruha, a forró hajszárító képest levegő szárítás.13 a bőr tályogok esetében a kezelés magában foglalja a tályogok bemetszését és elvezetését szisztémás antibiotikumokkal vagy anélkül, a fertőzés súlyosságától függően.,14
a CA-MRSA kezelése általában olyan szerek alkalmazását foglalja magában, mint a klindamicin, a tetraciklinek és a trimetoprim-szulfametoxazol (TMP-SMX). A rifampin antibiotikumot soha nem szabad monoterápiaként alkalmazni az MRSA kezelésére. A rezisztencia gyorsan fejlődik a rifampin monoterápiával; azonban, ha egy másik anti-MRSA szerrel kombinálva alkalmazzák, hatékonyabban képes felszámolni a szervezeteket a hordozó helyekről.15 a fent említett antibiotikumok általában életképes kezelési lehetőségek járóbeteg-alapon kezelt betegeknél., A kórházi kezelést igénylő súlyos fertőzések esetén az IV antibiotikumok, köztük a vankomicin, a linezolid, a quinupristin-dalfopristin, a daptomicin, a tigeciklin és a telavancin megfelelő terápiák (1.táblázat).
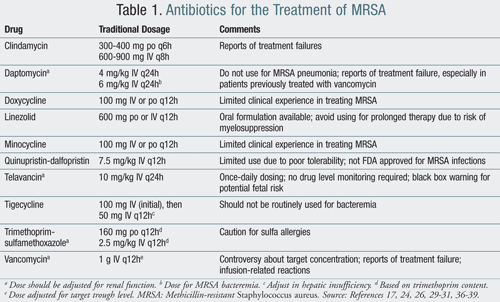
bár a klindamicin (Kleocin) alkalmazható CA-MRSA-ra, a rezisztenciáról azt jelentették, hogy a vele kezelt betegeknél legfeljebb 19%. Így a klindamicinnel kezelt betegeket szorosabban ellenőrizni kell az önindukált rezisztencia kialakulása szempontjából.,16 a klindamicin összefüggésbe hozható a Clostridium difficile fertőzések kialakulásával is, ami hosszabb ideig korlátozza annak alkalmazását.17
tmp-SMX (Bactrim) a vankomicin-kezelés alternatívájának tekinthető bizonyos MRSA-fertőzések esetén. A klindamicinhez hasonlóan azonban beszámoltak a kezelés sikertelenségéről. Ez a terápia korlátozott mértékben alkalmazható a szulfonamid allergiák magas előfordulási gyakorisága miatt is, amelyek a népesség legfeljebb 10% – ánál fordultak elő.,18
a minociklin (Minocin) és a doxiciklin (Vibramicin) tetraciklin antibiotikumok, amelyeket MRSA kezelésére alkalmaztak. Ezeknek az ágenseknek csak korlátozott mennyiségű adat áll rendelkezésre az MRSA-ban történő alkalmazásra vonatkozóan, de klinikai sikerről számoltak be.19
HA-MRSA
parenterális antibiotikumok kezelése a ha-MRSA kezelésének arany standardja. Több évtizede széles körben használják a vankomicin glikopeptid antibiotikumot.
A vankomicin (Vankocin) gátolja a sejtfal szintézisét; in vitro azonban lassabb baktericid hatással rendelkezik., A túlzott használata miatt beszámoltak a csökkent érzékenységről és a vankomicin heterorezisztencia kialakulásáról S aureus-ban.20,21 a >2 mcg/mL minimális gátló koncentrációjú s aureus szubpopulációjának (MIC) növekedése a vankomicinhez (továbbiakban: Mic creep) mind mikrobiológiai, mind klinikai kudarchoz kapcsolódik. A nemzeti klinikai laboratóriumi szabványok Bizottsága (NCCLS) új töréspontokat javasolt a vankomicin számára—a MIC “érzékeny” értéke ≤4 mcg/mL-ről ≤2 mcg/mL-re változik.,22 A javaslat indoklása részben anekdotikus klinikai megfigyeléseken alapul, amelyek a vankomicin standard dózisaival történő kezelés során fellépő kezelési kudarcokról szólnak 4 mcg/mL-es MIC-ben szenvedő betegeknél. Ezen túlmenően súlyos fertőzések, például tüdőgyulladás és osteomyelitis esetén a vankomicin gyenge szöveti penetrációja miatt magasabb vályúszintre (azaz 15-20 mcg/mL-es vályúszintre) lehet szükség. Volt néhány anekdotikus jelentés a lehetséges nephrotoxicitásról ezekkel a magas vályúszintekkel kapcsolatban.,
Jeffres et al az antimikrobiális szerekről és a kemoterápiáról (ICAAC) szóló 2006-os Interscience konferencián absztrakt képet mutatott be, amely a magasabb vankomicin-vályúszint mellett vizsgálta a nephrotoxicitás kockázatát.23 A tanulmány számolt be 30% kockázat, a vesekárosító (meghatározott növekedése 0,5 mg/dL vagy 50% – kal növeli a szérum kreatinin-szint a kiindulási értékhez) a betegek vankomicin minimális szinten 315 mcg/mL képest 13% – os, a betegek minimális szint <15 mcg/mL.23 egyes betegpopulációkban nagyobb a vankomicin által indukált nephrotoxicitás kialakulásának kockázata., Ezek közé tartoznak az ismert kockázati tényezők, mint például az idősebb életkor, kritikusan beteg, alacsonyabb vesefunkciójú, valamint más nephrotoxikus szerek, például aminoglikozidok egyidejű alkalmazása. Mindezek a tényezők az újabb ügynökök szükségességének és használatának növekedéséhez vezettek.
a Linezolid (Zyvox) az első oxazolidinon, amelyet az MRSA által okozott bőr-és lágyszöveti fertőzések, bacter-emia, valamint közösségi és nosocomiális pneumonia kezelésére hagytak jóvá.24 gátolja a fehérjeszintézis megindítását az 50-es riboszómában; azonban, ellentétben a legtöbb más gyógyszerrel, bakteriosztatikus szer., Használatának előnyei közé tartozik egy olyan orális készítmény rendelkezésre állása, amely kiváló biohasznosulási tulajdonságokkal rendelkezik, veseelégtelenségben szenvedő betegeknél, beleértve a veseelégtelenségben szenvedő betegeket is, dózismódosítás nélkül. Az alkalmazás egyik korlátozó tényezője, különösen a terápia hosszabb időtartamára, a myelosuppressio azoknál a betegeknél, akik több mint 14 napig linezolidot kaptak.24,25 bár orális készítményként kapható, költségének köszönhetően nem használják annyira a járóbeteg-környezetben., Számos biztosítási kötvény nem vonatkozik rá, így a betegeknek esetleg a gyártó betegsegítő programjait kell használniuk.
a daptomicin (Cubicin), egy gyors baktericid hatású lipopeptid antibiotikum, bonyolult bőr-és lágyszöveti fertőzések, valamint az MRSA által okozott bakterémia kezelésére engedélyezett.26 hatásmechanizmusa magában foglalja a bakteriális sejtfal depolarizációját. A daptomicin mellékhatásai közé tartozik az emelkedett kreatin-kináz (CK) és a rhabdomyolysis, különösen olyan betegeknél, akik egyidejűleg HMG-CoA reduktáz gátlókat (sztatinokat) szednek., Ezért a beteg daptomicint kapásakor heti CK-szintet kell levonni. Azt is meg kell jegyezni, hogy jelentettek MRSA-rezisztenciát a daptomicinnel szemben, különösen hosszan tartó alkalmazás esetén, valamint olyan betegeknél, akiknél korábban vankomicint kaptak.26-28 A Daptomicint nem szabad MRSA tüdőgyulladás kezelésére alkalmazni, mivel aktivitását pulmonalis felületaktív anyagok gátolják.
A Quinupristin-dalfopristin (Synercid) egy streptogramin, amely aktivitást mutat az MRSA ellen., Bár az FDA nem hagyta jóvá az MRSA-fertőzésekben való alkalmazásra, bőr-és lágyszöveti fertőzésekben alkalmazzák olyan betegeknél, akik nem tolerálják vagy elmulasztják a vankomicin-terápiát. Mivel ezt a kezelést a betegek rosszul tolerálták, alkalmazása a klinikai gyakorlatban korlátozott.29 A főbb mellékhatások közé tartozik a hyperbilirubinaemia, a myalgiák és az arthralgiák. Ezen tényezők alapján ezt az anyagot csak utolsó lehetőségként használják, ha a betegek kudarcot vallottak, vagy nem tolerálják más szereket.,
újabb terápiák
a tigeciklin (Tygacil) az első bakteriosztatikus szer az antibiotikumok glicilciklin osztályában (a tetraciklin szintetikus származéka). A készítmény bonyolult bőr-és bőrszerkezeti fertőzések (cSSSI), komplikált intraabdominalis fertőzések, valamint az MRSA által okozott, közösségben szerzett pneumonia kezelésére javallt.30 a tigeciklint nem szabad rutinszerűen bakterémiára alkalmazni a nem megfelelő szérumszintek elérésével kapcsolatos aggodalmak miatt., Mivel a tigeciklin széles spektrumú antibiotikum, alkalmazását kórházi betegek súlyos és életveszélyes fertőzéseire kell korlátozni.
a Telavancin (Vibativ) a legújabb gyógyszer, amelyet az FDA jóváhagyott az MRSA fertőzések kezelésére.31 ez a vankomicinhez hasonló lipoglikopeptid, bár hatásmechanizmusa különbözik. A Telavancin a plazmamembrán depolarizációjával megzavarja a sejtmembrán permeabilitását, növeli a sejt adeno-szinusz trifoszfát és kálium (k+) permeabilitását és szivárgását., Ezeknek a változásoknak az időzítése korrelál a bakteriális életképesség gyors, koncentrációfüggő elvesztésével, ami arra utal, hogy a telavancin korai baktericid aktivitása a sejtmembrán potenciál disszipációjából és a membrán permeabilitásának növekedéséből ered.
klinikai vizsgálatok kimutatták, hogy a telavancin nem rosszabb a vankomicinnél a cSSSI kezelésében.32,33 a telavancin egyik előnye a vankomicinnel szemben a napi egyszeri adagolás, és nincs szükség a gyógyszerszintek ellenőrzésére. Azonban, mint a vankomicin, az adagot veseelégtelenségben szenvedő betegeknél módosítani kell.,31 a vesefunkciót minden betegnél monitorozni kell a kezelés alatt és után. A Telavancin a QTc megnyúlásával jár, és óvatosan kell alkalmazni azoknál a betegeknél, akik olyan gyógyszereket szednek, amelyek szintén meghosszabbíthatják a QTc-t. A klinikai vizsgálatok összehasonlítása telavancin a vankomicin, mellékhatások, több, mint 10% – val kezelt betegek telavancin tartalmazza ízérzési zavarok, hányinger, hányás, habos vizelet.31 súlyos mellékhatást jelentettek a telavancin-nal kezelt betegek 7% – ánál, és leggyakrabban vese -, légzőszervi vagy szívbetegségeket jelentettek., Van egy fekete doboz figyelmeztetés vonatkozó magzati kockázatok telavancin használja; így a szülőképes korú kell szérum terhességi teszt megkezdése előtt telavancin.31
A Ceftobiprole (Zeftera) az első cefalosporin, amely baktericid hatással rendelkezik az MRSA ellen. Antibakteriális aktivitása magában foglalja a sejtfal szintézisében részt vevő penicillinkötő fehérjék gátlását. A klinikai vizsgálatokban ugyanolyan hatékony volt, mint a vankomicin és a ceftazidim kombinációja a cSSSI kezelésében.,34 Ez általában jól tolerálható, a fő mellékhatások a gyógyszer, beleértve a hányinger és íz zavarok. A Ceftobiprole-t jelenleg nem engedélyezték az Egyesült Államokban történő felhasználásra, és bár korábban Kanadában engedélyezték, a gyártó 2010.április 16-tól abbahagyta a gyógyszer értékesítését. 35 Ez az európai szabályozó testületek (európai emberi felhasználásra szánt gyógyszerek bizottsága) és az Egyesült Államok (FDA) ajánlásait követte, hogy ne hagyja jóvá a gyógyszert., Bár a III. fázisú eredmények a ceftobiprol előnyére utaltak, aggályok merültek fel ezen vizsgálati eredmények integritásával kapcsolatban, mivel a vizsgálati helyek egy részéből származó klinikai adatokat manipulálták. Ezzel a közelmúltbeli fejlődéssel a ceftobiprole használatának jövője az amerikai piacon továbbra is megkérdőjelezhető.
következtetés
a CA-MRSA, valamint a hetero-rezisztens MRSA megjelenésével fontos, hogy a gyógyszerészek ismerjék az MRSA-fertőzések kezelésére rendelkezésre álló összes hatóanyagot. Fontos továbbá a megfelelő antimikrobiális szer kiválasztása a kezelendő fertőzéshez., Ezenkívül a tágabb aktivitású (pl. tigeciklin) szereket nagyon súlyos fertőzésekre és multipatogén fertőzések kialakulására kell fenntartani. Rendkívül fontos, hogy az újabb szereket súlyosabb fertőzésekre fenntartsák a rezisztencia kialakulásának minimalizálása érdekében.
1. Boucher HW, Corey GR. A meticillin-rezisztens Staphylococcus aureus epidemiológiája. Clinic Dis.
2. Styers D, Sheehan DJ, Hogan P, et al., A jelenlegi antimikrobiális rezisztencia minták és tendenciák laboratóriumi alapú megfigyelése a Staphylococcus aureus között: 2005 státusz az Egyesült Államokban. Ann Clin Mikrobiol Antimicrob. 2006;5:2.
3. Csien JW, Kucia ML, Salata RA. Linezolid, oxazolidinon alkalmazása multirezisztens Gram-pozitív bakteriális fertőzések kezelésében. Clinic Dis. 2000;30:146-151.
4. Soriano A, Martinez JA, Mensa J, et al. A meticillin rezisztencia patogén jelentősége a Staphylococcus aureus bacteremiában szenvedő betegeknél. Clinic Dis. 2000;30:368-673.
5. Graffunder EM, Venezia RA., A nozokomiális meticillin-rezisztens Staphylococcus aureus (MRSA) fertőzéssel kapcsolatos kockázati tényezők, beleértve az antimikrobiális szerek korábbi alkalmazását is. J Antimikrob Chemother. 2002;49:999-1005.
6. Klevens RM, Edwards JR, Tenover FC, et al. A meticillin-rezisztens Staphylococcus aureus epidemiológiájának változásai az amerikai kórházak intenzív osztályain, 1992-2003. Clinic Dis.
7. Levine DP, Cushing RD, Jui J, Brown WJ. Közösség által szerzett meticillin-rezisztens Staphylococcus aureus endocarditis a detroiti Orvosi Központban. Ann Gyakornok Orvos. 1982;97:330-338.
8., Lodise TP Jr, McKinnon PS, Rybak M. predikciós modell a meticillin-rezisztencia kockázatának kitett Staphylococcus aureus bacteraemiában szenvedő betegek azonosítására. Fertőz Ellenőrzés Hosp Epidemiol. 2003;24:655-661.
9. Király MD, Humphrey BJ, Wang YF, et al. A közösségben szerzett meticillin-rezisztens Staphylococcus aureus USA 300 klón megjelenése a bőr-és lágyszöveti fertőzések legfőbb oka. Ann Gyakornok Orvos. 2006;144:309-317.
10. Betegségek elleni és Megelőzési Központok., Meticillin-rezisztens Staphylococcus aureus fertőzések között versenyképes sport résztvevők-Colorado, Indiana, Pennsylvania, and Los Angeles County, 2000-2003. MMWR. 2003;52:793-795.
11. Lowy FD. Staphylococcus aureus fertőzések. N Engl J Med. 1998;339:520-532.
12. Chambers HF. A Staphylococcus aureus változó epidemiológiája? Emerg Dis.
13. Közösségi kapcsolódó MRSA információk klinikusok számára. CDC. www.cdc.gov/ncidod/dhqp/ar_ 2008;46 (suppl 5): S344-S349. 2006;42:389-391. 2001;7:178-182.mrsa_ca_clinicians.html. Hozzáférés 2010.Július 4-Én.
14. Rybak MJ, LaPlante KL., Közösséghez kapcsolódó meticillin-rezisztens Staphylococcus aureus; felülvizsgálat. Farmakoterápia. 2005;25:74-85.
15. Gorwitz RJ, Jernigan DB, Powers JH, et al. Az MRSA klinikai kezelésének stratégiái a közösségben: a Betegségvédelmi és Megelőzési Központok által összehívott szakértői találkozó összefoglalása. 2006. március. www.cdc.gov/ncidod/dhqp/pdf/ar/CAMRSA_ExpMtgStrategies.pdf.hozzáférés 2010. július 4-én.
16. Sabol KE, Echevarria KL, Lewis js II. közösséghez kapcsolódó meticillin-rezisztens Staphylococcus aureus: új hiba, régi gyógyszerek. Ann Pharmacother. 2006;40:1125-1133.
17., Kleocin (klindamicin)csomag betét. New York, NY: Pfizer Inc; November 2005.
18. Strom BL, Schinnar R, Apter AJ, et al. A szulfonamid antibiotikumok és a szulfonamid nemantibiotikumok közötti keresztérzékenység hiánya. N Engl J Med. 2003;349:1628-1635.
19. Nicolau DP, Freeman CD, Nightingale CH, et al. Minociklin versus vankomicin kezelésére kísérleti endocarditis okozta oxacillin-rezisztens Staphylococcus aureus. Antimikrob Szerek Chemother. 1994;38:1515-1518.
20. Sakoulas G., Moellering RC Jr., Növekvő antibiotikum-rezisztencia a meticillin-rezisztens Staphylococcus aureus törzsek között. Clinic Dis. 2008;46 (suppl 5): S360-S367.
21. Rybak MJ, Akins RL. Meticillin-rezisztens Staphylococcus aureus kialakulása közbenső glikopeptidek rezisztenciával: klinikai jelentősége és kezelési lehetőségei. Drogok. 201;61:1-7.
22. Tenover FC, Moellering RC Jr. a vankomicin klinikai és laboratóriumi Standard Intézet felülvizsgálatának indoka minimális gátló koncentráció értelmező kritériumok a Staphylococcus aureus esetében. Clinic Dis. 2007;44:1208-1215.
23., Jeffres MN, Micek ST, Isakow W, et al. A nephrotoxicitás gyakoribb előfordulása magasabb vankomicin szérumszinttel. Az antimikrobiális szerekről és kemoterápiáról szóló 46. Interscience konferencia programja és összefoglalói (ICAAC); 2006. szeptember 27-30.; San Francisco, kb. Absztrakt K789.
24. Zyvox (linezolid) csomagolás beszúrása. New York, NY: Pfizer Inc; December 2009.
25. Kuter DJ, Tillotson GS. Az antimikrobiális szerek hematológiai hatásai, az oxazolidinonra, a linezolidra összpontosítva. Farmakoterápia. 201;21:1010-1013.
26. Cubicin (daptomicin) betegtájékoztató., Lexington, MA: Cubist Pharmaceuticals; January 2010.
27. Murthy MH, Olson ME, Wickert RW, et al. Daptomycin non-susceptible methicillin-resistant Staphylococcus aureus USA 300 isolate. J Med Microbiol. 2008;57:1036-1038.
28. Mangili A, Bica I, Snydman R, Hamer DH. Daptomycin-resistant methicillin-resistant Staphylococcus aureus bacteremia. Clin Infect Dis. 2005;40:1058-1060.
29. Synercid (quinupristin-dalfopristin) package insert. Greenville, NC: Monarch Pharmaceuticals; June 2008.
30. Tygacil (tigecycline) package insert. Philadelphia, PA: Wyeth Pharmaceuticals; September 2009.,
31. Vibativ (telavancin) használati utasítás. Deerfield, IL: Astellas Pharma US, Inc; szeptember 2009.
32. Stryjewski ME, Chu VH, O ‘ Riordan WD, et al. Telavancin versus standard therapy for the treatory of complicated skin and skin structure infections caused by Gram pozitív baktériumok: FAST 2 study. Antimikrob Szerek Chemother. 2006;50:862-867.
33. Corey GR. Tanulmányok a telavancin a cSSSI. Papír bemutatott: harmadik Nemzetközi szimpózium rezisztens Gram-pozitív fertőzések; október 10, 2006; Niagara-on-the-Lake, Kanada.
34. Vidaillac C, Rybak MJ., Ceftobiprole: first cephalosporin with activity against methicillin-resistant Staphylococcus aureus. Pharmacotherapy. 2009;29:511-525.
35. Discontinuation of the sale of ceftobiprole in Canada. Basilea Pharmaceutica. April 9, 2010. http://hugin.info/134390/R/1401931/356785.pdf. Accessed July 12, 2010.
36. Vibramycin (doxycycline) package insert. New York, NY: Pfizer Inc; April 2007.
37. Minocin (minocycline) package insert. Philadelphia, PA: Triax Pharmaceuticals; March 2006.
38. Bactrim (trimethoprim-sulfamethoxazole) package insert. Philadelphia, PA: AR Scientific; November 2006.
39., Vancocin (vancomycin) package insert. Exton, PA: ViroPharma Inc; October 2005.