US Pharm. 2010; 35(8):HS2-HS4.
Staphylococcus aureus résistant à la méthicilline (SARM) est l’une des principales causes d’infections nosocomiales et communautaires.1,2 Les infections dues au SARM sont associées à un risque élevé de morbidité et de mortalité et entraînent des coûts de soins de santé élevés.3-5 L’incidence des infections à SARM aux États-Unis a augmenté régulièrement au cours des dernières années, passant de 22% en 1995 à 60% en 2003.,6 Le SARM associé aux soins de santé (SARM–HA) est lié aux hôpitaux et aux établissements de soins de longue durée et est fréquent chez les patients ayant une hospitalisation prolongée, une utilisation antérieure d’antimicrobiens, des ulcères de décubitus, une dialyse, des cathéters à demeure, des tétées entérales ou des antécédents d’abus de drogues intraveineuses.7,8 Au cours des dernières années, cependant, une nouvelle souche de SARM appelée SARM associé à la communauté (SARM-CA) a augmenté., Cela semble être acquis en ambulatoire, et la transmission se fait par contact physique étroit, comme dans les garderies, les réserves indiennes et les établissements correctionnels, ainsi que parmi les athlètes, le personnel militaire et les hommes ayant des relations sexuelles avec des hommes.7,9,10
Distinguer les souches de SARM
Plusieurs rapports ont révélé des différences entre les souches HA-SARM et CA-SARM, y compris la présence de génotypes différents entre les deux souches. Le SARM-CA est sensible à plusieurs antibiotiques non bêta-lactamines, alors que les souches de SARM-HA ne le sont pas., Les souches de CA-SARM sont plus susceptibles de coder certains facteurs virulents qui ont été associés à une pneumonie sévère (en particulier chez les enfants) et à des infections de la peau et des tissus mous chez les adultes.8,11,12 Le CDC a établi les critères permettant de différencier le SARM-CA du SARM-HA. Ces lignes directrices comprennent l’isolement d’une culture positive de SARM dans les 48 heures suivant l’admission d’un patient à l’hôpital. Pour être considéré comme CA-SARM, le patient ne doit pas avoir l’un des éléments suivants: hospitalisation récente; admission dans une maison de soins infirmiers, un hospice ou un établissement de soins infirmiers qualifié; dialyse; ou chirurgie récente., Le patient ne doit pas non plus avoir de cathéters à demeure ou d’autres dispositifs médicaux.13
Traitement du SARM-CA
Le CDC recommande que la gestion et la prévention des éclosions de SARM-CA comprennent la couverture des infections qui produisent du pus, le lavage fréquent des mains, le non-partage d’objets personnels, le lavage du linge et des vêtements souillés à l’eau chaude et le séchage des chiffons dans13 Pour les abcès cutanés, le traitement comprend l’incision et le drainage des abcès avec ou sans antibiotiques systémiques, en fonction de la gravité de l’infection.,14
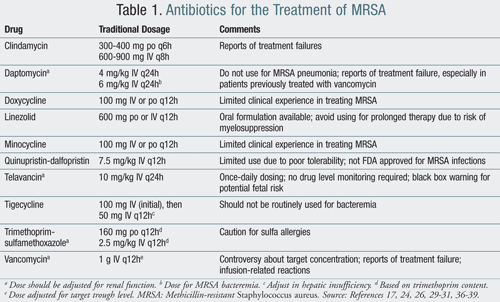
Le traitement du SARM-CA comprend généralement l’utilisation d’agents tels que la clindamycine, les tétracyclines et le triméthoprime-sulfaméthoxazole (TMP-SMX). L’antibiotique rifampine ne doit jamais être utilisé en monothérapie pour la prise en charge du SARM. La résistance se développe rapidement avec la rifampine en monothérapie; cependant, lorsqu’elle est utilisée en association avec un autre agent anti-SARM, elle peut éradiquer plus efficacement les organismes des sites porteurs.15 Les antibiotiques susmentionnés sont généralement des options de traitement viables chez les patients traités en ambulatoire., Dans les infections graves nécessitant une hospitalisation, les antibiotiques IV, notamment la vancomycine, le linézolide, la quinupristine-dalfopristine, la daptomycine, la tigécycline et la télavancine, sont des traitements appropriés qui peuvent être utilisés (TABLEAU 1).
Bien que la clindamycine (Cléocine) puisse être utilisée pour le SARM-CA, la résistance a été rapportée jusqu’à 19% chez les patients traités avec elle. Ainsi, les patients traités par la clindamycine doivent être surveillés de plus près pour le développement d’une résistance auto-induite.,16 La clindamycine a également été associée au développement d’infections à Clostridium difficile, limitant son utilisation sur une période prolongée.17
Le TMP-SMX (Bactrim) peut être considéré comme une alternative au traitement par la vancomycine dans certains cas d’infections à SARM. Cependant, comme avec la clindamycine, il y a eu des rapports d’échecs de traitement. Cette thérapie a également une utilisation limitée en raison de la forte incidence des allergies aux sulfonamides, qui ont été signalées chez jusqu’à 10% de la population.,18
La minocycline (Minocine) et la doxycycline (vibramycine) sont des antibiotiques tétracyclines utilisés dans le traitement du SARM. Ces agents ne disposent que de données limitées sur leur utilisation dans le SARM, mais leur succès clinique a été signalé.19
Traitement du SARM-HA
Les antibiotiques parentéraux sont considérés comme l’étalon-or pour le traitement du SARM-HA. Depuis plusieurs décennies, l’antibiotique glycopeptidique vancomycine est largement utilisé.
La vancomycine (vancocine) inhibe la synthèse de la paroi cellulaire; cependant, elle a une activité bactéricide plus lente in vitro., Avec sa surutilisation, il y a eu des rapports de susceptibilités réduites et l’émergence de l’hétérorésistance de vancomycine dans S aureus.20,21 L’augmentation d’une sous-population de S aureus avec une concentration inhibitrice minimale (CMI) de >2 mcg/mL en vancomycine (appelée fluage CMI) est associée à l’échec microbiologique et clinique. Le National Committee for Clinical Laboratory Standards (NCCLS) a proposé de nouveaux points d’arrêt pour la vancomycine—en changeant la CMI pour « sensible” de ≤4 mcg/mL à ≤2 mcg/mL.,22 La justification de cette proposition repose en partie sur des observations cliniques anecdotiques d’échecs de traitement pendant le traitement avec des doses standard de vancomycine chez des patients ayant une CMI de 4 mcg/mL. En outre, des niveaux creux plus élevés (c.-à-d. des niveaux creux de 15-20 mcg/mL) peuvent être nécessaires pour des infections graves comme la pneumonie et l’ostéomyélite dues à une mauvaise pénétration des tissus par la vancomycine. Il y a eu quelques rapports anecdotiques de néphrotoxicité possible associée à ces niveaux creux élevés.,
Jeffres et al ont présenté un résumé à la Conférence Interscience sur les agents antimicrobiens et la chimiothérapie (ICAAC) de 2006 qui a examiné le risque de néphrotoxicité avec des niveaux creux de vancomycine plus élevés.23 Dans leur étude, ils ont signalé un risque de néphrotoxicité de 30% (défini comme une augmentation de 0,5 mg/dL ou une augmentation de 50% de la créatinine sérique par rapport à l’inclusion) chez les patients présentant des concentrations minimales de vancomycine de 315 mcg/mL comparativement à 13% chez les patients présentant des concentrations minimales <15 mcg/mL.23 Certaines populations de patients courent un risque plus élevé de développer une néphro-toxicité induite par la vancomycine., Ceux-ci comprennent des facteurs de risque connus tels que l’âge avancé, être gravement malade, avoir une fonction rénale inférieure et l’utilisation concomitante d’autres agents néphrotoxiques comme les aminoglycosides. Tous ces facteurs ont conduit à une augmentation du besoin et de l’utilisation des nouveaux agents.
Le linézolide (Zyvox) est le premier oxazolidinone approuvé pour le traitement des infections de la peau et des tissus mous, des infections bactériennes et des pneumonies communautaires et nosocomiales causées par le SARM.24 Il inhibe l’initiation de la synthèse des protéines au niveau du ribosome des années 50; cependant, contrairement à la plupart des autres médicaments, il s’agit d’un agent bactériostatique., Les avantages de son utilisation incluent la disponibilité d’une formulation orale qui a d’excellentes propriétés de biodisponibilité, sans ajustement posologique justifié chez les patients atteints d’insuffisance rénale, y compris ceux recevant des thérapies de remplacement rénal. Un facteur limitant son utilisation, en particulier pour la durée prolongée du traitement, est la myélosuppression chez les patients qui ont reçu du linézolide pendant plus de 14 jours.24,25 Bien que disponible sous forme orale, il n’est pas utilisé autant en ambulatoire en raison de son coût., Il n’est pas non plus couvert par de nombreuses polices d’assurance, de sorte que les patients peuvent avoir besoin d’utiliser les programmes d’aide aux patients du fabricant.
La daptomycine (Cubicine), un antibiotique lipopeptidique à activité bactéricide rapide, est approuvée pour le traitement des infections compliquées de la peau et des tissus mous, ainsi que des bactériémies causées par le SARM.26 Son mécanisme d’action implique la dépolarisation de la paroi cellulaire bactérienne. Les effets secondaires de la daptomycine comprennent une augmentation de la créatine kinase (CK) et de la rhabdomyolyse, en particulier chez les patients prenant simultanément des inhibiteurs de la HMG-CoA réductase (statines)., Par conséquent, les niveaux hebdomadaires de CK doivent être établis pendant qu’un patient reçoit de la daptomycine. Il convient également de noter que des cas de résistance au SARM à la daptomycine ont été signalés, en particulier lors d’une utilisation prolongée et chez des patients ayant déjà été exposés à la vancomycine.26-28 La daptomycine ne doit pas être utilisée pour le traitement de la pneumonie à SARM car son activité est inhibée par les tensioactifs pulmonaires.
Quinupristine-dalfopristine (Synercid) est un streptogramine qui a une activité contre le SARM., Bien que non approuvé par la FDA pour une utilisation dans les infections à SARM, il est utilisé dans les infections de la peau et des tissus mous chez les patients qui sont intolérants au traitement à la vancomycine ou qui échouent. Parce que ce traitement a été mal toléré par les patients, son utilisation est limitée dans la pratique clinique.29 Parmi les principaux événements indésirables, on compte l’hyperbilirubinémie, les myalgies et les arthralgies. Sur la base de ces facteurs, cet agent n’est utilisé qu’en dernière option lorsque les patients ont échoué ou ne peuvent pas tolérer d’autres agents.,
Nouvelles thérapies
La tigécycline (Tygacil) est le premier agent bactériostatique de la classe des antibiotiques glycylcycline (un dérivé synthétique de la tétracycline). Il est indiqué pour le traitement des infections compliquées de la peau et de la structure de la peau (cSSSI), des infections intra-abdominales compliquées et des pneumonies communautaires causées par le SARM.30 La tigécycline ne doit pas être systématiquement utilisée pour la bactériémie en raison de préoccupations concernant l’atteinte de taux sériques inadéquats., Étant donné que la tigécycline est un antibiotique à large spectre, son utilisation doit être limitée aux infections graves et potentiellement mortelles chez les patients hospitalisés.
Telavancin (Vibativ) est le médicament le plus récent à être approuvé par la FDA pour le traitement des infections à SARM.31 C’est un lipoglycopeptide semblable à la vancomycine, bien que son mécanisme d’action diffère. La télavancine perturbe la perméabilité de la membrane cellulaire par dépolarisation de la membrane plasmique, augmentant la perméabilité et la fuite de l’adéno-sinus triphosphate cellulaire et du potassium (K+)., Le moment de ces changements est en corrélation avec une perte rapide de viabilité bactérienne dépendante de la concentration, ce qui suggère que l’activité bactéricide précoce de la télavancine résulte de la dissipation du potentiel membranaire cellulaire et d’une augmentation de la perméabilité membranaire.
Des études cliniques ont montré que la télavancine n’est pas inférieure à la vancomycine dans le traitement de cSSSI.32,33 L’un des avantages de la télavancine par rapport à la vancomycine est l’administration d’une dose quotidienne et la surveillance des niveaux de médicaments n’est pas nécessaire. Cependant, comme la vancomycine, la dose doit être ajustée chez les patients atteints d’insuffisance rénale.,31 la fonction Rénale doit être surveillée pendant et après l’arrêt du traitement chez tous les patients. La télavancine est associée à un allongement de l’intervalle QTc et doit être utilisée avec prudence chez les patients prenant des médicaments qui pourraient également prolonger l’intervalle QTc. Dans les essais cliniques comparant la télavancine à la vancomycine, les effets indésirables rapportés chez plus de 10% des patients traités par la télavancine comprenaient des troubles du goût, des nausées, des vomissements et des urines mousseuses.31 Événements indésirables graves ont été rapportés chez 7% des patients traités par télavancine et comprenaient le plus souvent des événements rénaux, respiratoires ou cardiaques., Il existe un avertissement de boîte noire concernant le risque fœtal associé à l’utilisation de la télavancine; ainsi, les femmes en âge de procréer doivent subir un test de grossesse sérique avant de commencer la télavancine.31
Le ceftobiprole (Zeftera) est la première céphalosporine ayant une activité bactéricide contre le SARM. Son activité antibactérienne comprend l’inhibition des protéines de liaison à la pénicilline impliquées dans la synthèse de la paroi cellulaire. Dans les études cliniques, il était aussi efficace que la combinaison de vancomycine et de ceftazidime dans le traitement de cSSSI.,34 Il est généralement bien toléré, avec les principaux événements indésirables du médicament, y compris les nausées et les troubles du goût. L’utilisation du Ceftobiprole n’est actuellement pas approuvée aux États-Unis et, bien qu’il ait déjà été approuvé au Canada, le fabricant a mis fin à la vente du médicament le 16 avril 201035.Cela faisait suite aux recommandations des organismes de réglementation européens (Comité européen des médicaments à usage humain) et américains (FDA) de ne pas approuver le médicament., Bien que les résultats de la phase III suggèrent des avantages du ceftobiprole, l’intégrité de ces résultats de l’étude soulève des préoccupations en raison de la falsification des données cliniques de certains des sites de l’étude. Avec ce développement récent, l’avenir de l’utilisation du ceftobiprole sur le marché américain reste discutable.
Conclusion
Avec l’émergence du SARM-CA et du SARM hétéro-résistant, il est important que les pharmaciens connaissent tous les agents disponibles pour la prise en charge des infections au SARM. Il est également essentiel de choisir l’agent antimicrobien approprié pour l’infection traitée., En outre, les agents ayant un spectre d’activité plus large (p. ex., la tigécycline) doivent être réservés pour les infections très graves et dans le cadre d’infections à pathogènes multiples. Il est également de la plus haute importance de réserver les nouveaux agents pour les infections plus graves afin de minimiser le développement de la résistance.
1. Boucher HW, Corey GR. Épidémiologie de Staphylococcus aureus résistant à la méthicilline. Clin Infect Dis.
2. Styers D, Sheehan DJ, Hogan P, et al., La surveillance par les laboratoires de l’actuel profils de résistance aux antimicrobiens et les tendances chez Staphylococcus aureus: 2005 statut aux Etats-unis. Ann Clin Microbiol Antimicrob. 2006;5:2.
3. Chien JW, Kucia ML, Salata RA. Utilisation de linézolide, un oxazolidinone, dans le traitement des infections bactériennes gram-positives multirésistantes. Clin Infect Dis. 2000;30:146-151.
4. Soriano A, Martinez JA, Mensa J, et coll. Importance pathogène de la résistance à la méthicilline pour les patients atteints de bactériémie à Staphylococcus aureus. Clin Infect Dis. 2000;30:368-673.
5. Graffunder EM, Venezia RA., Facteurs de risque associés à l’infection nosocomiale à Staphylococcus aureus résistant à la méthicilline (SARM), y compris l’utilisation antérieure d’antimicrobiens. J Antimicrob Chemother. 2002;49:999-1005.
6. Klevens RM, Edwards JR, Tenover FC, et coll. Changements dans l’épidémiologie du Staphylococcus aureus résistant à la méthicilline dans les unités de soins intensifs des hôpitaux américains, 1992-2003. Clin Infect Dis.
7. Levine DP, Cushing RD, Jui J, Brown WJ. Endocardite Staphylococcus aureus résistante à la méthicilline acquise dans la communauté au Detroit Medical Center. Ann Intern Med. 1982;97:330-338.
8., Lodise TP Jr, McKinnon PS, M. Rybak modèle de Prédiction pour identifier les patients avec bactériémie à Staphylococcus aureus à risque pour la résistance à la méthicilline. Infecter le contrôle Hosp Epidemiol. 2003;24:655-661.
9. Le Roi MD, Humphrey BJ, Wang YF, et coll. Émergence du clone Staphylococcus aureus USA 300 résistant à la méthicilline acquis par la communauté comme cause prédominante des infections de la peau et des tissus mous. Ann Intern Med. 2006;144:309-317.
10. Centers for Disease Control and Prevention., Infections à Staphylococcus aureus résistantes à la méthicilline chez les participants à des sports de compétition-Colorado, Indiana, Pennsylvanie et comté de Los Angeles, 2000-2003. MMWR. 2003;52:793-795.
11. Lowy FD. Infections à Staphylococcus aureus. N Engl J Med. 1998;339:520-532.
12. Chambres HF. L’évolution de l’épidémiologie de Staphylococcus aureus? Emerg Infect Dis.
13. Renseignements sur le SARM associé à la communauté à l’intention des cliniciens. La CDC. www.cdc.gov/ncidod/dhqp/ar_ 2008; 46 (supplément 5): S344-S349. 2006;42:389-391. 2001;7:178-182.mrsa_ca_clinicians.HTML. Consulté le 4 juillet 2010.
14. Rybak MJ, LaPlante KL., La communauté résistant à la méthicilline Staphylococcus aureus; un examen. Pharmacothérapie. 2005;25:74-85.
15. Gorwitz RJ, Jernigan DB, Powers JH, et coll. Stratégies pour la gestion clinique de SARM dans la communauté: le résumé d’une réunion d’experts convoquée par le Centers for Disease Control and Prevention. En mars 2006. www.cdc.gov/ncidod/dhqp/pdf/ar/CAMRSA_ExpMtgStrategies.pdf. Consulté le 4 juillet 2010.
16. Sabol KE, Echevarria KL, Lewis JS II. Staphylococcus aureus résistant à la méthicilline associé à la communauté: nouvel insecte, anciens médicaments. Ann Pharmacother. 2006;40:1125-1133.
17., Cléocine (clindamycine) notice. New York, NY: Pfizer Inc; Novembre 2005.
18. Strom BL, Schinnar R, Apter AJ, et coll. Absence de sensibilité croisée entre les antibiotiques sulfonamides et les nonantibiotiques sulfonamides. N Engl J Med. 2003;349:1628-1635.
19. Nicolau DP, Freeman CD, Nightingale CH, et coll. Minocycline versus vancomycine pour le traitement de l’endocardite expérimentale causée par Staphylococcus aureus résistant à l’oxacilline. Agents Antimicrobiens Chemother. 1994;38:1515-1518.
20. Sakoulas G, Moellering RC Jr, L’augmentation de la résistance aux antibiotiques chez résistant à la méthicilline Staphylococcus aureus (souches. Clin Infect Dis. 2008; 46 (supplément 5): S360-S367.
21. Rybak MJ, Akins RL. Émergence de Staphylococcus aureus résistant à la méthicilline avec une résistance intermédiaire aux glycopeptides: signification clinique et options de traitement. Drogue. 201;61:1-7.
22. Tenover FC, Moellering RC Jr La justification de la révision du Clinical and Laboratory Standards Institute à la vancomycine, la concentration inhibitrice minimale critères d’interprétation pour Staphylococcus aureus. Clin Infect Dis. 2007;44:1208-1215.
23., Jeffres MN, Micek ST, Isakow W, et coll. Augmentation de l’incidence de néphrotoxicité avec des concentrations sériques minimales de vancomycine plus élevées. Programme et résumés de la 46e Conférence Interscience sur les Agents antimicrobiens et la chimiothérapie( ICAAC); 27-30 septembre 2006; San Francisco, CA. Résumé K789.
le 24. Zyvox (linézolide) notice d’emballage. New York, NY: Pfizer Inc; Décembre 2009.
25. Kuter DJ, Tillotson GS. Effets hématologiques des antimicrobiens, un accent sur l’oxazolidinone, linézolide. Pharmacothérapie. 201;21:1010-1013.
26. Cubicin (daptomycine) notice d’emballage., Lexington, MA: Cubist Pharmaceuticals; January 2010.
27. Murthy MH, Olson ME, Wickert RW, et al. Daptomycin non-susceptible methicillin-resistant Staphylococcus aureus USA 300 isolate. J Med Microbiol. 2008;57:1036-1038.
28. Mangili A, Bica I, Snydman R, Hamer DH. Daptomycin-resistant methicillin-resistant Staphylococcus aureus bacteremia. Clin Infect Dis. 2005;40:1058-1060.
29. Synercid (quinupristin-dalfopristin) package insert. Greenville, NC: Monarch Pharmaceuticals; June 2008.
30. Tygacil (tigecycline) package insert. Philadelphia, PA: Wyeth Pharmaceuticals; September 2009.,
le 31. Vibativ (telavancin) notice d’emballage. Deerfield, IL: Astellas Pharma États-Unis, Inc; Septembre 2009.
32. Stryjewski ME, Chu VH, O’Riordan DEO, et coll. Télavancine versus thérapie standard pour le traitement des infections compliquées de la peau et de la structure de la peau causées par des bactéries à gram positif: étude FAST 2. Agents antimicrobiens Chemother. 2006;50:862-867.
33. Corey GR. Études de télavancine dans cSSSI. Communication présentée à: Troisième Symposium international sur les infections à Gram Positif résistantes; 10 octobre 2006; Niagara-on-the-Lake, Canada.
34. Vidaillac C, Rybak MJ., Ceftobiprole: first cephalosporin with activity against methicillin-resistant Staphylococcus aureus. Pharmacotherapy. 2009;29:511-525.
35. Discontinuation of the sale of ceftobiprole in Canada. Basilea Pharmaceutica. April 9, 2010. http://hugin.info/134390/R/1401931/356785.pdf. Accessed July 12, 2010.
36. Vibramycin (doxycycline) package insert. New York, NY: Pfizer Inc; April 2007.
37. Minocin (minocycline) package insert. Philadelphia, PA: Triax Pharmaceuticals; March 2006.
38. Bactrim (trimethoprim-sulfamethoxazole) package insert. Philadelphia, PA: AR Scientific; November 2006.
39., Vancocin (vancomycin) package insert. Exton, PA: ViroPharma Inc; October 2005.