CONTEXTE
Principe: La synthèse d’aspirine à partir d’acide salicylique se produit par acétylation en milieu acide. L’acide salicylique interagit avec l’anhydride acétique en présence de quelques gouttes d’acide sulfurique concentré pour produire de l’aspirine et d’une molécule d’acide acétique., Le but de l’ajout d’acide sulfurique (catalyseur) est d’aider et d’augmenter le processus de détachement de l’ion acétate (CH3COO–) de l’anhydride acétique qui est finalement associé à l’ion H+ du groupe hydroxy phénolique dans l’acide salicylique pour être éliminé en tant que mole d’acide acétique.1
Objectif: préparer l’aspirine à partir de l’acide salicylique.,
Réaction:
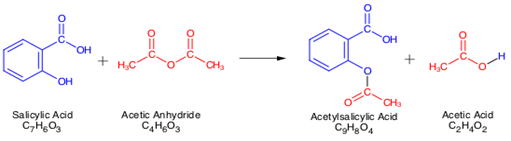
Mécanisme:
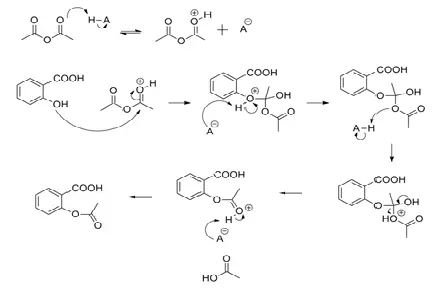
Utilisation:
Utilisé pour le soulagement des mineurs douleurs/maux et aussi la douleur légère à modérée. Il est recommandé pour l’arthrite et les conditions arthritiques connexes, la prophylaxie de l’infarctus du myocarde. Il réduit le risque d’attaques ischémiques transitoires chez les hommes.,
REQUIREMENTS
Chemicals: Salicylic acid – 6 g
Acetic anhydride – 8.,5 ml
Concentrated H2SO4 – 3-4 drops
Methylated spirit
Apparatus: Conical flask – 250 ml
Buchner funnel
Glass rod
Beaker
Filter paper
PROCEDURE
Weigh 6 gs of salicylic acid and transfer it to a clean and dry 250 ml conical flask. Add 8.,5 ml d’anhydride acétique et 3-4 gouttes d’acide sulfurique concentré à le flacon soigneusement et bien mélanger. Réchauffer le mélange au bain-marie à 60 degrés environ 20 min en remuant fréquemment. Laisser refroidir le contenu du flacon et verser dans 100 ml d’eau froide dans un bécher de 250 ml en remuant constamment. Filtrer le produit brut sur un entonnoir Buchner par aspiration, laver à l’eau froide. Recristalliser de l’eau bouillante avec de petites quantités d’alcool méthylé. Sécher le produit synthétisé dans un four à 90 °C et calculer le rendement.,
Calcul
Ici réactif limitant est l’acide salicylique; par conséquent, le rendement devrait être calculé à partir de son montant pris.
la formule Moléculaire de l’acide salicylique = C7H6O3
la formule Moléculaire de l’acide acétylsalicylique (aspirine) = C9H8O4
poids Moléculaire de l’acide salicylique = 138 g/mole
poids Moléculaire de l’acide acétylsalicylique (aspirine) = 180 g/mole
rendement Théorique:
138 g de l’acide salicylique donne 180 g d’aspirine
Donc, 6 g de l’acide salicylique va donner ? (X) g d’aspirine
X =( 180 × 6)/138 = 7.,82 g
rendement Théorique = 7.82 g
Pratique rendement = —– g
% de Rendement = (Pratique de Rendement)/(Rendement Théorique) × 100
CONCLUSION
Aspirine a été synthétisé et le rendement a été trouvé pour être — %. (Le produit est obtenu sous forme de cristaux incolores, rendement 11 g et m. p. 136-137 °C.)