Introduction
L’une des découvertes les plus importantes dans le domaine de la microscopie fluorescente a été trouvée dans une méduse dans les années 1960. Osamu Shimomura de l’Université de Princeton étudiait Aequorea victoria, une méduse bioluminescente., Il convient de noter ici que la luminescence n’est pas la même que la fluorescence:
- Luminescence: émission spontanée de lumière d’une substance (lorsque cette substance est un animal, on parle de bioluminescence)
- Fluorescence: émission de lumière d’une substance qui a absorbé la lumière et devient excitée
Grâce à l’étude de A. victoria, deux protéines majeures ont été découvertes: l’aequorine (une photoprotéine) et la protéine fluorescente verte (GFP). La méduse produit du calcium, qui interagit avec l’aequorine et produit une luminescence bleue., Cette lumière bleue est absorbée par le GFP et réémise sous forme de fluorescence verte. Ces protéines ont été isolées et purifiées à partir de la méduse et sont largement utilisées dans la recherche à ce jour. Pour cette recherche, Osamu Shimomura et ses collègues ont remporté le prix Nobel de chimie en 2008.
Protéine fluorescente verte
La GFP est excitée par la lumière dans la partie bleue/violette / ultraviolette du spectre et émet de la lumière dans la partie verte (d’où son nom). La structure de la protéine peut être vue sur la Fig.1., GFP est une forme de baril avec la partie fluorescente (le chromophore) composée de seulement trois acides aminés. Lorsque ce chromophore absorbe la lumière bleue, il émet une fluorescence verte.
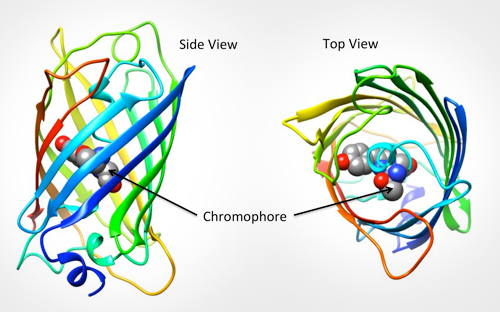
GFP Dans la recherche
L’utilisation de la GFP dans la recherche est devenue claire une fois que le gène de la GFP a également été isolé et que la GFP a pu être ajoutée à des cellules ou greffée génétiquement dans des organismes vivants. Quelques applications et avantages de GFP discutés ci-dessous.
Le GFP comme marqueur de toxicité: en raison du fait que le GFP diminue en intensité de fluorescence avec une toxicité croissante, il peut être utilisé comme marqueur de toxicité environnementale., Le GFP peut être ajouté aux organismes hôtes sans effet négatif, puis l’intensité suivie dans différents environnements dans divers organismes.
GFP est héréditaire, si un organisme a GFP frappé dans son génome, GFP sera naturellement transmis à la progéniture sans aucun processus supplémentaire, permettant des moyens non invasifs d’introduire un marqueur fluorescent et de le suivre à travers des générations d’animaux ou de cellules. GFP n’interfère avec aucun processus biologique., Les souris transgéniques peuvent être marquées avec du GFP, qui est ensuite facilement observé chez leur progéniture simplement en les exposant à la lumière bleue ou UV, comme on le voit sur la Fig.2.
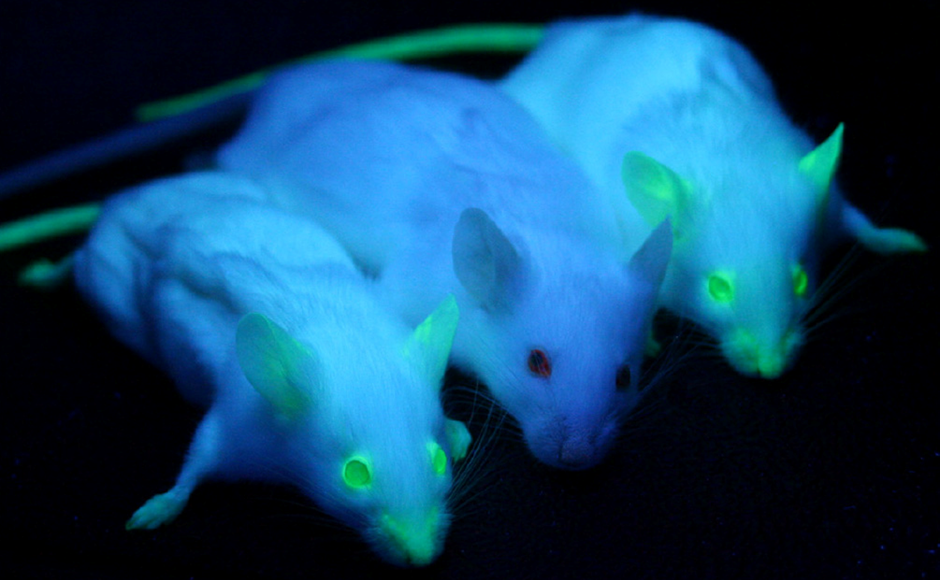
Le GFP peut être fusionné à d’autres protéines, rendant effectivement ces protéines fluorescentes. Cela peut être fait avec des lieurs spéciaux afin que le GFP n’affecte pas la fonction de la protéine d’intérêt et qu’il puisse toujours diffuser à travers les cellules. Cela permet à toute protéine d’être localisée et suivie à l’aide d’une microscopie fluorescente standard, en faisant briller une lumière bleue sur les cellules, la protéine d’intérêt sera fluorescente avec une lumière verte.,
GFP dans des expériences sur cellules vivantes: la molécule fluorescente verte classique est l’isothiocyanate de fluorescéine (FITC), mais elle est toxique pour les cellules et ne peut pas être utilisée directement sans d’abord fixer les cellules ou causer des dommages inévitables. Le GFP est beaucoup moins nocif car il s’agit d’une protéine naturelle et peut être utilisé dans des expériences sur des cellules vivantes tout en ne causant pratiquement aucun dommage, surtout s’il est transmis à la progéniture.
GFP dans les applications avancées de microscopie., Plusieurs applications de microscopie à fluorescence telles que la récupération de fluorescence après photobleaching (FRAP) et le transfert d’énergie par résonance de Förster (FRET) ont été développées avec GFP, permettant aux chercheurs d’utiliser des applications toujours plus spécifiques et puissantes de la fluorescence pour leur imagerie. Ces techniques sont décrites dans d’autres articles courts, à savoir qu’est-ce que FRET et qu’est-ce que FRAP?
La GFP est modifiable, car le code génétique et d’acides aminés de la GFP est bien compris, elle a fait l’objet de plusieurs modifications., Premièrement, le GFP a été modifié pour produire du GFP amélioré (eGFP), qui a une intensité de fluorescence accrue, une plus grande photostabilité, des pics d’excitation plus pratiques et un rendement plus élevé à température ambiante. Les modifications apportées directement au chromophore permettent au GFP de fluorescer avec différentes couleurs, créant du bleu (BFP), du cyan (CFP), du jaune (YFP), du rouge (RFP) et d’autres, qui ont tous été améliorés séparément et ont leurs propres applications. Certaines modifications remarquables incluent mCherry (rouge), Citrine et Vénus (jaune), et Céruléen (cyan) pour n’en nommer que quelques-unes., Des familles entières de protéines fluorescentes existent maintenant, toutes dérivées du GFP original, comme on le voit sur la Fig.3.
Résumé
La GFP est un élément fondamental de la microscopie à fluorescence en raison de la facilité d’utilisation et des applications limitées uniquement par l’imagination du chercheur. Les améliorations constantes de la GFP au fil du temps ont fait avancer la microscopie à fluorescence et la recherche, en raison de la nature très flexible de la GFP et du grand nombre de recherches basées sur l’utilisation de la GFP et de ses nombreuses variantes.