nom commun: mouches du cerf, mouches jaunes et mouches du chevalnom scientifique: Chrysops, Diachlorus et Tabanus spp. (Insecta: Diptera: Tabanidae)
La famille des Tabanidae, communément appelée mouches des chevaux et mouches des cerfs, contient des parasites du bétail, des chevaux et des humains. En Floride, il y a 35 espèces de Tabanidae qui sont considérées comme économiquement importantes. Les mouches des chevaux appartiennent au genre Tabanus et les mouches des cerfs au genre Chrysops., La mouche jaune, Diachlorus ferrugatus (Fabricius), est connue en Floride comme un mordeur féroce. Comme les moustiques, c’est la mouche femelle qui est responsable d’infliger une morsure. Les mâles sont principalement des mangeoires de pollen et de nectar. Les tabanidés sont très probablement rencontrés en été chaud et au début de l’automne. Ils sont actifs pendant la journée.
la Figure 1. Une femelle adulte, Chrysops cincticornis, pond des œufs. Photographie de Jerry Butler, Université de Floride.,
Distribution (Retour en haut de page)
Les mouches des chevaux et les mouches des cerfs sont distribuées dans le monde entier. Ils ne sont cependant pas signalés à Hawaii, au Groenland et en Islande. Aux États-Unis, la Floride produit une grande population de tabanidés en raison de la disponibilité d’un habitat convenable. Le climat doux de la Floride et les grandes zones humides et non développées en permanence fournissent de bonnes zones de reproduction.
Description (Haut de page)
Œufs: Les œufs sont pondus en masses allant de 100 à 1000 œufs., Les œufs sont pondus en couches sur une surface verticale telle que le feuillage en surplomb, les rochers en saillie, les bâtons et la végétation aquatique. La végétation aquatique est préférée. Une sécrétion brillante ou crayeuse, qui aide à la protection de l’eau, recouvre souvent les œufs. Les surfaces verticales sur lesquelles les œufs sont déposés sont toujours directement sur l’eau et un sol humide favorable au développement des larves. La femelle ne déposera pas de masses d’œufs sur une végétation trop dense. Les œufs sont initialement d’une couleur blanc crème, mais s’assombrissent rapidement en gris et noir. Les œufs sont de forme cylindrique et mesurent de 1 à 2,5 mm de longueur., Les œufs éclosent en cinq à sept jours, selon les conditions météorologiques ambiantes, et les larves tombent dans le sol humide et l’eau en dessous.
la Figure 2. Mouche du cerf, Chrysops sp., masse d’oeuf après l’assombrissement. Photographie de Jerry Butler, Université de Floride.
la Figure 3. Habitat typique utilisé par les mouches piqueuses pour la ponte. Photographie de John Capinera, Université de Floride.
Larves: Les larves utilisent une épine à éclosion pour sortir de la caisse de l’œuf., Les larves sont aquatiques, semi-aquatiques ou terrestres. Chrysops spp. sont appelés « hydrobiontes » et se trouvent dans les zones à forte teneur en eau. Tabanus spp. préférez les substrats plus secs et sont des « hémi-hydrobiontes ». Les larves se rétrécissent à chaque extrémité et sont généralement de couleur blanchâtre, mais peuvent également être brunâtres ou vertes selon les espèces. Des bandes noires se trouvent autour de chaque segment du corps chez de nombreuses espèces. La larve respire à travers un siphon trachéal situé à leur extrémité postérieure. La larve a une petite tête et 11 à 12 segments supplémentaires. Les larves traversent six à neuf stades., Le temps passé au stade larvaire peut durer de quelques mois à un an. Les larves de Chrysops se nourrissent de matière organique dans le sol. Tabanus spp. se nourrit de larves d’insectes, de crustacés et de vers de terre. Même si les Tabanus spp. sont considérés comme carnivores et cannibales, des rapports de jusqu’à 120 larves par yard carré ont été trouvés. La larve se déplace dans les 2,5 à 5,0 cm supérieurs du sol, où elle est plus sèche, lorsqu’elle est prête à se nymphoser. Dans les deux jours qui suivent le déplacement à la surface, le stade nymphal est atteint.,
la Figure 4. Larve typique d’une espèce de Tabanidae. Photo de Jason M. Squitier, Université de Floride.
Pupes: Les pupes sont de couleur brune, arrondies vers l’avant, effilées vers l’arrière, et ont des pattes et des ailes attachées au corps. Il y a une rangée d’épines entourant chaque segment abdominal. Un « aster » nymphal composé de six projections pointues est situé au sommet de l’abdomen. Le stade nymphal dure généralement de deux à trois semaines.,
la Figure 5. Pupe typique des Tabanidae. Photo de Jason M. Squitier, Université de Floride.
Adulte: La mouche adulte émerge de la nymphe par une fente située le long du thorax de la nymphe. Dans la plupart des espèces, les mâles émergent avant les femelles. Après l’apparition des deux sexes, les mouches s’accouplent. L’accouplement commence avec le mâle poursuivant la femelle. L’accouplement est initié dans les airs et terminé au sol. La femelle dépose alors une masse d’œufs et est prête à chercher un hôte., Les Tabanidae adultes sont de grandes mouches au corps large et aux yeux exorbités. Les mâles sont facilement différenciés des mouches femelles parce que les yeux sont contigus chez les mâles et largement séparés chez les femelles. Les antennes sont trois segmentées. Le thorax et l’abdomen sont couverts de poils fins. Les mouches du cerf mesurent de 7 à 10 mm de long, tandis que les mouches du cheval mesurent de 10 à 25 mm. Les mouches du cerf sont jaunes à noires, ont des rayures sur l’abdomen et possèdent des ailes tachetées avec des taches sombres., Les mouches jaunes sont jaunâtres avec la même forme de corps que les mouches du cerf, mais ont des yeux violet foncé à noir marqués de lignes vertes fluorescentes. Les mouches à cheval sont noires à brun foncé avec des yeux verts ou noirs. Les mouches des cerfs adultes ont des éperons apicaux sur les tibias postérieurs qui ne sont pas présents chez les mouches des chevaux.
la Figure 6. Femelle adulte cerf mouche, Chrysops pikei Whitney. Photographie par Sturgis McKeever, Georgia Southern University; www.insectimages.org.
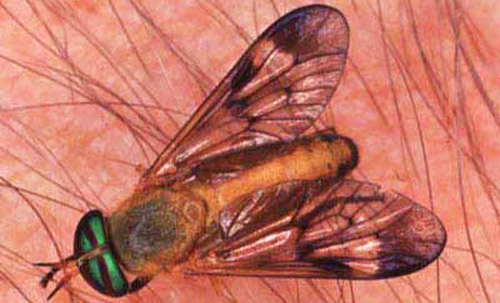
la Figure 7., Mouche jaune adulte, Diachlorus ferrugatus (Fabricius). Photographie de Jerry Butler, Université de Floride.
la Figure 8. Adulte cheval mouche, Tabanus sp. Photographie de James Castner, Université de Floride.
Cycle de vie (Haut de page)
Les tabanidés adultes sont rencontrés en Floride entre les mois de mai et septembre. La plupart des espèces hivernent au stade larvaire et se nymphosent au printemps et au début de l’été. Une masse d’œufs a été trouvée dès le 5 mai et le 13 octobre., La plupart ont un cycle de vie d’un an, mais certaines espèces plus grandes peuvent prendre deux ou trois ans. La durée de vie adulte est de 30 à 60 jours.
Dégâts (Retour en haut)
Les tabanidés guettent dans les zones ombragées sous les buissons et les arbres un hôte. La vue est le principal mécanisme de recherche de l’hôte, mais le dioxyde de carbone et l’odeur jouent également un rôle. Les objets en mouvement, surtout s’ils sont de couleur foncée, sont les plus enclins à attaquer. Les attaques se produisent pendant la journée avec un pic qui commence au lever du soleil et dure trois heures. Un deuxième pic est deux heures avant le coucher du soleil et commence peu après., La fréquence d’attaque est faible par temps couvert ou à des températures inférieures à 22 ºC et supérieures à 32 ºC. Sur le bétail, les morsures se produisent sur l’abdomen, les jambes et le cou. Les tabanides infligent des blessures profondes qui provoquent un flux de sang. Les mandibules et les maxilles pénètrent la peau dans une action en ciseaux. Les anticoagulants contenus dans la salive sont pompés dans la plaie et le sang est ingéré par la labelle épongeuse. Les agents pathogènes peuvent être transmis par des mouches qui sont perturbées en se nourrissant d’un animal et commencent à se nourrir d’un autre., On sait que les mouches des cerfs peuvent mécaniquement vectoriser la Tularémie et le Loa loa, et que les mouches des chevaux transmettent l’Anthrax. Les attaques de mouches entraînent une diminution des gains et une faible production de lait chez les animaux d’élevage. En 1976, les pertes estimées aux États-Unis étaient de 40 millions de dollars. Un ranch de bétail dans le Kentucky a perdu en moyenne 100 livres. par animal en raison de tabanidés. Il n’est pas rare de voir jusqu’à 100 mouches se nourrir d’un animal en même temps. Vingt à trente mouches nourrissant pendant six heures sont capables de prendre 100 cc de sang.,
Lutte biologique (Haut de page)
Il n’existe aucun programme de lutte biologique efficace pour lutter contre les tabanidés. Il existe des insectes bénéfiques indigènes qui ciblent les tabanidés. Les œufs sont parasités par des familles d’hyménoptères comme les Trichogrammatidae, les Scelionidae et les Chalcididae. Les Diapriidae et les Pteromalidae (Hyménoptères) et les Bombyliidae et les Tachinidae (Diptères) parasitent les larves et les pupes. Les adultes tabanidés sont utilisés comme provisions pour la construction de nids de guêpes. Les aigrettes bovines et les killdeer sont également des mangeoires de tabanidés.,
Gestion (Haut de page)
Actuellement, il n’existe pas de moyens adéquats pour gérer les populations. Les pièges sont parfois efficaces dans de petites zones telles que les cours, les sites de camping et les piscines. Le piégeage des mouches nuisibles a réduit leur nombre sur la côte atlantique des États-Unis. Les pièges ont été efficaces lorsqu’ils sont utilisés autour de bovins confinés dans des zones gérables.
Certains pièges sont des boules noires et brillantes. Les mouches sont attirées par ces objets lorsque le vent les déplace., Les pièges à malaise peuvent attraper un grand nombre de mouches en se trouvant simplement sur leur trajectoire de vol ou en utilisant des attractifs, tels que le CO2 et l’octénol. Ces pièges sont surtout utiles pour l’échantillonnage. Pour la protection personnelle, les chemises et les pantalons à manches longues en combinaison avec un répulsif contenant du diéthyltoluamide (DEET), de la citronnelle ou du géraniol sont affectifs. Pour le bétail, les pyréthroïdes fonctionnent comme des répulsifs limités. Les méthodes d’auto-application ne sont pas efficaces pour les mouches à cheval. Les étiquettes auriculaires et les colliers de tête imprégnés d’insecticides ont réussi à contrôler., Pour le piégeage par enlèvement, des recherches récentes ont montré que les cylindres bleus (gobelets inversés, par exemple) recouverts d’un matériau collant et fixés à des objets à déplacement lent (<7 mi/h) (l’avant d’un camion ou d’une tondeuse à gazon) ou sur un capuchon porté au sommet de la tête d’une personne sont efficaces pour réduire l’abondance de ces mouches. Voir Trolling Deer Fly Trap pour plus d’informations.
la Figure 9. Ball trap, sphère noire, utilisé pour attirer les mouches mordantes. Photo de Jason Squitier, Université de Floride.,
la Figure 10. Piège attractif, avec sphère noire, utilisé pour attirer les mouches mordantes. Photographie par Andy Rasmussen, en Floride, Un&M University.
la Figure 11. Les pièges à malaise peuvent attraper un grand nombre de mouches piqueuses en se trouvant simplement sur leur trajectoire de vol ou en utilisant des attractifs, tels que le CO2 et l’octénol. Photo de Jason Squitier, Université de Floride.
la Figure 12., Un cylindre de couleur bleue recouvert d’un matériau collant constitue un piège efficace pour les mouches à cerf et autres tabanidés lorsqu’il est attaché à un objet en mouvement lent (< 7 mi/hr). Photographie de R. F. Mizell, Université de Floride.
Certaines méthodes à grande échelle telles que la manipulation de l’habitat ont été suggérées. Cela pourrait être fait en enlevant les plantes ligneuses inutiles des zones résidentielles ou en drainant les zones humides pour réduire l’habitat de reproduction convenable.
L’utilisation d’insecticides est généralement considéré comme économiquement irréalisable., Des insecticides granulaires ont été appliqués sur l’eau dans les années 1950, mais les effets sur l’environnement ont finalement été pris en compte. La pulvérisation pour les adultes est également inefficace. Une protection individuelle contre les adultes peut être obtenue en utilisant un répulsif sur la peau et les vêtements exposés avant l’exposition.
la Floride Insectes Guide de Gestion pour les mouches piqueuses
Références Sélectionnées (Haut de page)
- Anderson JF. 1973. Comportement mordant des mouches du cerf de Virginie (Diptera: Tabanidae). Annales de la Société entomologique d’Amérique 66: 21-23.
- Burnet SUIS, Hays KL. 1974., Certaines influences des facteurs météorologiques sur l’activité de vol des mouches femelles (Diptera: Tabanidae). L’Entomologie De L’Environnement 3: 515-521.
- Borror DJ, Triplehorn CA, Johnson NF. 1992. Une introduction à l’étude des insectes. Sanders Collège De L’Édition, De Ft. Valoir. 512 pp.
- Catts EP, Olkowski W. 1972. Biologie des Tabanides (Diptères): accouplement et comportement alimentaire de Chrysops fulginosus. L’Entomologie De L’Environnement 1: 448-453.
- Curran CH. 1934. Les Familles et les genres de Diptères nord-américains. American Museum of Natural History, New York. pp. 148-149.
- Essig EO., 1958. Insectes et Acariens de l’Ouest de l’Amérique du Nord. La société Macmillan Co. De New-York. 1050 pp.
- Fairchild GO, Weems Jr HV. 1973. Doachlorus ferrugatus (Fabricius), une mouche piquante féroce (Diptera: Tabanidae). La floride Ministère de l’Agriculture et des Services aux Consommateurs, Division de l’Usine de l’Industrie de l’Entomologie Circulaire 139.
- Foster CA, Renuad GD, Hays KL. 1973. Certains effets de l’environnement sur la ponte par Chrysops (Diptera: Tabanidae). L’Entomologie De L’Environnement 2: 1048-1050.
- Français FE, Kline DL. 1989. 1-octen-3-ol, un piège attractif efficace pour les Tabanidae (Diptères)., Journal d’entomologie médicale 26: 459-461.
- Français FE, Hagan DL. 1995. Un piège à boîte à deux niveaux capture Chrysops atlanticus et C. fuliginosus (Diptera: Tabanidae) près d’un marais salé de Géorgie. Journal d’entomologie médicale 32: 197-200.
- Hansens EJ, Robinson JW. 1973. Émergence et mouvement des mouches Chrysops fluginosus et Chrysops atlanticus. Annales de la Société entomologique d’Amérique 66: 1215-1218.
- Harwood RF, James MT. 1979. Entomologie en Santé Humaine et Animale. Macmillan Publishing Co. De New-York. 548 pp.
- Herms WB. 1961., Entomologie médicale. Macmillan Co. De New-York. 582 pp.
- Jones CM, Anthony DW. 1964. Les Tabanidae (Diptères) de Floride. U. S. D. A. Bulletin 1295: 1-85.
- Logothetis C, Schwardt HH. 1948. Études biologiques sur les mouches à cheval de New York. Journal d’entomologie économique 41: 335-336.
- Mckeever S, Français FE. 1997. Fascinant, beau, mangeoires de sang. Entomologiste américain 43: 217-225.
- Mizell RF. (Décembre 1998). Le piège à mouches de cerf à la traîne. Alerte antiparasitaire UF / IFAS. (29 mai 2014).
- Pechuman LL. 1973., Mouches à cheval et mouches à cerf de Virginie (Diptera: Tabanidae). Virginie Division De La Recherche Bulletin De 81: 1-9.
- Riley WA, Johannsen OA. 1938. Entomologie médicale. McGraw-Hill Book Co, Inc. De New-York. 483 pp.
- Tashiro H, Schwart HH. 1949. La biologie des principales espèces de mouches à cheval du centre de New York. Journal d’entomologie économique 42: 269-272. s
- Mur R, Shearer D. 1997. Entomologie vétérinaire. Chapman & Hall de New York. 439 pp.
- Wilson BH. 1968. Réduction des popoulations de tabanidés sur les bovins avec des pièges collants appâtés avec de la glace carbonique., Journal d’entomologie économique 61: 827-829.