Le but des organes lymphoïdes est de fournir une immunité au corps. Ce deuxième article d’une série en six parties explique les organes lymphoïdes primaires et secondaires ainsi que leur signification clinique et leur structure. Il est livré avec une auto-évaluation vous permet de tester vos connaissances après l’avoir lu,
Résumé
Cet article est le deuxième d’une série en six parties sur le système lymphatique. Il discute du rôle des organes lymphoïdes, qui est de développer et de fournir une immunité au corps., Les organes lymphoïdes primaires sont la moelle osseuse rouge, dans laquelle le sang et les cellules immunitaires sont produits, et le thymus, où les lymphocytes T mûrissent. Les ganglions lymphatiques et la rate sont les principaux organes lymphoïdes secondaires; ils filtrent les agents pathogènes et maintiennent la population de lymphocytes matures.
Citation: Nigam Y, Knight J (2020) Le système lymphatique 2: structure et fonction des organes lymphoïdes. Temps de soins infirmiers; 116: 11, 44-48.,
Auteurs: Yamni Nigam est professeur en sciences biomédicales; John Knight est professeur agrégé en sciences biomédicales; tous deux au Collège des Sciences Humaines et de la Santé de l’Université de Swansea.,
- Cet article a été examiné en double aveugle par des pairs
- Faites défiler vers le bas pour lire l’article ou téléchargez un PDF imprimable ici (si le PDF ne parvient pas à télécharger entièrement, veuillez réessayer en utilisant un navigateur différent)
- Cliquez ici pour voir les autres articles de cette série
- Évaluez vos connaissances et obtenez des les principaux organes lymphoïdes et leur rôle dans le développement et l’immunité du corps., Les organes lymphoïdes comprennent la moelle osseuse rouge, le thymus, la rate et les grappes de ganglions lymphatiques (Fig 1). Ils ont de nombreux rôles fonctionnels dans le corps, notamment:
- Production de cellules sanguines, y compris les globules rouges (érythrocytes), les globules blancs (leucocytes) et les plaquettes (thrombocytes);
- Élimination des globules rouges endommagés;
- Maturation des cellules immunitaires;
- Piégeage de matières étrangères.,
La moelle osseuse rouge et le thymus sont considérés comme des organes lymphoïdes primaires, car la majorité des cellules immunitaires proviennent d’eux.

La moelle osseuse rouge
la moelle Osseuse est molle, gélatineuse tissus présents dans la cavité centrale des os longs comme le fémur et l’humérus. Les cellules sanguines et les cellules immunitaires proviennent de la moelle osseuse; elles se développent à partir de cellules souches immatures (hémocytoblastes), qui suivent des voies de développement distinctes pour devenir des érythrocytes, des leucocytes ou des plaquettes., Les cellules souches se multiplient rapidement pour produire des milliards de cellules sanguines chaque jour; ce processus est connu sous le nom d’hématopoïèse et est décrit dans la figure 2.

Pour assurer une production et une différenciation continues des cellules sanguines pour remplacer celles qui ont perdu leur fonction ou leur âge, des cellules souches hématopoïétiques sont présentes à l’âge adulte. Dans l’embryon, les cellules sanguines sont initialement fabriquées dans le sac vitellin mais, au fur et à mesure du développement de l’embryon, cette fonction est reprise par la rate, les ganglions lymphatiques et le foie., Plus tard dans la gestation, la moelle osseuse reprend la plupart des fonctions hématopoïétiques de sorte qu’à la naissance, tout le squelette est rempli de moelle osseuse rouge.
La moelle osseuse rouge produit tous les érythrocytes, leucocytes et plaquettes. Les cellules souches hématopoïétiques de la moelle osseuse suivent les lignées myéloïdes ou lymphoïdes pour créer des cellules sanguines distinctes (Fig 2); il s’agit notamment des cellules progénitrices myéloïdes (monocytes, macrophages, neutrophiles, basophiles, éosinophiles, érythrocytes, cellules dendritiques et plaquettes) et des cellules progénitrices lymphoïdes (lymphocytes T, lymphocytes B et cellules tueuses naturelles).,
Certaines cellules lymphoïdes (lymphocytes) commencent à vivre dans la moelle osseuse rouge et se forment complètement dans les organes lymphatiques, y compris le thymus, la rate et les ganglions lymphatiques. Lorsque la puberté est atteinte et que la croissance ralentit, une conversion physiologique se produit, transformant la moelle osseuse rouge en moelle osseuse jaune. Tout ce processus est terminé à l’âge de 25 ans, lorsque la distribution de la moelle osseuse rouge montre son modèle adulte dans les os.,
Le schéma est caractérisé par:
- La présence de moelle osseuse rouge dans le squelette axial (les corps vertébraux, l’os sacré et les parties médiales des os de la hanche) et les extrémités articulaires des os huméraux et fémoraux;
- Les parties les plus distales du squelette étant remplies uniquement de moelle osseuse jaune, qui sert principalement de réserve pour les graisses, assurant la subsistance et maintenant le bon environnement pour le fonctionnement de l’os.,
Cependant, dans des conditions particulières, comme une perte de sang sévère ou de la fièvre, la moelle jaune peut revenir à la moelle rouge (Malkiewicz et Dziedzic 2012).
Maladies de la moelle osseuse et greffes
Toute maladie ou trouble qui constitue une menace pour la moelle osseuse peut affecter de nombreux systèmes du corps, en particulier s’il empêche les cellules souches de se transformer en cellules essentielles. Ceux connus pour endommager la capacité productive de la moelle et détruire les cellules souches comprennent:
- Leucémie;
- Lymphome de Hodgkin;
- Autres lymphomes.,
Un nombre croissant de maladies peuvent être traitées par une greffe de moelle osseuse ou un transfert de cellules souches hématopoïétiques; ceci est souvent réalisé en récoltant des cellules souches de donneurs appropriées dans les crêtes iliaques postérieures de l’os de la hanche, où la concentration de moelle osseuse rouge est la plus élevée.
Le thymus
Le thymus est un organe bi-lobé, gris rosé, situé juste au-dessus du cœur dans le médiastin, où il repose sous le sternum (sternum)., Structurellement, le thymus ressemble à un petit nœud papillon, qui s’atrophie progressivement (rétrécit) avec l’âge. Chez les pré-pubescents, le thymus est un organe relativement grand et très actif qui, généralement, pèse environ 40g, mais chez un adulte d’âge moyen, il peut avoir suffisamment rétréci pour être difficile à localiser., À l’âge de 20 ans, le thymus est 50% plus petit qu’il ne l’était à la naissance, et à l’âge de 60 ans, il a rétréci à un sixième de sa taille d’origine (Bilder, 2016); c’est ce qu’on appelle l’involution thymique
Chacun des deux lobes du thymus est entouré d’une capsule, à l’intérieur de laquelle se trouvent de nombreux petits lobules – mesurant généralement de 2 à 3 mm de largeur-qui sont maintenus ensemble par du tissu conjonctif lâche., Chaque lobule est constitué de follicules composés d’un cadre de cellules épithéliales sécrétrices de thyomsine et d’une population de lymphocytes T; ces cellules sont communément appelées cellules T (le » T » désigne leur origine en tant que cellules matures du thymus). Les lobules ont deux zones distinctes:
- Un cortex externe dense qui est riche en lymphocytes T à division active;
- Une médullaire interne, qui est beaucoup plus pâle et fonctionne comme une zone de maturation des lymphocytes T.,
En plus d’être un organe lymphoïde majeur, le thymus est également reconnu comme faisant partie du système endocrinien car il sécrète une famille d’hormones collectivement appelées thymosine; c’est un groupe de plusieurs hormones structurellement apparentées sécrétées par les cellules épithéliales thymiques. Ces hormones sont essentielles à la fonction immunitaire normale et de nombreux membres de la famille de la thymosine sont utilisés thérapeutiquement pour traiter les cancers, les infections et les maladies telles que la sclérose en plaques (Severa et al, 2019).,
Rôle dans la maturation des lymphocytes T
Les lymphocytes T proviennent sous forme de cellules souches hématopoïétiques de la moelle osseuse rouge (Fig 2). Une population de ces cellules souches hématopoïétiques s’infiltre dans le thymus, se divisant plus loin dans les régions corticales des lobules puis migrant dans les régions médullaires pour mûrir en lymphocytes T actifs; ce processus de maturation des lymphocytes T est contrôlé par l’hormone thymosine., Une partie de ces lymphocytes T matures migrent continuellement du thymus vers le sang et d’autres organes lymphoïdes (rate et ganglions lymphatiques), où ils jouent un rôle majeur dans les réponses immunitaires spécifiques de l’organisme (qui sera discuté en détail dans la partie 3 de cette série). L’importance de ces cellules est évidente chez les patients dont les populations de lymphocytes T sont épuisées, tels que ceux infectés par le VIH.
L’une des fonctions les plus importantes du thymus est la programmation des lymphocytes T pour reconnaître les antigènes « auto » à travers un processus appelé éducation thymique., Ce processus permet aux lymphocytes T matures de distinguer le matériel étranger, et donc potentiellement pathogène, des antigènes appartenant au corps. Il a été démontré que l’ablation du thymus peut entraîner une augmentation des maladies auto-immunes, car cette capacité à se reconnaître est diminuée (Sherer et al, 1999).
Signification clinique
Les maladies du thymus comprennent le cancer du thymique et la myasthénie grave (MG). MG se produit lorsque le thymus produit des anticorps qui bloquent ou détruisent les sites des récepteurs musculaires, ce qui affaiblit les muscles et les fatigue facilement., Il affecte le plus souvent les muscles qui contrôlent les yeux et les paupières, ce qui entraîne des paupières tombantes et des difficultés à faire des expressions faciales; mâcher, avaler et parler deviennent également difficiles. MG peut affecter les personnes de tout âge, mais commence généralement chez les femmes âgées <40 ans et les hommes âgés >60 ans.
Dans la plupart des cas de cancer MG ou thymique, la thymectomie est recommandée., Les patients qui ont subi une thymectomie peuvent développer une immunodéficience connue sous le nom de syndrome de Good, ce qui augmente leur sensibilité aux pathogènes opportunistes bactériens, fongiques et viraux; cette affection est cependant relativement rare.
La rate
La rate et les ganglions lymphatiques sont deux organes lymphoïdes secondaires majeurs qui jouent un rôle clé dans:
- Filtrer et détruire les agents pathogènes indésirables;
- Maintenir la population de lymphocytes matures (qui sont des globules blancs) pour permettre à la réponse immunitaire adaptative de commencer.,
Lorsque des antigènes étrangers atteignent ces organes, ils initient l’activation des lymphocytes et l’expansion clonale et la maturation subséquentes de ces globules blancs importants. Les lymphocytes matures peuvent alors quitter les organes secondaires pour entrer dans la circulation, ou se rendre dans d’autres zones et cibler des antigènes étrangers.
La rate est le plus grand organe lymphoïde., Situé dans la région hypochondriaque supérieure gauche de la cavité abdominale, entre le diaphragme et le fond de l’estomac, il fonctionne principalement comme un filtre pour le sang, l’amenant en contact étroit avec les phagocytes (globules blancs dans la rate qui rechercheront et « mangeront » tous les agents pathogènes dans le sang) et les lymphocytes.
En raison de sa vascularisation étendue, la rate est un organe ovale violacé foncé; chez l’adulte, elle mesure environ 12 cm de long, 7 cm de large et pèse environ 150g., Cependant, la taille de la rate peut varier en fonction des circonstances: elle diminue lors de la famine, après un exercice intense et après une hémorragie sévère (Gujar et al, 2017), et des études récentes indiquent une augmentation de la taille chez les individus bien nourris et lors de l’ingestion de nourriture (Garnitschnig et al, 2020).
La rate (Figure 3) est enfermée dans une capsule fibro-élastique dense qui fait saillie dans l’organe sous forme de trabécules; ces trabécules constituent le cadre de l’organe., Le sang entre dans la rate à partir de l’artère splénique et sort par la veine splénique, qui sont toutes deux au niveau du hile; la veine splénique devient finalement un affluent de la veine porte hépatique.

La rate est composée de deux régions:
- Stroma – comprenant la capsule externe dense avec ses trabécules, quelques fibres et fibroblastes (cellules qui sécrètent le collagène du tissu conjonctif);
- Parenchyme – composé de deux types de tissu entremêlant appelé pulpe blanche et pulpe rouge.,
La pulpe blanche est une masse de centres germinaux de lymphocytes B en division (cellules B), entourés de lymphocytes T et de cellules accessoires, y compris les macrophages et les cellules dendritiques; ces cellules sont disposées sous forme de nodules lymphatiques autour des branches de l’artère splénique. Lorsque le sang s’écoule dans la rate par l’artère splénique, il pénètre dans les artères centrales plus petites de la pulpe blanche, atteignant finalement la pulpe rouge. La pulpe rouge est un tissu spongieux, représentant 75% du volume splénique (Pivkin et al, 2016); elle se compose de sinus veineux remplis de sang et de cordons spléniques.,
Les cordons spléniques sont constitués de globules rouges et blancs et de plasmocytes (cellules B productrices d’anticorps); par conséquent, la pulpe rouge fonctionne principalement comme un système de filtration pour le sang, tandis que la pulpe blanche est l’endroit où les réponses adaptatives des cellules T et B sont montées. La couleur de la pulpe blanche provient des lymphocytes étroitement emballés et la couleur de la pulpe rouge est due au nombre élevé d’érythrocytes (Stewart et McKenzie, 2002).,
Fonctions
La rate a trois fonctions principales:
- Pour créer une réponse immunitaire et éliminer les micro-organismes de la circulation;
- Pour détruire les globules rouges endommagés et usés;
- Pour stocker les plaquettes (et le sang).
La fonction immunologique principale de la rate est d’éliminer les micro-organismes de la circulation. Les nodules lymphatiques sont disposés comme des manchons autour des vaisseaux sanguins, apportant du sang dans la rate., Dans la pulpe blanche se trouvent des nodules spléniques appelés corpuscules malpighiens, qui sont riches en cellules B, de sorte que cette partie du tissu lymphoïde répond rapidement à une stimulation antigénique étrangère en produisant des anticorps. Les parois du maillage des sinus dans la pulpe rouge contiennent également des phagocytes qui engloutissent les particules étrangères et les débris cellulaires, les filtrant efficacement et les retirant de la circulation.
Dans la destruction de la rate des globules rouges anciens et sénescents, ils sont digérés par les macrophages phagocytaires dans la pulpe rouge. L’hémoglobine est ensuite divisée en hémoglobine et globine., La globine est décomposée en ses acides aminés constitutifs, qui peuvent être utilisés dans la synthèse d’une nouvelle protéine. Haem se compose d’un atome de fer entouré de quatre anneaux non-fer (pyrrole).
Le fer est retiré et transporté pour être stocké sous forme de ferritine, puis réutilisé pour fabriquer de l’hémoglobine nouvelle dans la moelle osseuse rouge; les macrophages convertissent les anneaux pyrrole en pigment vert biliverdine puis en pigment jaune bilirubine. Les deux sont transportés vers le foie lié à l’albumine plasmatique., La bilirubine, le pigment le plus toxique, est conjuguée dans le foie pour former un composé moins toxique, qui est excrété dans la bile.
La pulpe rouge sert en partie à stocker une grande réserve de plaquettes du corps – jusqu’à un tiers de l’apport plaquettaire total. Chez certains animaux – en particulier les mammifères sportifs tels que les chevaux, les lévriers et les renards – la rate est également un important réservoir de sang, qui est libéré dans la circulation pendant les périodes de stress pour améliorer les performances aérobies., Chez l’homme, cependant, la rate ne contribue qu’à un faible pourcentage de cellules sanguines dans la circulation active sous stress physiologique; le volume sanguin total stocké ne serait que de 200 à 250 ml (Bakovic et al, 2005). La capsule de la rate peut se contracter à la suite d’une hémorragie, libérant cette réserve dans la circulation dans le corps.
La rate joue également un rôle mineur dans l’hématopoïèse: la rate produit généralement des érythrocytes, ainsi que la moelle osseuse, chez les fœtus de moins de cinq mois de gestation.,
Signification clinique
Comme la rate est la plus grande collection de tissu lymphoïde dans le corps, les infections qui provoquent la prolifération des globules blancs et la stimulation antigénique peuvent provoquer une expansion des centres germinaux de l’organe, entraînant son élargissement (splénomégalie). Cela se produit dans de nombreuses maladies-par exemple, le paludisme, la cirrhose et la leucémie. La rate n’est généralement pas palpable, mais une rate hypertrophiée est palpable pendant l’inspiration profonde. L’élargissement peut également être causé par une obstruction du flux sanguin, par exemple dans la veine porte hépatique.,
Ablation
La position anatomique de la rate coïncide avec la dixième côte gauche. Compte tenu de sa proximité avec la paroi abdominale, c’est l’un des organes les plus souvent blessés dans les traumatismes abdominaux contondants. La rate est un organe fragile et, en raison de sa nature hautement vascularisée, toute lésion provoquant une rupture entraînera rapidement une hémorragie intrapéritonéale sévère; la mort peut en résulter par une perte de sang massive et un choc.
Une lésion splénique modérée peut être gérée de manière conservatrice, mais une rupture ou une rupture de la rate importante peut être traitée par une ablation complète et rapide (splénectomie)., Cependant, les données actuelles soutiennent la prise en charge non opératoire réussie de nombreuses blessures spléniques traumatiques, dans l’intention de réduire le besoin d’élimination complète (Armstrong et al, 2019).
Les patients traités pour certaines maladies malignes peuvent également nécessiter une splénectomie partielle ou totale et, bien que d’autres structures telles que la moelle osseuse et le foie puissent prendre en charge certaines des fonctions habituellement exercées par la rate, ces patients peuvent présenter un risque accru d’infection., Avec une infection post-splénectomie écrasante, il existe également un risque accru de septicémie, associée à une morbidité et à une mortalité importantes. L’infection est habituellement avec des agents pathogènes encapsulés, y compris Streptococcus pneumoniae, Haemophilus influenzae et Neisseria meningitidis. Les lignes directrices cliniques pour aider à réduire le risque d’infection préconisent une éducation sur la prévention des infections, la vaccination et la prophylaxie antibiotique (Arnott et al, 2018).,
« Les ganglions lymphatiques enflés et la fièvre sont des signes sûrs que le corps développe une réponse immunitaire efficace contre un agent pathogène incriminé”
Ganglions lymphatiques
Les ganglions lymphatiques varient en taille et en forme, mais sont généralement des structures en forme de haricot regroupées à des endroits spécifiques du corps. Bien que leur taille varie, chaque nœud a une structure interne caractéristique (Fig 4).,
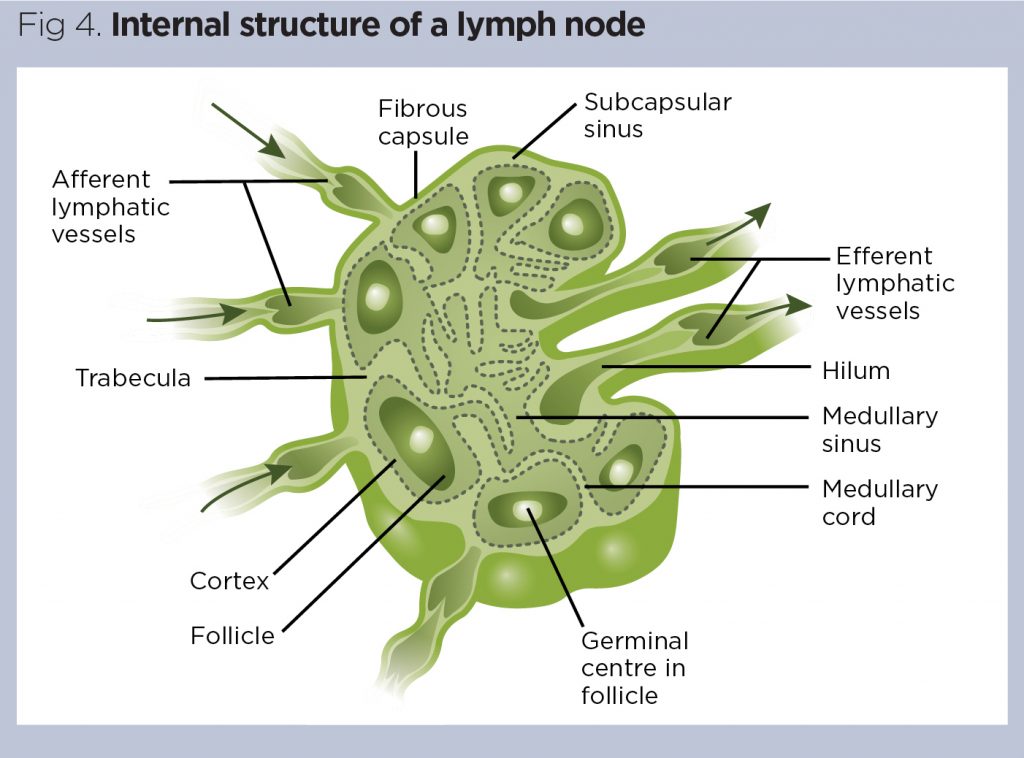
Les parties centrales du ganglion lymphatique sont essentielles à sa fonction; ici, il y a un grand nombre de macrophages fixes, qui phagocytent des matières étrangères telles que des bactéries au contact, et des populations de cellules B et T. Les ganglions lymphatiques sont essentiels à la plupart des réponses immunitaires médiées par les anticorps: lorsque les macrophages phagocytaires piègent du matériel pathogène, ce matériel est présenté aux lymphocytes afin que des anticorps puissent être générés.,
Chaque ganglion lymphatique est alimenté par un ou plusieurs vaisseaux lymphatiques afférents, qui délivrent une lymphe brute non modifiée directement à partir des tissus voisins. Un nœud sain et pleinement fonctionnel élimine la majorité des agents pathogènes de la lymphe avant que le liquide ne quitte par l’intermédiaire d’un ou plusieurs vaisseaux lymphatiques efférents. En plus de son apport lymphatique, chaque ganglion lymphatique est alimenté en sang via une petite artère; l’artère délivre une variété de leucocytes, qui peuplent les régions internes du ganglion.,
Lorsque l’infection est présente, les ganglions lymphatiques deviennent de plus en plus métaboliquement actifs et leurs besoins en oxygène augmentent. Une petite veine transporte le sang désoxygéné loin de chaque nœud et le renvoie aux veines principales. En période d’infection, ce sang veineux peut transporter une variété de messagers chimiques (cytokines) qui sont produits par les leucocytes résidents dans les nœuds. Ces cytokines agissent comme des signaux d’alerte généraux, alertant le corps de la menace potentielle et activant une variété de réactions immunitaires spécifiques.,
Structure
La structure d’un ganglion lymphatique n’est pas différente de celle de la rate. Chaque ganglion lymphatique est divisé en plusieurs régions:
- Capsule fibreuse-elle forme une gaine externe protectrice et a des trabécules qui s’étendent périodiquement dans le ganglion, le subdivisant en petits compartiments;
- Cortex externe (cortex nodulaire) – juste à l’intérieur de la marge capsulaire, il se compose de nombreux follicules riches en cellules B., Lorsque des agents pathogènes sont présents, ces follicules se dilatent pour révéler des centres germinaux proéminents contenant des cellules B qui se divisent activement et sécrètent des anticorps;
- Cortex interne (paracortex) – il se trouve juste en dessous du cortex externe et est particulièrement riche en lymphocytes T, qui circulent également continuellement dans la plupart des autres régions du nœud;
- Médulla-la partie interne centrale du nœud qui contient un grand nombre de macrophages phagocytaires fixes., Ceux-ci surveillent continuellement la lymphe pour les matières étrangères potentiellement pathogènes (un processus connu sous le nom d’immuno-surveillance), qu’ils phagocytent au contact.
Signification clinique
Au cours de l’infection, les cellules B productrices d’anticorps commencent à proliférer dans les centres germinaux, provoquant l’élargissement des ganglions lymphatiques affectés et devenant palpables et tendres. Certaines des cytokines libérées sont pyrogènes (ce qui signifie qu’elles provoquent de la fièvre) et agissent directement sur le centre thermorégulateur de l’hypothalamus pour augmenter la température corporelle., Comme la majorité des agents pathogènes humains se divisent de manière optimale à environ 37°C, cette augmentation de la température corporelle sert à ralentir la réplication bactérienne, ce qui permet au système immunitaire de traiter l’infection plus efficacement. Les ganglions lymphatiques enflés et la fièvre sont tous deux des signes sûrs que le corps monte une réponse immunitaire efficace contre l’agent pathogène incriminé; cela sera discuté plus en détail dans la partie 3 de cette série.
Autres lymphatique composants
d’Autres types de tissu lymphatique existent également., Le tissu lymphoïde associé à la muqueuse (MALT) est positionné pour protéger les voies respiratoires et gastro-intestinales de l’invasion par les microbes. Les éléments suivants sont constitués de MALT:
- Tissu lymphoïde associé à l’intestin;
- Tissu lymphoïde associé aux bronches;
- Les amygdales palatines, linguales et pharyngiennes.
Les amygdales sont des agrégats de tissu lymphatique stratégiquement situés pour empêcher les corps étrangers et les agents pathogènes de pénétrer dans le corps., Les amygdales palatines sont dans le pharynx, les amygdales linguales dans la cavité buccale et les amygdales pharyngiennes (végétations adénoïdes) sont à l’arrière de la cavité nasale; en conséquence, les amygdales elles-mêmes sont à haut risque d’infection et d’inflammation (amygdalite). Cette question sera également examinée plus en détail dans la partie 3.,> Le sang et les cellules immunitaires sont produits à l’intérieur de la moelle osseuse rouge, au cours d’un processus appelé hématopoïèse

- Testez vos connaissances avec l’auto-évaluation des temps de soins infirmiers après avoir lu cet article., Si vous obtenez un score de 80% ou plus, vous recevrez un certificat personnalisé que vous pourrez télécharger et stocker dans votre portefeuille NT en tant que preuve de DPC ou de revalidation.
- Prenez l’auto-évaluation des temps de soins infirmiers pour cet article
Arnott A et al (2018) Un registre pour les patients atteints d’asplénie/hyposplénisme réduit le risque d’infections par des organismes encapsulés. Clinique Des Maladies Infectieuses; 67: 4, 557-561.
Baković D et al (2005) Effet de l’homme de la rate contraction sur la variation de la circulation des globules. Expérimentale et clinique, la Pharmacologie et de la Physiologie; 32: 11, 944-951.
Bilder G (2016) Aggin Biologique humain: Des Macromolécules aux Systèmes d’organes. Wiley.
Garnitschnig L et al (2020) Dynamique postprandiale du volume splénique chez des volontaires sains. Rapports physiologiques; 8: 2, e14319.,
Gujar S et al (2017) Une étude cadavérique de la rate humaine et de sa signification clinique. Revue nationale d’Anatomie Clinique; 6: 1, 35-41.
Małkiewicz A, Dziedzic M (2012) Reconversion de la moelle osseuse: imagerie des changements physiologiques de la moelle osseuse. Journal polonais de radiologie; 77: 4, 45-50.
Pivkin IV et al (2016) Biomécanique des globules rouges dans la rate humaine et conséquences pour la physiologie et la maladie. Actes de l’Académie Nationale des Sciences des États-unis d’Amérique; 113: 28, 7804-7809.,
Severa M et al (2019) Thymosins dans la sclérose en plaques et ses modèles expérimentaux: le passage de la base à l’application clinique. Sclérose en plaques et troubles connexes; 27: 52-60.
Sherer Y et al (1999) La double relation entre la thymectomie et l’auto-immunité: le kaléidoscope de la maladie auto-immune. Dans: Paul S (ed) Réactions auto-immunes. Immunologie contemporaine. Totowa, NJ: Humana Press.
Stewart IB, McKenzie DC (2002) La rate humaine pendant le stress physiologique. Médecine sportive; 32: 6, 361-369.