Réactions de précipitation et règles de solubilité
Une réaction de précipitation est une réaction dans laquelle les substances dissoutes réagissent pour former un (ou plusieurs) produits solides. De nombreuses réactions de ce type impliquent l’échange d’ions entre des composés ioniques en solution aqueuse et sont parfois appelées réactions de double déplacement, de double remplacement ou de métathèse., Ces réactions sont courantes dans la nature et sont responsables de la formation de récifs coralliens dans les eaux océaniques et de calculs rénaux chez les animaux. Ils sont largement utilisés dans l’industrie pour la production d’un certain nombre de produits chimiques de base et de spécialité. Les réactions de précipitation jouent également un rôle central dans de nombreuses techniques d’analyse chimique, y compris les tests ponctuels utilisés pour identifier les ions métalliques et les méthodes gravimétriques pour déterminer la composition de la matière (voir le dernier module de ce chapitre).,
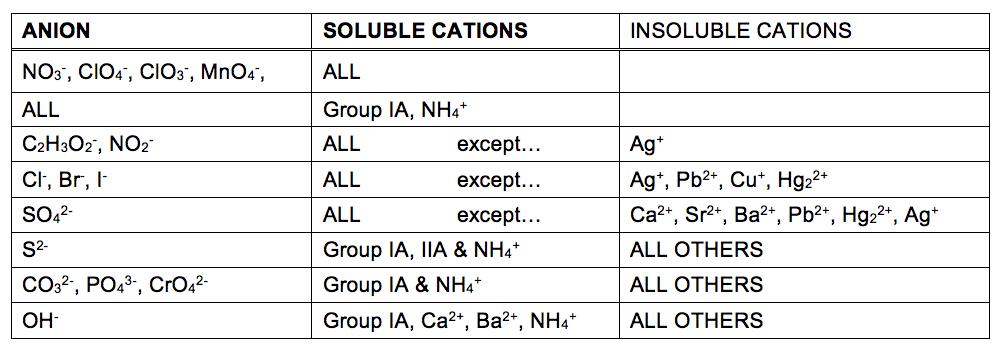
La mesure dans laquelle une substance peut être dissoute dans l’eau ou dans un solvant est exprimée quantitativement par sa solubilité, définie comme la concentration maximale d’une substance qui peut être atteinte dans des conditions spécifiées. Les substances ayant des solubilités relativement importantes sont dites solubles. Une substance précipitera lorsque les conditions de solution sont telles que sa concentration dépasse sa solubilité. Les substances ayant une solubilité relativement faible sont dites insolubles, et ce sont les substances qui précipitent facilement de la solution., Plus d’informations sur ces concepts importants sont fournies dans le texte chapitre sur les solutions. Pour prédire l’identité des solides formés par les réactions de précipitation, on peut simplement se référer aux schémas de solubilité qui ont été observés pour de nombreux composés ioniques (tableau 1).
Un exemple frappant de précipitation est observé lorsque des solutions d’iodure de potassium et de nitrate de plomb sont mélangées, entraînant la formation d’iodure de plomb solide:
Cette observation est conforme aux lignes directrices sur la solubilité: Le seul composé insoluble parmi toutes les personnes impliquées est l’iodure de plomb, une des exceptions à la solubilité générale des sels d’iodure.,
L’équation ionique nette représentant cette réaction est la suivante:
L’iodure de plomb est un solide jaune vif qui était autrefois utilisé comme pigment d’artiste connu sous le nom de jaune d’iode (Figure 1). Les propriétés des cristaux PbI2 purs les rendent utiles pour la fabrication de détecteurs de rayons X et gamma.

Le tableau de solubilité du tableau 1 peut être utilisé pour prédire si une réaction de précipitation se produira lorsque des solutions de composés ioniques solubles sont mélangées. Il suffit d’identifier tous les ions présents dans la solution, puis d’envisager si possible l’appariement cation/anion pourrait entraîner un composé insoluble.
Par exemple, le mélange de solutions de nitrate d’argent et de fluorure de sodium donnera une solution contenant des ions Ag+, NO3−, Na+ et F−., Outre les deux composés ioniques présents à l’origine dans les solutions, AgNO3 et NaF, deux composés ioniques supplémentaires peuvent être dérivés de cette collection d’ions: NaNO3 et AgF.
Le tableau de solubilité indique que tous les sels de nitrate sont solubles, mais que l’AgF est l’une des exceptions à la solubilité générale des sels de fluorure. Une réaction de précipitation, par conséquent, est prévue pour se produire, comme décrit par les équations suivantes: