Objectifs d’apprentissage
- Décrire une molécule d’anticorps.
- Dessinez la structure » stick figure » de l’IgG, en indiquant la partie Fab (région variable) et la partie Fc (région constante).
- Indiquer les fonctions des parties Fab et Fc d’un anticorps.
- Indiquer ce que l’on entend par l’activité biologique d’un anticorps.
- Comparez la structure des IgM et des IgA sécrétoires avec celle des IgG.
Dans cette section, nous nous pencherons sur la structure des anticorps., Il existe cinq classes ou isotypes d’anticorps humains:
- immunoglobuline G (IgG),
- immunoglobuline M (IgM),
- immunoglobuline A (IgA),
- immunoglobuline D (IgD) et
- immunoglobuline E (gE).
Les anticorps les plus simples, tels que les IgG, les IgD et lesgE, sont des macromolécules en forme de « Y »appelées monomères. Un monomère est composé de quatre glycoprotéine chaînes: deux chaînes lourdes identiques et deux chaînes légères identiques. Les deux chaînes lourdes ont un poids moléculaire élevé qui varie avec la classe d’anticorps., Les chaînes légères sont disponibles en deux variétés: kappa ou lambda et ont un poids moléculaire plus faible que les chaînes lourdes. Les quatre chaînes de glycoprotéines sont reliées entre elles par des liaisons disulfure (S-S) et des liaisons non covalentes (Figure \(\PageIndex{1}\)).
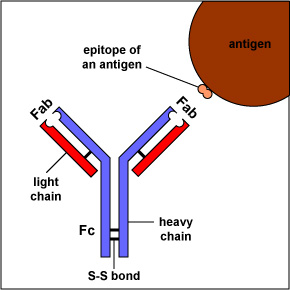
Des liaisons S-S supplémentaires replient les chaînes de glycoprotéines individuelles en un certain nombre de domaines globulaires distincts (Figure \(\PageIndex{2}\)). La zone où le haut du « Y » rejoint le bas s’appelle la charnière. Cette zone est flexible pour permettre à l’anticorps de se lier à des paires d’épitopes à différentes distances sur un antigène.
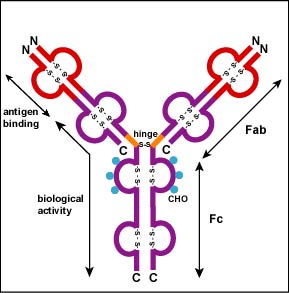
Les deux pointes du monomère » Y » sont appelées fragments de liaison à l’antigène ou parties Fab de l’anticorps (Figures 1-3)., Les 110 premiers acides aminés ou premier domaine de la chaîne lourde et légère de la région Fab de l’anticorps fournissent une spécificité pour la liaison d’un épitope sur un antigène. La séquence d’acides aminés de ce premier domaine de la chaîne légère et de la chaîne lourde présente d’énormes variations d’un anticorps à l’autre et constitue la région variable (région V)., En effet, chaque lymphocyte B, au début de son développement, devient génétiquement programmé par une série de réactions d’épissage de gènes pour produire un Fab avec une forme tridimensionnelle unique capable d’adapter un épitope avec une forme correspondante.
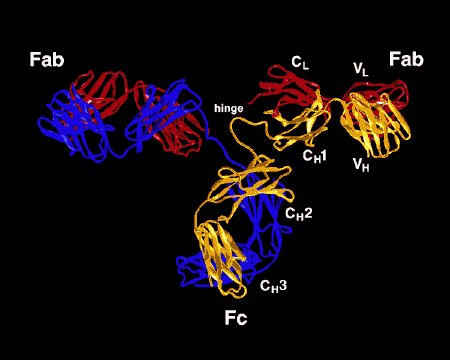
Figure \(\PageIndex{3}\): Dessin en ruban de la Molécule d’anticorps IgG2a, Dessin en ruban de la première molécule d’anticorps intacte jamais cristallisée (IgG2a). La partie Fab de l’anticorps présente une spécificité pour lier un épitope d’un antigène. La partie Fc dirige l’activité biologique de l’anticorps.,
Les différents gènes que les cellules épissent ensemble déterminent l’ordre des acides aminés de la partie Fab de la chaîne légère et lourde; la séquence d’acides aminés détermine la forme tridimensionnelle finale (Figure \(\PageIndex{4}\)). Par conséquent, différentes molécules d’anticorps produites par différents lymphocytes B auront différents ordres d’acides aminés aux extrémités de la Fab pour leur donner des formes uniques pour l’épitope de liaison. Le site de liaison à l’antigène est suffisamment grand pour contenir un épitope d’environ 5-7 acides aminés ou 3-4 résidus de sucre., Les épitopes se lient à la partie Fab de l’anticorps par des liaisons réversibles non covalentes.
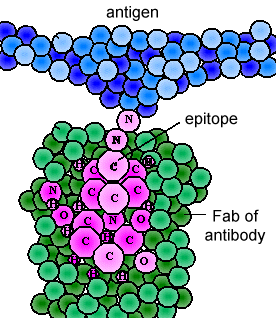
La partie inférieure du « Y », la région C terminale de chaque chaîne glycoprotéique, est appelée la partie Fc., La partie Fc, ainsi qu’un domaine de la chaîne lourde et légère de la région Fab a une séquence d’acides aminés constante et est appelée région constante (région C) de l’anticorps et définit la classe et la sous-classe de chaque anticorps. La partie Fc est responsable de l’activité biologique de l’anticorps (Figures 1-3), cependant, la partie Fc ne devient biologiquement active qu’après que le composant Fab s’est lié à son antigène correspondant., Selon la classe et la sous-classe d’anticorps, les activités biologiques de la partie Fc des anticorps comprennent la capacité de:
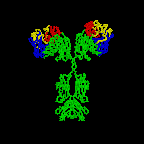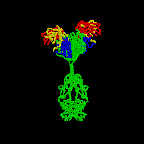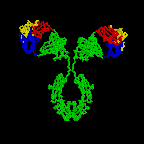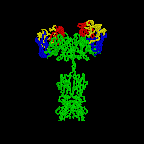
Les molécules d’anticorps individuelles en forme de « Y »sont appelées monomères et peuvent se lier à deux épitopes identiques. Les anticorps des classes IgG, IgD etgE sont des monomères.
Deux classes d’anticorps sont plus complexes., IgM (voir Figure \(\PageIndex{10}\)) est un pentamère, constitué de 5 molécules de type « Y »reliées à leurs parties Fc par une chaîne de jonction « J » ou. L’IgA sécrétoire (voir Figure \(\PageIndex{11}\)) est un dimère constitué de 2 molécules de type »Y « reliées à leurs parties Fc par une chaîne » J » et stabilisées pour résister à la digestion enzymatique dans les sécrétions corporelles au moyen d’un composant sécrétoire.
Résumé
- Il existe 5 classes ou isotypes d’anticorps ou d’immunoglobulines humaines: IgG, IgM, IgA, IgD etgE.,
- Les anticorps les plus simples, tels que les IgG, les IgD et lesgE, sont des macromolécules en forme de « Y »appelées monomères et sont composés de quatre chaînes glycoprotéiques: deux chaînes lourdes identiques et deux chaînes légères identiques.
- Les deux pointes du monomère « Y » sont appelées fragments de liaison à l’antigène ou parties Fab de l’anticorps et ces parties fournissent une spécificité pour la liaison d’un épitope sur un antigène.,
- Au début de son développement, chaque lymphocyte B devient génétiquement programmé par une série de réactions d’épissage de gènes pour produire un Fab avec une forme tridimensionnelle unique capable d’adapter un épitope à une forme correspondante.
- La partie Fc ne devient biologiquement active qu’après que le composant Fab s’est lié à son antigène correspondant. Les activités biologiques comprennent l’activation des voies du complément et la liaison aux récepteurs des phagocytes et d’autres cellules de défense pour favoriser l’immunité adaptative.
- L’IgM est un pentamère, constitué de 5 monomères joints à leurs parties Fc.,
- IgA est un dimère, constitué de 2 monomères réunis au niveau de leurs parties Fc.
Questions
Étudiez le matériel de cette section, puis écrivez les réponses à ces questions. Ne cliquez pas simplement sur les réponses et écrivez-les. Cela ne testera pas votre compréhension de ce tutoriel.
- Décrire une molécule d’anticorps. (ans)
- Correspond à ce qui suit:
_____ La région de l’anticorps qui fournit une spécificité pour lier un épitope sur un antigène., (ans)
_____ La région de l’anticorps qui est responsable de l’activité biologique des anticorps. (ans)
_____ Composé de quatre glycoprotéine chaînes. Il existe deux chaînes lourdes identiques ayant un poids moléculaire élevé et deux chaînes légères identiques. (ans)
_____ Un pentamère, constitué de 5 molécules de type « Y »reliées au niveau de leurs parties Fc par une chaîne de jonction « J » ou. (ans)
_____ Un dimère constitué de 2 molécules de type « Y »reliées à leurs parties Fc par une chaîne « J » et stabilisées pour résister à la digestion enzymatique., (ans)
- IgM
- les IgA sécrétoires
- IgG
- Fab
- Fc
- Choix Multiples (ans)
les Contributeurs et les Attributions
-
le Dr Gary Kaiser (COLLÈGE COMMUNAUTAIRE DU COMTÉ de BALTIMORE, CATONSVILLE CAMPUS)