12.7 Puskureita
Oppimisen Tavoitteet
- Määritä puskuri.
- tunnistaa puskurin kaksi komponenttia oikein.
Kuten edellä Kohdassa 12.4 ”Vahvat ja Heikot Hapot ja Emäkset ja Niiden Suolat”, heikkoja happoja ovat suhteellisen yleisiä, jopa elintarvikkeita syömme. Toisinaan kohtaamme kuitenkin voimakasta happoa tai emästä, kuten vatsahappoa, jonka voimakkaasti hapan pH on 1,7. Määritelmän, vahvat hapot ja emäkset voivat tuottaa suhteellisen suuri määrä H+ tai OH− – ioneja ja näin ollen on merkitty kemiallista toimintaa., Lisäksi hyvin pienet määrät vahvoja happoja ja emäksiä voivat muuttaa liuoksen pH: ta hyvin nopeasti. Jos 1 mL mahan happoa lisättiin verenkiertoon ja ei ole korjaava mekanismi olivat läsnä, pH verta laskisi noin 7,4 noin 4,7—pH, joka ei edistä edelleen elävä. Onneksi kehossa on mekanismi tällaisten dramaattisten pH-muutosten minimoimiseksi.
mekanismi liittyy bufferA ratkaisu, joka kestää dramaattisia muutoksia pH., ratkaisu, joka kestää dramaattisia muutoksia pH., Puskureita tehdä niin olemalla koostuu tiettyjä paria liuenneita aineita: joko heikkoa happoa ja suolaa, jotka on johdettu, että heikko happo tai heikko emäs sekä suola, että heikko pohja. Esimerkiksi puskuri voi koostua liuennut HC2H3O2 (heikko happo) ja NaC2H3O2 (suola johdettu, että heikko happo). Toinen esimerkki puskurista on liuos, joka sisältää NH3: n (heikko emäs) ja nh4cl: n (tästä heikosta emäksestä johdettu suola).
käyttäkäämme HC2H3O2 / NaC2H3O2-puskuria osoittaaksemme, miten Puskurit toimivat., Jos vahva pohja—lähde OH−(aq) – ioneja—on lisätä puskuriliuosta, ne OH− – ionit reagoivat HC2H3O2 happo-emäs reaktio:
HC2H3O2(aq) + OH−(aq) → H2O(ℓ) + C2H3O2−(aq)
sen Sijaan muuttamalla pH dramaattisesti tekemällä ratkaisu, laimentamaton, lisätty OH− – ionit reagoivat tehdä H2O, joten pH ei muutu paljon.
Jos vahva happo—lähde H+ – ioneja—on lisätä puskuriliuosta, H+ – ionit reagoivat anioni suolasta. Koska HC2H3O2 on heikko happo, se ei ionisoidu paljon., Tämä tarkoittaa, että jos paljon H+ – ioneja ja C2H3O2− ionit ovat läsnä samaan ratkaisuun, he tulevat yhdessä tehdä HC2H3O2:
H+(aq) + C2H3O2−(aq) → HC2H3O2(aq)
sen Sijaan muuttamalla pH dramaattisesti ja tehdä ratkaisu, hapan, lisätään H+ – ionit reagoivat tekemään molekyylejä heikko happo. Kuva 12.2 ”puskureiden toimet” kuvaa puskurin molempia toimia.
Kuva 12.2 Toimia Puskurit
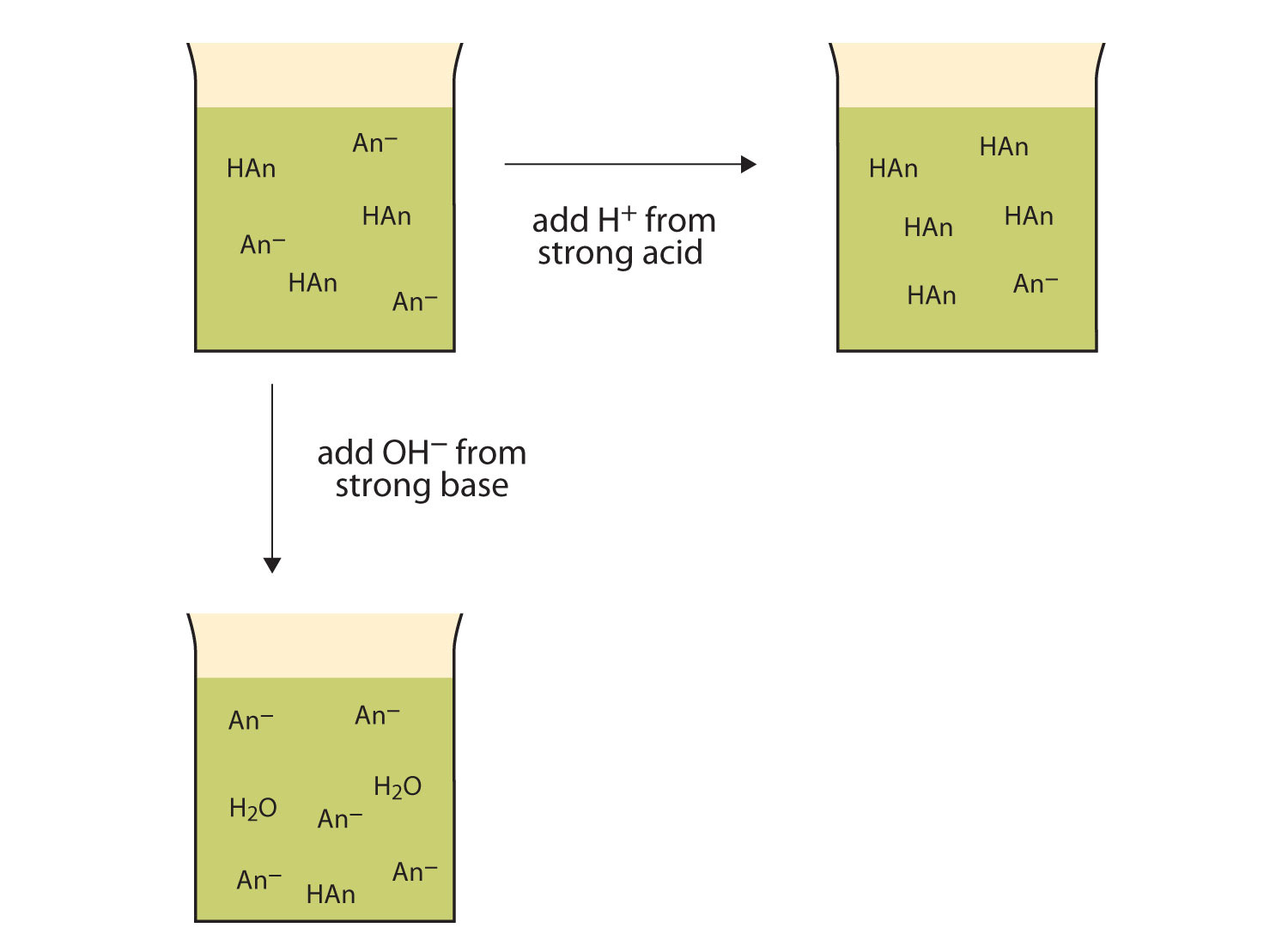
– Puskureita voi reagoida sekä vahvat hapot (top) ja vahvat emäkset (puoli) minimoida suuria muutoksia pH: ssa.,
heikoista emäksistä valmistetut Puskurit ja heikkojen emästen suolat toimivat samalla tavalla. Esimerkiksi puskuri sisältää NH3 ja NH4Cl -, NH3-molekyylit voivat reagoida ylimääräinen H+ – ioneja käyttöön vahvat hapot:
NH3(aq) + H+(aq) → NH4+(aq)
vaikka NH4+(aq) ioni voi reagoida tahansa OH− ioneja käyttöön vahvat emäkset:
NH4+(aq) + OH−(aq) → NH3(aq) + H2O(ℓ)
Esimerkki 15
mitkä yhdistelmät yhdisteitä voi tehdä puskuriliuos?,
- HCHO2 ja NaCHO2
- HCl: a ja NaCl: a
- CH3NH2 ja CH3NH3Cl
- NH3: a ja NaOH
Ratkaisu
- HCHO2 on muurahais-happo, heikko happo, kun taas NaCHO2 on suolaa valmistettu anioni heikko happo (formaatti ion ). Näiden kahden aineen tekisi puskuriliuosta.
- HCl on vahva happo, ei heikko happo, joten näiden kahden aineen ei tehdä puskuriliuosta.
- CH3NH2 on metyyliamiinia, joka on NH3: n kaltainen ja jonka yksi sen H-atomeista on substituoitu CH3-ryhmällä. Koska sitä ei ole lueteltu taulukossa 12.,2 ”Vahvat hapot ja emäkset”, voimme olettaa, että se on heikko pohja. Yhdiste CH3NH3Cl on suolaa, valmistettu, että heikko pohja, joten näiden kahden aineen tekisi puskuriliuosta.
- NH3 on heikko pohja, mutta NaOH on vahva pohja. Näiden kahden soluten yhdistelmä ei tekisi puskuriliuosta.
Testaa Itsesi
mitkä yhdistelmät yhdisteitä voi tehdä puskuriliuos?,
- NaHCO3: a ja NaCl: a
- H3PO4 ja NaH2PO4
- NH3 ja (NH4)3PO4
- NaOH: a ja NaCl: a
Vastauksia
- ei
- kyllä
- kyllä
- ei
Puskurit toimivat hyvin vain rajoitetun määriä lisätään vahvaa happoa tai emästä. Kun jompikumpi soluutti on täysin reagoitu, liuos ei ole enää puskuri, ja pH: ssa voi tapahtua nopeita muutoksia. Sanomme, että puskuri on tietty kapasiteettisuuri määrä vahvaa happoa tai pohja puskuri voi torjua.., Puskurit, joilla on enemmän solute liuennut niihin aluksi on suurempi kapasiteetti, kuten voidaan odottaa.
Ihmisen veri on puskurointi järjestelmä vähentää äärimmäisiä muutoksia pH: ssa. Yksi puskuri verta perustuu läsnäolo HCO3− ja H2CO3 . Tämän puskurin läsnä, vaikka jotkut vatsa happo oli löytää tiensä suoraan verenkiertoon, muuttaa pH verta olisi minimaalinen. Monien elimistön solujen sisällä on fosfaatti-ioneihin perustuva puskurijärjestelmä.,
Ruoka ja Juoma App: Happo, Joka Helpottaa Kipua
Vaikka lääkkeet eivät ole täsmälleen ”ruoka ja juoma” meillä nielemään niitä, joten katsotaanpa katsomaan happoa, joka on luultavasti yleisin lääkkeitä: asetyylisalisyylihappo, joka tunnetaan myös nimellä aspiriini. Aspiriini on tunnettu kipulääke ja kuumetta alentava aine.
aspiriinin rakenne on esitetty oheisessa kuvassa. Happoosa on ympyröity; juuri siinä osassa oleva h-atomi voidaan luovuttaa aspiriinin toimiessa Brønsted-Lowry-happona. Koska sitä ei ole esitetty taulukossa 12.,2″ vahvoja happoja ja emäksiä”, asetyylisalisyylihappo on heikko happo. Kuitenkin, se on edelleen hapan, ja kun otetaan huomioon, että jotkut ihmiset kuluttavat suhteellisen suuria määriä aspiriinia päivittäin, sen hapan luonne voi aiheuttaa ongelmia vatsassa vuori, vaikka vatsa puolustuskykyä vastaan oman mahan happoa.
Kuva 12.3 molekyylirakenne Aspiriini
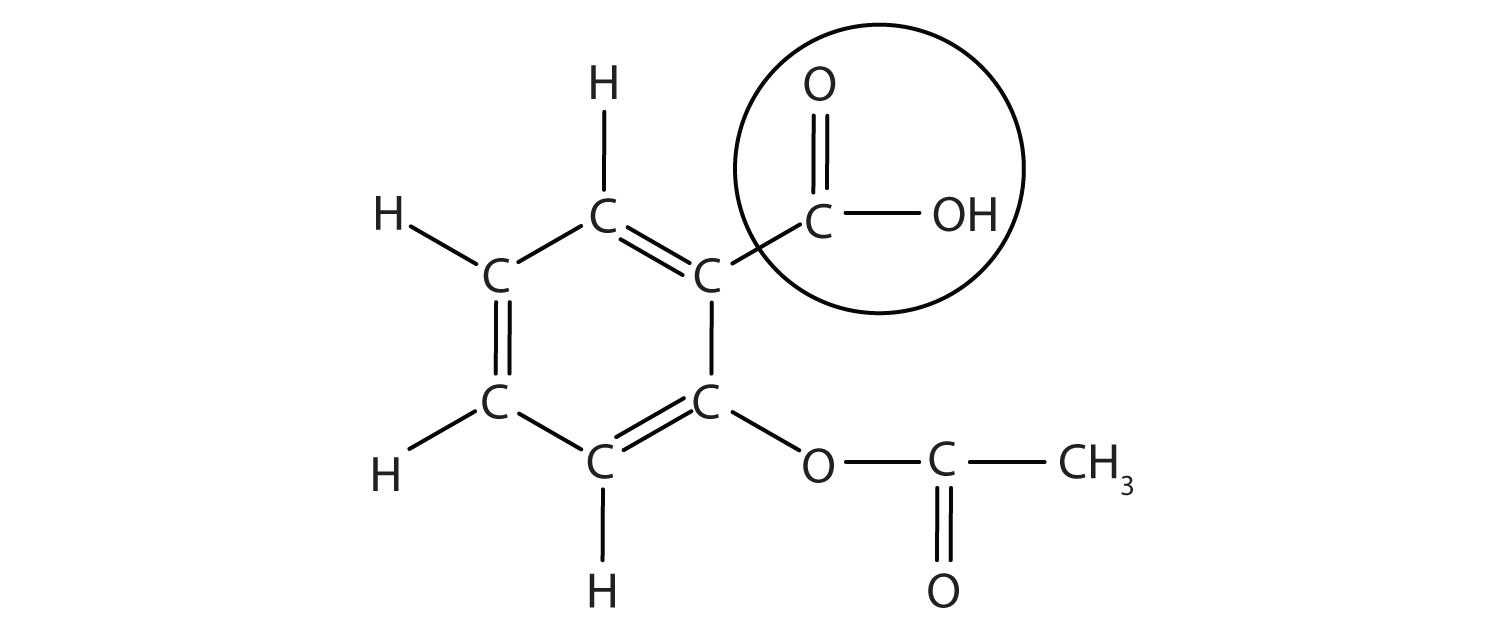
kiersi atomit ovat happo osa molekyylin.
koska aspiriinin happoominaisuudet voivat olla ongelmallisia, monet aspiriinimerkit tarjoavat lääkkeestä ”puskuroidun aspiriinin” muodon., Näissä tapauksissa, aspiriini sisältää myös puskuroida agentti—yleensä MgO—, joka säätelee happamuutta aspiriini vähentää sen hapan sivuvaikutuksia.
yhtä hyödyllinen ja yleinen kuin aspiriini on, sitä markkinoitiin virallisesti lääkkeenä vuodesta 1899 alkaen. Yhdysvaltain elintarvike-ja lääkevirasto FDA perustettiin vasta vuonna 1906., Jotkut ovat väittäneet, että jos FDA oli muodostettu ennen kuin aspiriini otettiin käyttöön, aspiriini voi koskaan saanut hyväksynnän, koska sen mahdollisia sivuvaikutuksia—ruoansulatuskanavan verenvuoto, korvien soiminen, Reyen oireyhtymä (maksasairaus), ja jotkut allergisia reaktioita. Kuitenkin viime aikoina aspiriini on mainostetut sen vaikutuksia vähentää sydänkohtauksia ja aivohalvauksia, joten on todennäköistä, että aspiriini on tullut jäädäkseen.
Key Takeaway
- puskuri on ratkaisu, joka kestää äkillisiä muutoksia pH: ssa.
Harjoitukset
-
Määritä puskuri., Mitä kahta toisiinsa liittyvää kemiallista komponenttia tarvitaan puskurin tekemiseen?
-
Voiko puskuria tehdä yhdistämällä vahva happo vahvaan emäseen? Miksi tai miksi ei?
-
mitkä yhdisteiden yhdistelmät voivat tehdä puskurin? Oletetaan vesiliuokset.
- HCl: a ja NaCl: a
- HNO2 ja NaNO2
- NH4NO3 ja HNO3
- NH4NO3-ja NH3
-
mitkä yhdistelmät yhdisteitä voi tehdä puskuri? Oletetaan vesiliuokset.,
- H3PO4 ja Na3PO4
- NaHCO3: a ja Na2CO3: a
- NaNO3-ja Ca(NO3)2
- HN3-ja NH3
-
jokaisen yhdistelmä Harjoitus 3, joka on puskuri, kirjoita kemialliset yhtälöt reaktioita puskurin osia, kun vahva happo ja vahva emäs lisätään.
-
jokaisen yhdistelmä Harjoitus 4, joka on puskuri, kirjoittaa kemiallisia yhtälöitä varten reaktioita puskurin osia, kun vahva happo ja vahva emäs lisätään.,
-
täydellinen fosfaattipuskuria järjestelmä perustuu neljään aineita: H3PO4, H2PO4−, HPO42− ja PO43−. Mitä erilaisia puskuriliuoksia näistä aineista voidaan tehdä?
-
Selitä, miksi NaBr voi olla osa joko happamassa tai perus puskuri.
-
on tehty kaksi liuosta, jotka sisältävät samat soluuttipitoisuudet. Yksi ratkaisu koostuu H3PO4 ja Na3PO4, kun taas toinen koostuu HCN ja NaCN. Minkä ratkaisun pitäisi olla suurempi kapasiteetti puskurina?,
-
on tehty kaksi liuosta, jotka sisältävät samat soluuttipitoisuudet. Yksi ratkaisu koostuu NH3 ja NH4NO3, kun taas toinen koostuu H2SO4 ja Na2SO4. Minkä ratkaisun pitäisi olla suurempi kapasiteetti puskurina?
Vastauksia
-
puskuri on yhdistelmä heikko happo tai emäs ja suola, että heikko happo tai emäs.,
-
-
- ei
- kyllä
- ei
- kyllä
-
-
3b: vahva happo: NO2− + H+ → HNO2; vahva pohja: HNO2 + OH− → NO2− + H2O; 3d: vahva pohja: NH4+ + OH− → NH3 + H2O; vahva happo: NH3 + H+ → NH4+
-
-
– Puskureita voidaan tehdä kolme yhdistelmiä: (1) H3PO4-ja H2PO4−, (2) H2PO4− ja HPO42−, ja (3) HPO42− ja PO43−. (Teknisesti puskuri voidaan tehdä mistä tahansa kahdesta komponentista.,)
-
-
fosfaattipuskuria pitäisi olla suurempi kapasiteetti.
-