fondo
principio: la síntesis de aspirina a partir de ácido salicílico se produce por proceso de acetilación en medio ácido. El ácido salicílico interactúa con el anhídrido acético en presencia de pocas gotas de ácido sulfúrico concentrado para producir aspirina y una molécula de ácido acético., El propósito de agregar ácido sulfúrico (catalizador) es ayudar y aumentar el proceso de separar el ion acetato (CH3COO–) del anhídrido acético que finalmente se asocia con el ion H+ del grupo hidroxilo fenólico en ácido salicílico para ser eliminado como mol de ácido acético.1
objetivo: preparar aspirina a partir de ácido salicílico.,
la Reacción:
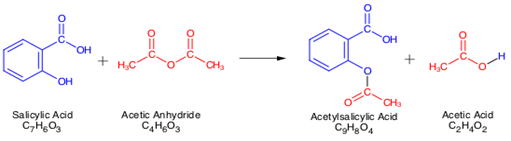
Mecanismo:
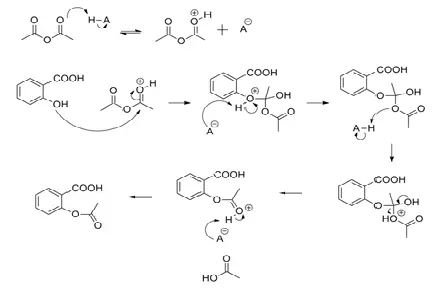
Uso:
Utilizado para el alivio de los dolores de menor importancia/dolores y también el dolor leve a moderado. Se recomienda para la artritis y las condiciones artríticas relacionadas, profilaxis del infarto de miocardio. Reduce el riesgo de ataques isquémicos transitorios en los hombres.,
REQUIREMENTS
Chemicals: Salicylic acid – 6 g
Acetic anhydride – 8.,5 ml
Concentrated H2SO4 – 3-4 drops
Methylated spirit
Apparatus: Conical flask – 250 ml
Buchner funnel
Glass rod
Beaker
Filter paper
PROCEDURE
Weigh 6 gs of salicylic acid and transfer it to a clean and dry 250 ml conical flask. Add 8.,5 ml de anhídrido acético y 3-4 gotas de ácido sulfúrico concentrado en el matraz cuidadosamente y mezclar bien. Calentar la mezcla en baño de agua a 60 grados aproximadamente 20 min con agitación frecuente. Dejar enfriar el contenido del matraz y verter en 100 ml de agua fría en un vaso de precipitados de 250 ml con agitación constante. Filtrar el producto crudo en un embudo Buchner por succión, lavar con agua fría. Recristalizar a partir de agua hirviendo junto con pequeñas cantidades de alcohol metilado. Secar el producto sintetizado en un horno a 90 ° C y calcular el rendimiento.,
cálculo
Aquí el reactivo limitante es el ácido salicílico; por lo tanto, el rendimiento debe calcularse a partir de su cantidad tomada.
la fórmula Molecular del ácido salicílico = C7H6O3
la fórmula Molecular del ácido acetilsalicílico (aspirina) = C9H8O4
peso Molecular del ácido salicílico = 138 g/mol
peso Molecular de ácido acetil salicílico (aspirina) = 180 g/mol
rendimiento Teórico:
138 g de ácido salicílico da 180 g de aspirina
por lo Tanto, 6 g de ácido salicílico va a dar ? (X) g de aspirina
X =( 180 × 6)/138 = 7.,82 g
rendimiento Teórico = 7.82 g
Práctica rendimiento = —– g
el% de Rendimiento = (Práctica Rendimiento)/(Rendimiento Teórico) x 100
CONCLUSIÓN
Aspirina fue sintetizado y el rendimiento fue encontrado para ser — %. (El producto se obtiene como cristales incoloros, rendimiento 11 g y m. p. 136-137 °C.)