Introducción
uno de los descubrimientos más importantes en el campo de la microscopía fluorescente se encontró en una medusa en la década de 1960. Osamu Shimomura de la Universidad de Princeton estaba estudiando Aequorea victoria, una medusa bioluminiscente., Debe señalarse aquí que la luminiscencia no es lo mismo que la fluorescencia:
- luminiscencia: la emisión espontánea de luz de una sustancia (cuando esa sustancia es un animal, se denomina bioluminiscencia)
- fluorescencia: la emisión de luz de una sustancia que ha absorbido la luz y se excita
a través del estudio de A. victoria, se descubrieron dos proteínas principales: aequorina (una fotoproteína) y proteína fluorescente verde (GFP). La medusa produce calcio, que interactúa con la aequorina y produce luminiscencia azul., Esta luz azul es absorbida por GFP y reemitida como fluorescencia verde. Estas proteínas se han aislado y purificado de las medusas y se utilizan en gran medida en la investigación hasta el día de hoy. Por esta investigación, Osamu Shimomura y sus colegas ganaron el Premio Nobel de Química en 2008.
Green Fluorescent Protein
la GFP es excitada por la luz en la porción azul/violeta / ULTRAVIOLETA del espectro y emite luz en la porción verde (de ahí el nombre). La estructura de la proteína se puede ver en la Fig.1., GFP es una forma del barril con la porción fluorescente (el cromóforo) hecha de apenas tres aminoácidos. Cuando este cromóforo absorbe la luz azul, emite fluorescencia verde.
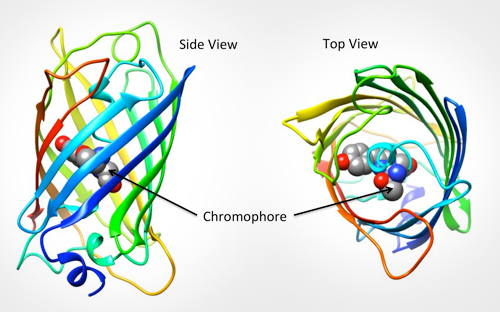
GFP en la investigación
el uso de GFP en la investigación se hizo evidente una vez que el gen para GFP también fue aislado y GFP podría ser añadido a las células o genéticamente injertado en organismos vivos. Algunas aplicaciones y ventajas de GFP se discuten a continuación.
GFP como marcador de toxicidad: debido al hecho de que GFP disminuye en intensidad de fluorescencia con toxicidad creciente, puede ser utilizado como marcador para la toxicidad ambiental., GFP se puede agregar a los organismos huéspedes sin efecto negativo, y luego la intensidad rastreada a través de diferentes ambientes en varios organismos.
GFP es heredable, si un organismo tiene GFP noqueado en su genoma, GFP se pasará naturalmente a la descendencia sin ningún proceso adicional, lo que permite formas no invasivas de introducir un marcador fluorescente y rastrearlo a través de generaciones de animales o células. GFP no interfiere con ningún proceso biológico., Los ratones transgénicos pueden ser etiquetados con GFP, que luego se observa fácilmente en sus crías simplemente exponiéndolos a la luz azul o UV, como se ve en la Fig.2.
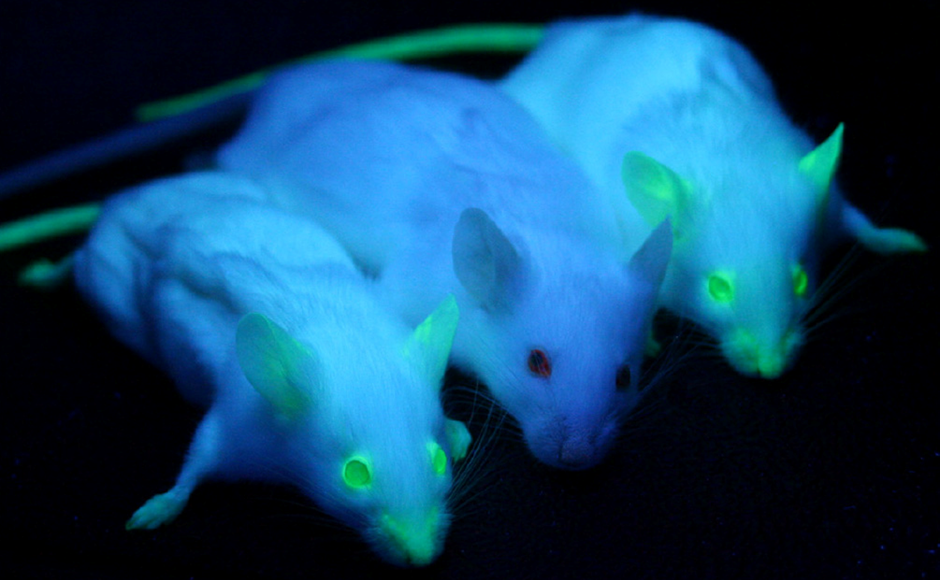
GFP se puede fusionar a otras proteínas, haciendo efectivamente esas proteínas fluorescentes. Esto se puede hacer con enlazadores especiales para que la GFP no afecte la función de la proteína de interés, y todavía puede difundirse a través de las células. Esto permite que cualquier proteína sea localizada y rastreada usando microscopía fluorescente estándar, al brillar una luz azul en las células, la proteína de interés volverá a fluorescer con una luz verde.,
GFP en experimentos con células vivas: la molécula fluorescente verde clásica es el isotiocianato de fluoresceína (FITC), pero esto es tóxico para las células y no se puede usar directamente sin reparar primero las células o causar daños inevitables. GFP es mucho menos dañino pues es una proteína natural y se puede utilizar en experimentos en células vivas mientras que no causa virtualmente ningún daño, especialmente si se pasa encendido a la descendencia.
GFP en aplicaciones de microscopía avanzada., Varias aplicaciones de microscopía de fluorescencia, como la recuperación de fluorescencia después del fotoblanqueo (FRAP) y la transferencia de energía de resonancia de Förster (FRET) se desarrollaron con GFP, lo que permite a los investigadores utilizar aplicaciones de fluorescencia cada vez más específicas y poderosas para sus imágenes. Estas técnicas se describen en otros artículos cortos, a saber, ¿qué es FRET y qué es FRAP?
la GFP es modificable, ya que el código genético y de aminoácidos para la GFP se entiende bien, ha estado sujeta a varias modificaciones., En primer lugar, GFP se modificó para producir GFP mejorado (eGFP), que ha aumentado la intensidad de fluorescencia, mayor fotoestabilidad, picos de excitación más convenientes y una mayor eficiencia a temperatura ambiente. Las modificaciones directamente en el cromóforo permiten que GFP fluore con diferentes colores, creando azul (BFP), cian (CFP), amarillo (yfp), rojo (RFP) y otros, todos los cuales se han mejorado por separado y tienen sus propias aplicaciones. Algunas modificaciones destacadas incluyen mCherry (rojo), Citrino y Venus (amarillo), y cerúleo (Cian) para nombrar algunos., Ahora existen familias enteras de proteínas fluorescentes, todas derivadas de la GFP original, como se ve en la Fig.3.
resumen
El GFP es una parte fundamental de la microscopía de fluorescencia debido a la facilidad de uso y las aplicaciones están limitadas solo por la imaginación del investigador. Las mejoras constantes en GFP a lo largo del tiempo han causado que la microscopía de fluorescencia y la investigación avancen, debido a la naturaleza altamente flexible de GFP y el gran cuerpo de investigación basado en el uso de GFP y sus muchas variantes.