US Pharm. 2010; 35 (8): HS2-HS4.
el Staphylococcus aureus resistente a la meticilina (SARM) es una de las principales causas de infecciones adquiridas tanto en la atención médica como en la comunidad.1,2 las infecciones por SARM están asociadas con un alto riesgo de morbilidad y mortalidad y conllevan altos costos de atención médica.3-5 la incidencia de infecciones por SARM en los Estados Unidos ha aumentado constantemente en los últimos años del 22% en 1995 al 60% en 2003.,6 el SARM asociado a la atención médica (SARM-HA) está relacionado con hospitales y centros de atención a largo plazo y es común en pacientes con hospitalización prolongada, uso previo de antimicrobianos, úlceras de decúbito, diálisis, catéteres permanentes, alimentación enteral o antecedentes de abuso de drogas intravenosas.7,8 en los últimos años, sin embargo, ha habido un aumento en una nueva cepa de SARM llamada SARM asociada a la comunidad (CA-SARM)., Esto parece adquirirse en el entorno ambulatorio, y la transmisión es a través del contacto físico cercano, como en guarderías, reservas indias e instalaciones correccionales y entre atletas, personal militar y hombres que tienen relaciones sexuales con hombres.7,9,10
distinguiendo cepas MRSA
varios informes han revelado diferencias entre cepas HA-MRSA y CA-MRSA, incluyendo la presencia de diferentes genotipos entre las dos cepas. CA-MRSA es susceptible a varios antibióticos no beta-lactámicos, mientras que las cepas de Ha-MRSA no lo son., Las cepas de CA-MRSA tienen más probabilidades de codificar ciertos factores virulentos que se han asociado con neumonía grave (especialmente en niños) e infecciones de la piel y tejidos blandos en adultos.8,11,12 el CDC ha establecido los criterios para diferenciar CA-MRSA de HA-MRSA. Estas pautas incluyen aislar un cultivo de SARM positivo dentro de las 48 horas posteriores a la admisión del paciente al hospital. Para ser considerado CA-MRSA, el paciente no debe tener ninguno de los siguientes: hospitalización reciente; admisión a un hogar de ancianos, hospicio o centro de enfermería especializada; diálisis; o cirugía reciente., El paciente tampoco debe tener catéteres permanentes u otros dispositivos médicos.13
El tratamiento de CA-MRSA
los CDC recomiendan que el manejo y la prevención de brotes de CA-MRSA incluya cubrir las infecciones que producen pus, lavarse las manos con frecuencia, no compartir artículos personales, lavar ropa sucia y ropa con agua caliente y secar paños en una secadora caliente en comparación con el secado al aire.13 para los abscesos cutáneos, el tratamiento incluye incisión y drenaje de los abscesos con o sin antibióticos sistémicos, dependiendo de la gravedad de la infección.,14
El tratamiento de CA-MRSA generalmente incluye el uso de agentes como clindamicina, tetraciclinas y trimetoprim-sulfametoxazol (TMP-SMX). El antibiótico rifampicina nunca debe utilizarse como monoterapia para el tratamiento del SARM. La resistencia se desarrolla rápidamente con la rifampicina en monoterapia; sin embargo, cuando se usa en combinación con otro agente anti-MRSA, puede erradicar los organismos de los sitios portadores de manera más efectiva.15 los antibióticos mencionados anteriormente suelen ser opciones de tratamiento viables en pacientes tratados de forma ambulatoria., En las infecciones graves que requieren hospitalización, los antibióticos intravenosos que incluyen vancomicina, linezolid, quinupristina-dalfopristina, daptomicina, tigeciclina y telavancina son terapias apropiadas que se pueden usar (tabla 1).
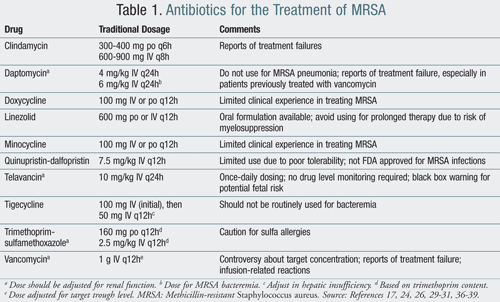
aunque la clindamicina (Cleocin) podría usarse para CA-MRSA, se ha informado que la resistencia es de hasta 19% en pacientes tratados con ella. Por lo tanto, los pacientes tratados con clindamicina deben ser monitorizados más estrechamente para el desarrollo de resistencia autoinducida.,16 La clindamicina también se ha asociado con el desarrollo de infecciones por Clostridium difficile, limitando su uso durante un período prolongado.17
TMP-SMX (Bactrim) puede considerarse una alternativa al tratamiento con vancomicina en algunos casos de infecciones por SARM. Sin embargo, al igual que con la clindamicina, se han notificado casos de fracaso del tratamiento. Esta terapia también tiene un uso limitado debido a la alta incidencia de alergias a las sulfonamidas, que se han reportado que ocurren en hasta el 10% de la población.,18
la minociclina (Minocin) y la doxiciclina (Vibramicina) son antibióticos de tetraciclina que se han utilizado para el tratamiento del SARM. Estos fármacos solo tienen Datos limitados sobre su uso en MRSA, pero se ha informado de éxito clínico.19
tratamiento de HA-MRSA
los antibióticos parenterales se consideran el estándar de oro para el tratamiento de HA-MRSA. Durante varias décadas, el antibiótico glicopéptido vancomicina ha sido ampliamente utilizado.
vancomicina (Vancocin) inhibe la síntesis de la pared celular; sin embargo, tiene una actividad bactericida más lenta in vitro., Con su uso excesivo, ha habido informes de susceptibilidades reducidas y la aparición de heteroresistencia a vancomicina en s aureus.20,21 el aumento de una subpoblación de s aureus con una concentración mínima inhibitoria (CMI) de >2 mcg/mL a vancomicina (conocida como fluencia de la CMI) se asocia con fracaso microbiológico y clínico. El National Committee for Clinical Laboratory Standards (NCCLS) ha propuesto nuevos puntos de corte para vancomicina, cambiando la CMI para «susceptible» de ≤4 mcg/mL a ≤2 mcg/mL.,22 la justificación de esta propuesta se basa en parte en observaciones clínicas anecdóticas de fracasos del tratamiento durante el tratamiento con dosis estándar de vancomicina en pacientes con CMI de 4 mcg/mL. Además, pueden requerirse niveles valle más altos (es decir, niveles Valle de 15-20 mcg/mL) para infecciones graves como neumonía y osteomielitis debido a la escasa penetración tisular de la vancomicina. Ha habido algunos informes anecdóticos de posible nefrotoxicidad asociada con estos niveles Valle altos.,
Jeffres et al presentaron un resumen en la Conferencia Interscience sobre agentes antimicrobianos y quimioterapia (ICAAC) de 2006 que revisó el riesgo de nefrotoxicidad con niveles Valle de vancomicina más altos.23 en su estudio, notificaron un riesgo de nefrotoxicidad del 30% (definido como un aumento de 0,5 mg/dL o un aumento del 50% de la creatinina sérica desde el valor basal) en pacientes con niveles Valle de vancomicina de 315 mcg/mL en comparación con el 13% en pacientes con niveles Valle <15 mcg/mL.23 algunas poblaciones de pacientes tienen un mayor riesgo de desarrollar nefrotoxicidad inducida por vancomicina., Estos incluyen factores de riesgo conocidos como la edad avanzada, estar críticamente enfermo, tener una función renal más baja y el uso concomitante de otros agentes nefrotóxicos como aminoglucósidos. Todos estos factores han llevado a un aumento en la necesidad y el uso de los agentes más nuevos.
Linezolid (Zyvox) es la primera oxazolidinona aprobada para el tratamiento de infecciones de la piel y tejidos blandos, bacter-emia y neumonía comunitaria y nosocomial causada por SARM.24 inhibe el inicio de la síntesis de proteínas en el ribosoma de los años 50; sin embargo, a diferencia de la mayoría de los otros fármacos, es un agente bacteriostático., Las ventajas de su uso incluyen la disponibilidad de una formulación oral que tiene excelentes propiedades de biodisponibilidad, sin que se justifique un ajuste de dosis en pacientes con insuficiencia renal, incluidos aquellos que reciben tratamientos de reemplazo renal. Un factor limitante de su uso, especialmente durante la duración prolongada del tratamiento, es la mielosupresión entre los pacientes que recibieron linezolid durante más de 14 días.24,25 aunque disponible como una formulación oral, no se utiliza tanto en el entorno ambulatorio debido a su costo., Tampoco está cubierto por muchas pólizas de seguro, por lo que los pacientes pueden necesitar usar los programas de asistencia al paciente del fabricante.
La daptomicina (Cubicin), un antibiótico lipopéptido con actividad bactericida rápida, está aprobada para el tratamiento de infecciones complicadas de la piel y tejidos blandos, así como bacteriemia causada por MRSA.26 Su mecanismo de acción implica la despolarización de la pared celular bacteriana. Los efectos secundarios de la daptomicina incluyen elevación de la creatina quinasa (CK) y rabdomiolisis, especialmente en pacientes que toman inhibidores concurrentes de la HMG-CoA reductasa (estatinas)., Por lo tanto, los niveles semanales de CK se deben extraer mientras que un paciente está recibiendo daptomicina. También debe tenerse en cuenta que se han notificado casos de resistencia a la daptomicina por SARM, especialmente con uso prolongado y en pacientes con exposición previa a vancomicina.26-28 la daptomicina no debe utilizarse para el tratamiento de la neumonía por SARM porque su actividad es inhibida por surfactantes pulmonares.
La Quinupristina-dalfopristina (Synercid) es una estreptogramina que tiene actividad contra el SARM., Aunque no está aprobado por la FDA para su uso en infecciones por SARM, se usa en infecciones de la piel y tejidos blandos en pacientes que son intolerantes o fallan en el tratamiento con vancomicina. Debido a que este tratamiento ha sido mal tolerado por los pacientes, su uso es limitado en la práctica clínica.29 algunos de los principales eventos adversos incluyen hiperbilirrubinemia, mialgias y artralgias. En base a estos factores, este agente se usa solo como última opción cuando los pacientes han fallado o no pueden tolerar otros agentes.,
terapias más nuevas
tigeciclina (Tygacil) es el primer agente bacteriostático en la clase de antibióticos glicilciclina (un derivado sintético de la tetraciclina). Está indicado para el tratamiento de infecciones complicadas de la piel y la estructura de la piel (cSSSI), infecciones intrabdominales complicadas y neumonía adquirida en la comunidad causada por SARM.La tigeciclina no debe utilizarse de forma rutinaria para la bacteremia debido a la preocupación por alcanzar niveles séricos inadecuados., Debido a que la tigeciclina es un antibiótico de amplio espectro, su uso debe restringirse a infecciones graves y potencialmente mortales en pacientes hospitalizados.
Telavancina (Vibativ) es el medicamento más nuevo aprobado por la FDA para el tratamiento de infecciones por SARM.31 es un lipoglicopéptido similar a la vancomicina, aunque su mecanismo de acción difiere. La telavancina altera la permeabilidad de la membrana celular por despolarización de la membrana plasmática, aumentando la permeabilidad y fuga de trifosfato adeno-sinusoidal celular y potasio (K+)., El tiempo de estos cambios se correlaciona con la pérdida rápida, dependiente de la concentración de la viabilidad bacteriana, lo que sugiere que la actividad bactericida temprana de telavancina resulta de la disipación del potencial de membrana celular y un aumento en la permeabilidad de la membrana.
Los estudios clínicos han demostrado que telavancina no es inferior a vancomicina en el tratamiento de la cSSSI.32,33 una ventaja que tiene telavancina sobre la vancomicina es la dosificación una vez al día y no es necesario monitorizar los niveles del fármaco. Sin embargo, al igual que la vancomicina, la dosis debe ajustarse en pacientes con insuficiencia renal.,Se debe monitorizar la función Renal durante y después de la interrupción del tratamiento en todos los pacientes. Telavancina se asocia con la prolongación del QTc y se debe utilizar con precaución en pacientes con medicamentos que también podrían prolongar el QTc. En ensayos clínicos que compararon telavancina con vancomicina, las reacciones adversas notificadas en más del 10% de los pacientes tratados con telavancina incluyeron alteración del gusto, náuseas, vómitos y orina espumosa.31 se notificaron acontecimientos adversos graves en el 7% de los pacientes tratados con telavancina y los más frecuentes fueron acontecimientos renales, respiratorios o cardíacos., Hay una advertencia de caja negra sobre el riesgo fetal asociado con el uso de telavancina; por lo tanto, las mujeres en edad fértil deben hacerse una prueba de embarazo en suero antes de comenzar a usar telavancina.31
Ceftobiprole (Zeftera) es la primera cefalosporina con actividad bactericida contra MRSA. Su actividad antibacteriana incluye la inhibición de las proteínas de unión a la penicilina involucradas en la síntesis de la pared celular. En los ensayos clínicos, fue tan eficaz como la combinación de vancomicina y ceftazidima en el tratamiento de la ICSS.,34 en general, es bien tolerado, con los principales eventos adversos del medicamento, incluyendo náuseas y alteraciones del gusto. Ceftobiprol no está aprobado actualmente para su uso en los EE.UU., y aunque fue aprobado previamente para su uso en Canadá, el fabricante suspendió la venta del medicamento a partir del 16 de abril de 2010.35 esto fue siguiendo las recomendaciones de los organismos reguladores en Europa (Comité Europeo de medicamentos de uso humano) y los EE.UU. (FDA) para no aprobar el medicamento., Aunque los resultados de la fase III sugirieron un beneficio de ceftobiprol, hubo preocupaciones en cuanto a la integridad de estos resultados del estudio debido a la manipulación de los datos clínicos de algunos de los sitios del estudio. Con este reciente desarrollo, el futuro del uso de ceftobiprol en el mercado estadounidense sigue siendo cuestionable.
conclusión
con la aparición de SARM-CA y SARM hetero-resistente, es importante que los farmacéuticos estén familiarizados con todos los agentes disponibles para el tratamiento de las infecciones por SARM. También es esencial elegir el agente antimicrobiano adecuado para la infección que se está tratando., Además, los agentes con un espectro de actividad más amplio (p. ej., tigeciclina) deben reservarse para infecciones muy graves y en el contexto de infecciones por múltiples patógenos. También es de suma importancia reservar los nuevos agentes para infecciones más graves con el fin de minimizar el desarrollo de resistencia.
1. Boucher HW, Corey GR. Epidemiology of methicillin-resistant Staphylococcus aureus. Clin Infect Dis.
2. Styers D, Sheehan DJ, Hogan P, et al., Laboratory-based surveillance of current antimicrobial resistance patterns and trends among Staphylococcus aureus: 2005 status in the United States. Ann Clin Microbiol Antimicrob. 2006;5:2.3. Chien JW, Kucia ML, Salata RA. Uso de linezolid, una oxazolidinona, en el tratamiento de infecciones bacterianas grampositivas multirresistentes. Clin Infect Dis. 2000;30:146-151.
4. Soriano A, Martinez JA, Mensa J, et al. Importancia patogénica de la resistencia a la meticilina en pacientes con bacteremia por Staphylococcus aureus. Clin Infect Dis. 2000;30:368-673.
5. Graffunder EM, Venezia RA., Factores de riesgo asociados con la infección nosocomial por Staphylococcus aureus resistente a la meticilina (SARM), incluido el uso previo de antimicrobianos. J Antimicrob Chemother. 2002;49:999-1005.
6. Klevens RM, Edwards JR, Tenover FC, et al. Changes in the epidemiology of methicillin-resistant Staphylococcus aureus in intensive care units in US hospitals, 1992-2003. Clin Infect Dis.
7. Levine DP, Cushing RD, Jui J, Brown WJ. Endocarditis por Staphylococcus aureus resistente a la meticilina adquirida en la comunidad en el Centro Médico de Detroit. Ann Intern Med. 1982;97:330-338.
8., Lodise TP Jr, McKinnon PS, Rybak M. Prediction model to identify patients with Staphylococcus aureus bacteremia at risk for methicillin resistance. Control De Infecciones Hosp Epidemiol. 2003;24:655-661.
9. King MD, Humphrey BJ, Wang YF, et al. Aparición del clon Staphylococcus aureus USA 300 resistente a la meticilina adquirido en la comunidad como causa predominante de infecciones de piel y tejidos blandos. Ann Intern Med. 2006;144:309-317.10. Centros para el Control y la prevención de enfermedades., Infecciones por Staphylococcus aureus resistentes a meticilina entre participantes de deportes competitivos-Colorado, Indiana, Pennsylvania y el Condado de Los Ángeles, 2000-2003. MMWR. 2003;52:793-795.11. Lowy FD. Infecciones por Staphylococcus aureus. N Engl J Med. 1998;339:520-532.12. Chambers HF. La epidemiología cambiante de Staphylococcus aureus? Emerg Infect Dis.13. Información de SARM asociada a la comunidad para médicos. CDC. www.cdc.gov/ncidod/dhqp/ar_ 2008; 46 (suppl 5): S344-S349. 2006;42:389-391. 2001;7:178-182.mrsa_ca_clinicians.HTML. Consultado El 4 De Julio De 2010.14. Rybak MJ, LaPlante KL., Staphylococcus aureus resistente a la meticilina asociado a la comunidad; una revisión. Farmacoterapia. 2005;25:74-85.15. Gorwitz RJ, Jernigan DB, Powers JH, et al. Estrategias para el manejo clínico del SARM en la comunidad: resumen de una reunión de expertos convocada por los Centros para el Control y la prevención de enfermedades. March 2006. www.cdc.gov/ncidod/dhqp/pdf/ar/CAMRSA_ExpMtgStrategies.pdf. Consultado el 4 de julio de 2010.16. Sabol KE, Echevarria KL, Lewis JS II. Community-associated methicillin-resistant Staphylococcus aureus: new bug, old drugs. Ann Pharmacother. 2006;40:1125-1133.17., Cleocin (clindamicina) prospecto. New York, NY: Pfizer Inc; November 2005.18. Strom BL, Schinnar R, Apter AJ, et al. Ausencia de sensibilidad cruzada entre los antibióticos sulfonamidas y los no antibióticos sulfonamidas. N Engl J Med. 2003;349:1628-1635.19. Nicolau DP, Freeman CD, Nightingale CH, et al. Minociclina versus vancomicina para el tratamiento de endocarditis experimental causada por Staphylococcus aureus resistente a oxacilina. Agentes Antimicrob Chemother. 1994;38:1515-1518.20. Sakoulas G, Moellering RC Jr., Aumento de la resistencia a los antibióticos entre cepas de Staphylococcus aureus resistentes a la meticilina. Clin Infect Dis. 2008; 46 (suppl 5): S360-S367.21. Rybak MJ, Akins RL. Aparición de Staphylococcus aureus resistente a la meticilina con resistencia intermedia a los glicopéptidos: importancia clínica y opciones de tratamiento. Droga. 201;61:1-7.22. Tenover FC, Moellering RC Jr. the rationale for revising the Clinical and Laboratory Standards Institute vancomycin minimal inhibitory concentration interpretative criteria for Staphylococcus aureus. Clin Infect Dis. 2007;44:1208-1215.23., Jeffres MN, Micek ST, Isakow W, et al. Aumento de la incidencia de nefrotoxicidad con concentraciones mínimas séricas de vancomicina más altas. Program and abstracts of the 46th Interscience Conference on Antimicrobial Agents and Chemotherapy (ICAAC); September 27-30, 2006; San Francisco, CA. Abstract K789.24. Prospecto de Zyvox (linezolid). New York, NY: Pfizer Inc; December 2009.25. Kuter DJ, TILLOTSON GS. Efectos hematológicos de los antimicrobianos, un enfoque en la oxazolidinona, linezolid. Farmacoterapia. 201;21:1010-1013.26. Cubicin (daptomicina) prospecto., Lexington, MA: Cubist Pharmaceuticals; January 2010.
27. Murthy MH, Olson ME, Wickert RW, et al. Daptomycin non-susceptible methicillin-resistant Staphylococcus aureus USA 300 isolate. J Med Microbiol. 2008;57:1036-1038.
28. Mangili A, Bica I, Snydman R, Hamer DH. Daptomycin-resistant methicillin-resistant Staphylococcus aureus bacteremia. Clin Infect Dis. 2005;40:1058-1060.
29. Synercid (quinupristin-dalfopristin) package insert. Greenville, NC: Monarch Pharmaceuticals; June 2008.
30. Tygacil (tigecycline) package insert. Philadelphia, PA: Wyeth Pharmaceuticals; September 2009.,31. Prospecto de vibativ (telavancina). Deerfield, IL: Astellas Pharma US, Inc; septiembre de 2009.32. Stryjewski ME, Chu VH, O’Riordan WD, et al. Telavancina versus terapia estándar para el tratamiento de infecciones complicadas de la piel y de la estructura de la piel causadas por bacterias gram positivas: estudio FAST 2. Agentes Antimicrob Chemother. 2006;50:862-867.33. Corey GR. Estudios de telavancina en cSSSI. Paper presented at: Third International Symposium on Resistant Gram-Positive Infections; October 10, 2006; Niagara-on-the-Lake, Canada.34. Vidaillac C, Rybak MJ., Ceftobiprole: first cephalosporin with activity against methicillin-resistant Staphylococcus aureus. Pharmacotherapy. 2009;29:511-525.
35. Discontinuation of the sale of ceftobiprole in Canada. Basilea Pharmaceutica. April 9, 2010. http://hugin.info/134390/R/1401931/356785.pdf. Accessed July 12, 2010.
36. Vibramycin (doxycycline) package insert. New York, NY: Pfizer Inc; April 2007.
37. Minocin (minocycline) package insert. Philadelphia, PA: Triax Pharmaceuticals; March 2006.
38. Bactrim (trimethoprim-sulfamethoxazole) package insert. Philadelphia, PA: AR Scientific; November 2006.
39., Vancocin (vancomycin) package insert. Exton, PA: ViroPharma Inc; October 2005.